题目内容
1.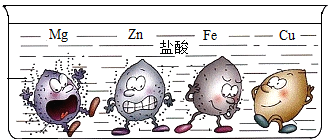 教材上有一幅很形象的卡通画表示金属与盐酸的反应现象.卡通人物表示一种金属,周围的小黑点表示反应中生成的气体,如图所示:
教材上有一幅很形象的卡通画表示金属与盐酸的反应现象.卡通人物表示一种金属,周围的小黑点表示反应中生成的气体,如图所示:(1)从图中可知金属与酸反应的基本规律是①排在H前面的金属能与酸反应生成H2;②排在H后面的金属,不能与酸反应生成H2.
(2)甲同学欲用其它方法验证铜、铁、镁的活动性顺序,他已经选择了打磨过的铁丝,你认为他还需要选的另外两种溶液是CuSO4溶液和MgSO4溶液.(填化学式)
(3)锌锰电池中有二氧化锰,随意丢弃会造成污染,工业上常利用金属铝的还原性回收锰,在高温下生成锰单质和另外一种氧化物,写出化学方程式4Al+3MnO2 $\frac{\underline{\;高温\;}}{\;}$2Al2O3+3Mn.
分析 (1)根据卡通画观察得出结论;
(2)验证金属的活动性顺序一般遵循:三取中的原则,可以据此解答;
(3)根据题目信息找出反应物和生成物写出反应的方程式.
解答 解:(1)从图中可以看出,排在H前面的金属能与酸反应生成H2,排在H后面的金属,不能与酸反应生成H2;
(2)根据铜、铁、镁的金属活动性顺序可以知道在有铁丝的情况下来验证这三种金属的活动性顺序应选择硫酸铜溶液和硫酸镁溶液;
(3)工业上利用铝和二氧化锰反应生成氧化铝和金属锰,化学方程式:4Al+3MnO2 $\frac{\underline{\;高温\;}}{\;}$2Al2O3+3Mn;
故答案为:(1)能与酸反应生成H2;
(2)CuSO4;MgSO4;
(3)4Al+3MnO2 $\frac{\underline{\;高温\;}}{\;}$2Al2O3+3Mn.
点评 本题考查学生对于金属活动性顺序的探究,在解答该类题目时要求我们熟练的掌握金属的活动顺序的应用,然后据此应用来进行解答.

练习册系列答案
相关题目
12.氢化钙固体是登山运动员常用的能源提供剂.某探究小组的同学通过查阅资料得知,氢化钙(CaH2)与水反应生成氢氧化钙和氢气.
请写出该反应的化学方程式:CaH2+2H2O=Ca(OH)2+2H2↑
探究小组的同学把一定量的CaH2加入碳酸钠溶液中,充分反应后过滤,得到滤渣和滤液,经检验滤渣的成分是碳酸钙.
【提出问题】滤液中溶质的成分是什么?
【猜想与假设】猜想一:氢氧化钠、碳酸钠、氢氧化钙
猜想二:氢氧化钠、碳酸钠
猜想三:氢氧化钠,氢氧化钙
猜想四:氢氧化钠
经过讨论,大家一致认为猜想猜想一不合理,请用化学方程式说明原因:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
【实验验证】
【反思与拓展】
①若向氯化铵的浓溶液中加一定量CaH2,充分反应,产生的气体是NH3,H2;
②登山运动员常用CaH2作为能源提供剂,与氢气相比,其优点是固体便于携带.
【定量分析】
探究小组的同学称取氢化钙样品的质量为10g,加入碳酸钠溶液中(假设氢化钙样品中的杂质不反应),充分反应后过滤、洗涤、烘干,得到滤渣质量为20g,试计算氢化钙样品中氢化钙的质量分数.(要求写出计算过程)
请写出该反应的化学方程式:CaH2+2H2O=Ca(OH)2+2H2↑
探究小组的同学把一定量的CaH2加入碳酸钠溶液中,充分反应后过滤,得到滤渣和滤液,经检验滤渣的成分是碳酸钙.
【提出问题】滤液中溶质的成分是什么?
【猜想与假设】猜想一:氢氧化钠、碳酸钠、氢氧化钙
猜想二:氢氧化钠、碳酸钠
猜想三:氢氧化钠,氢氧化钙
猜想四:氢氧化钠
经过讨论,大家一致认为猜想猜想一不合理,请用化学方程式说明原因:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
【实验验证】
| 实验 | 现象 | 结论 |
| 实验一:取滤液,向其中滴入少量碳酸钠溶液 | 无明显现象 | 猜想猜想三不成立 |
| 实验二:另取滤液,向其中加入足量稀盐酸 | 有气泡产生 | 猜想二成立 |
①若向氯化铵的浓溶液中加一定量CaH2,充分反应,产生的气体是NH3,H2;
②登山运动员常用CaH2作为能源提供剂,与氢气相比,其优点是固体便于携带.
【定量分析】
探究小组的同学称取氢化钙样品的质量为10g,加入碳酸钠溶液中(假设氢化钙样品中的杂质不反应),充分反应后过滤、洗涤、烘干,得到滤渣质量为20g,试计算氢化钙样品中氢化钙的质量分数.(要求写出计算过程)
16.除去下列物质中的少量杂质,所选试剂及操作都正确的是( )
| 序号 | 物质 | 杂质 | 试剂 | 操作 |
| A | CO | CO2 | 足量NaOH溶液 | 洗气 |
| B | CO2 | HCl | 足量NaOH溶液 | 洗气 |
| C | NaOH溶液 | Na2CO3 | 适量CaCl2溶液 | 过滤 |
| D | Fe粉 | CuO | 过量盐酸 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
6.某同学在实验室用三支试管分别取适量的稀盐酸、澄清石灰水、碳酸钠溶液,进行相关实验探究:
步骤1:向三支试管中分别滴加酚酞,Na2CO3溶液中显红色,则Na2CO3溶液显碱性;
步骤2:该同学把步骤1三支试管中的溶液同时倒入一只烧杯中,发现有气泡产生,最终有沉淀生成且溶液显红色;
步骤3:把烧杯中的混合物进行过滤,所得滤液中一定不含有原3种物质中的稀盐酸;(填物质名称)
(1)提出部分假设.步骤3所得滤液中溶质可能为:
假设①:NaCl Na2CO3; 假设②:NaCl CaCl2和NaOH;
假设③:NaCl Na2CO3和NaOH; 假设④:NaCl CaCl2和Na2CO3.
上述假设中,你认为不合理的假设是④(填序号),理由是CaCl2+Na2CO3═CaCO3↓+2NaCl(用化学方程式表示).
(2)完成实验方案.请填写与表中结论相符的实验现象.(提示CaCl2溶液显中性)
(3)反思评价.有同学提出将CaCl2溶液改为稀盐酸,若观察到有气泡产生且红色消失,则证明猜想③成立.小明同学认为不正确,其理由是无法确定溶液中是否存在氢氧化钠.
步骤1:向三支试管中分别滴加酚酞,Na2CO3溶液中显红色,则Na2CO3溶液显碱性;
步骤2:该同学把步骤1三支试管中的溶液同时倒入一只烧杯中,发现有气泡产生,最终有沉淀生成且溶液显红色;
步骤3:把烧杯中的混合物进行过滤,所得滤液中一定不含有原3种物质中的稀盐酸;(填物质名称)
(1)提出部分假设.步骤3所得滤液中溶质可能为:
假设①:NaCl Na2CO3; 假设②:NaCl CaCl2和NaOH;
假设③:NaCl Na2CO3和NaOH; 假设④:NaCl CaCl2和Na2CO3.
上述假设中,你认为不合理的假设是④(填序号),理由是CaCl2+Na2CO3═CaCO3↓+2NaCl(用化学方程式表示).
(2)完成实验方案.请填写与表中结论相符的实验现象.(提示CaCl2溶液显中性)
| 实验操作 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,加入足量CaCl2溶液,振荡 | 猜想③成立 |
10.同素异形体是同种元素组成的不同形态的单质,如碳元素就有金刚石、石墨、无定形碳等同素异形体,下列互为同素异形体的一组物质是( )
| A. | 氧气与臭氧 | B. | 水银与银 | C. | 干冰与冰 | D. | 氢气与液氢 |

 铜、铁、铝是我们生活中常见的金属.
铜、铁、铝是我们生活中常见的金属.