题目内容
11. 铜、铁、铝是我们生活中常见的金属.
铜、铁、铝是我们生活中常见的金属.(1)上述三种金属元素在地壳中的含量由多到少的顺序依次是铝、铁、铜.
(2)铝制品具有良好的抗腐蚀性能,是因为常温下,铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步被氧化.
(3)新制备的灰黑色极细铁粉暴露在空气中能点燃迅速燃烧生成红色的三氧化二铁粉末,试写出该反应的化学方程式4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3.
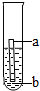
(4)丽丽同学从生活中发现,在潮湿的空气中铁比铜更容易锈蚀,由此她认为铁的金属活动性比铜强,她想通过如图实验来进一步证明.若图中A为金属铁,你认为B可能是硫酸铜溶液(其他合理的铜盐溶液也可)(填一种)溶液.
分析 (1)根据地壳中各元素含量的排序进行分析解答;
(2)根据铝的化学性质,在常温下,铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步被氧化;
(3)根据信息可知铁在不同的条件与氧气反应的生成物不同,根据信息写出反应的方程式;
(4)根据金属活动顺序的意义结合金属的化学性质进行分析解答.
解答 解:(1)地壳含量较多的元素(前五种)因此三种金属元素按含量从高到低的排序为:铝、铁、铜,故填:铝、铁、铜;
(2)在常温下,铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步被氧化;故填:常温下,铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步被氧化;
(3)铁粉在空气中生成三氧化二铁,故反应的方程式为:4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3;
(4)根据金属活动性顺序,位于前面的金属能把位于后面的金属从它们的盐溶液里置换出来,因此B可以是硫酸铜溶液;故填:硫酸铜溶液(其他合理的铜盐溶液也可).
点评 本题考查学生根据在常温下铝与空气氧气反应,铁丝在氧气中燃烧和金属生锈与防锈的等知识进行分析解题的能力,属基础性知识考查题.

练习册系列答案
 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案
相关题目
2.下列实验操作叙述正确的是( )
| A. | 实验用剩的药品应放回原试剂瓶中 | |
| B. | 过滤时,将玻璃棒靠在三层滤纸的一边 | |
| C. | 测某酸性溶液的pH时,先用水将pH试纸润湿 | |
| D. | 把烧杯置于铁架台的铁圈上直接加热 |
19.某校组织同学们对水资源状况进行调查,调查报告中的观点错误的是( )
| A. | 我国各地水资源分布不均 | |
| B. | 水的问题加剧了淡水资源危机 | |
| C. | 节约用水是每个公民应尽的义务 | |
| D. | 地表71%是水,可用的淡水资源非常丰富 |
6. 鉴别硬水与软水常用肥皂水,为了达到实验目的应控制的实验条件有( )
鉴别硬水与软水常用肥皂水,为了达到实验目的应控制的实验条件有( )
①两试管中加入的肥皂水浓度
②两试管中加入的肥皂水的滴数
③两种水样品中可溶性钙镁化合物的浓度
④两试管中水样品的体积.
 鉴别硬水与软水常用肥皂水,为了达到实验目的应控制的实验条件有( )
鉴别硬水与软水常用肥皂水,为了达到实验目的应控制的实验条件有( )①两试管中加入的肥皂水浓度
②两试管中加入的肥皂水的滴数
③两种水样品中可溶性钙镁化合物的浓度
④两试管中水样品的体积.
| A. | ①② | B. | ①④ | C. | ①②③ | D. | ①②④ |
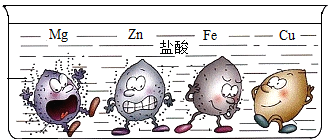 教材上有一幅很形象的卡通画表示金属与盐酸的反应现象.卡通人物表示一种金属,周围的小黑点表示反应中生成的气体,如图所示:
教材上有一幅很形象的卡通画表示金属与盐酸的反应现象.卡通人物表示一种金属,周围的小黑点表示反应中生成的气体,如图所示: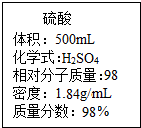 实验室有一瓶浓硫酸,瓶上标签如图,请根据标签上提供的数据解答下列问题.
实验室有一瓶浓硫酸,瓶上标签如图,请根据标签上提供的数据解答下列问题.