题目内容
9.53g质量分数为20%碳酸钠溶液与一定质量的氯化钙溶液恰好完全反应,生成10g沉淀,过滤后得滤液98.5g,求氯化钙溶液中氯化钙的质量分数.分析 根据质量守恒定律可以求算出氯化钙溶液的质量;根据氯化钙和碳酸钠反应的化学方程式结合生成的沉淀质量可以计算才固体混合物中氯化钙的质量;
解答 解:根据质量守恒定律可以求算出氯化钙溶液的质量为:10g+98.5g-53g=55.5g;
设氯化钙溶液中氯化钙的质量为x,
CaCl2+Na2CO3═CaCO3↓+2NaCl
111 100
x 10g
$\frac{111}{x}=\frac{100}{10g}$
x=11.1g
氯化钙溶液中氯化钙的质量分数=$\frac{11.1g}{55.5g}×$100%=20%
答案:氯化钙溶液中氯化钙的质量分数为20%
点评 要想解答好这类题目,首先,要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识等.然后,根据所给的问题情景或图表信息等,结合所学的相关知识和技能,细致地分析题意(或图表信息)等各种信息资源,并细心地探究、推理后,按照题目要求进行认真地选择或解答即可.

练习册系列答案
相关题目
20.有一种含碳酸钙的特殊纸张.为测定其中碳酸钙的含量,某课外活动小组的同学称取40g碎纸样品.分别在4只烧杯中进行了实验,实验数据见下表(假设纸张其它成分不溶于水,且不与水反应,生成的气体全部从溶液中逸出):
(1)求样品中碳酸钙的质量分数.
(2)烧杯④中物质充分反应后所得溶液的质量为43.36g.
| 烧杯 | 烧杯 | 烧杯 | 烧杯 | |
| 加入样品的质量/g | 10 | 10 | 10 | 10 |
| 加入稀盐酸的质量/g | 10 | 20 | 30 | 40 |
| 充分反应后生成气体的质量/g | 0.88 | 1.76 | 2.64 | 2.64 |
(2)烧杯④中物质充分反应后所得溶液的质量为43.36g.
17.下列实验操作叙述正确的是( )
| A. | 倾倒液体时,试剂瓶口紧挨着试管口快速倒入 | |
| B. | 加热蒸发过程中,当溶液蒸干时停止加热 | |
| C. | 用pH试纸测定溶液的酸碱度时,将pH试纸放入待测液中蘸取 | |
| D. | 过滤时,漏斗中液面低于滤纸的边缘 |
4.下列实验操作正确的是( )
| A. |  加热液体 | B. |  收集二氧化碳 | C. |  检查气密性 | D. |  取用固体 |
14.下列有关燃烧的说法不正确的是 ( )
| A. | 发生森林火灾要开辟隔离带,目的是清除可燃物 | |
| B. | 白磷保存在冷水中目的是为了隔绝氧气 | |
| C. | 将煤块制成蜂窝煤是为了使其燃烧更充分 | |
| D. | 用水灭火目的是为了降低可燃物的着火点 |
18. 小伟善于利用身边的物质巩固所学的知识,如图是他利用窗户进行的巩固性练习,请你用化学符号帮他填写完成各项内容:
小伟善于利用身边的物质巩固所学的知识,如图是他利用窗户进行的巩固性练习,请你用化学符号帮他填写完成各项内容:
A:Al;
B:Na+;
C:SiO2;
D:$\stackrel{+3}{Al}$2O3.
 小伟善于利用身边的物质巩固所学的知识,如图是他利用窗户进行的巩固性练习,请你用化学符号帮他填写完成各项内容:
小伟善于利用身边的物质巩固所学的知识,如图是他利用窗户进行的巩固性练习,请你用化学符号帮他填写完成各项内容:A:Al;
B:Na+;
C:SiO2;
D:$\stackrel{+3}{Al}$2O3.
19.某校组织同学们对水资源状况进行调查,调查报告中的观点错误的是( )
| A. | 我国各地水资源分布不均 | |
| B. | 水的问题加剧了淡水资源危机 | |
| C. | 节约用水是每个公民应尽的义务 | |
| D. | 地表71%是水,可用的淡水资源非常丰富 |
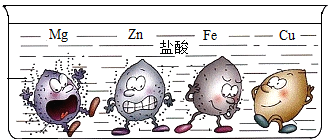 教材上有一幅很形象的卡通画表示金属与盐酸的反应现象.卡通人物表示一种金属,周围的小黑点表示反应中生成的气体,如图所示:
教材上有一幅很形象的卡通画表示金属与盐酸的反应现象.卡通人物表示一种金属,周围的小黑点表示反应中生成的气体,如图所示: