题目内容
9. 某班化学实验课进行酸碱盐的性质实验.
某班化学实验课进行酸碱盐的性质实验.【实验一】自制酸碱指示剂
(1)取少量紫包菜和白菜叶剪碎后分别在研钵中捣烂,加入酒精溶液浸泡;用纱布将浸泡出的汁液滤出,观察到紫包菜汁液为紫色,白菜汁液为无色.分别装好待用.
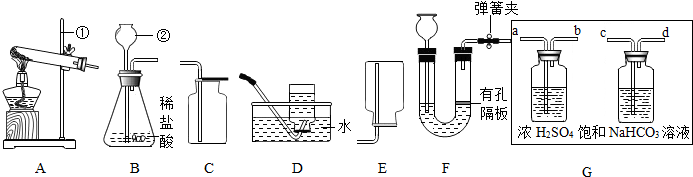
(2)取四支试管分别用NaOH溶液和稀盐酸进行实验,观察到现象如图.
记录如下:
| NaOH溶液 | 稀盐酸 | |
| 紫包菜汁液 | ①绿色 | ②红色 |
| 白菜汁液 | ③无色 | ④淡黄色 |
【实验二】探究碱和盐的性质
第一组学生进行CuSO4、NaOH溶液的反应,观察到的现象是有蓝色絮状沉淀生成,溶液颜色变浅;该反应的化学方程式为CuSO4+2NaOH=Na2SO4+Cu(OH)2↓.
第二组学生进行BaCl2、Na2CO3溶液的反应,反应的化学方程式为BaCl2+Na2CO3=BaCO3↓+2NaCl.
【实验三】废液再探究
结束后,两组同学将全部的废液集中倒进一个废液缸中.兴趣小组同学对废液进行过滤,得到无色滤液.
【提出问题】滤液中含有什么溶质?
【做出猜想】滤液中一定含有NaCl,还可能含有BaCl2、NaOH、Na2CO3、Na2SO4中的一种或几种.
【实验探究】
(1)取少量滤液加入试管中,滴加紫包菜汁液,溶液显绿色.
(2)继续加入足量的稀硫酸,溶液变成红色,无气泡和沉淀产生,则滤液中一定没有Na2CO3、BaCl2.
根据(1)(2)判断滤液中一定含有NaOH.
(3)为最终确定该滤液的组成,还需补充的实验是:另取少量滤液于试管中,滴加BaCl2溶液,观察到白色沉淀.
【实验结论】该无色滤液的组成为NaCl、NaOH、Na2SO4.
分析 根据物质的性质进行分析,适合做酸碱指示剂的物质应该在酸性和碱性溶液中显示不同的颜色,酸碱盐的溶液间若能两两交换成分生成水、气体或是沉淀,则反应能够进行,据此解答即可.
解答 解:(3)紫包菜汁液在稀盐酸中为红色,说明酸性溶液能使紫包菜汁液变红,在苹果汁中显示红色,故能说明苹果汁呈酸性,故填:酸;
【酸碱盐的性质】硫酸铜能与氢氧化钠反应生成氢氧化铜蓝色沉淀,故会观察到有蓝色絮状沉淀生成,溶液颜色变浅,该反应的化学方程式为:CuSO4+2NaOH=Na2SO4+Cu(OH)2↓;
氯化钡能与碳酸钠反应生成碳酸钡白色沉淀和氯化钠,故填:BaCl2+Na2CO3═BaCO3↓+2NaCl;
【做出猜想】滤液中一定含有NaCl,还可能含有BaCl2、NaOH、Na2CO3、Na2SO4中的一种或几种.
【实验探究
(2)稀硫酸能与氯化钡反应生成硫酸钡沉淀,能与碳酸钠反应生成二氧化碳,故含有氯化钡或是碳酸钠的猜想均不正确,溶液变成红色,说明含有NaOH;
(3)溶液呈碱性,且加入一种试剂能产生白色沉淀,则可能是加入了氯化钡溶液,与硫酸钠反应生成了硫酸钡沉淀,故填:另取少量滤液于试管中,滴加BaCl2溶液;
【实验结论】该无色滤液的组成为 Na2SO4、NaOH、NaCl.
答案:
(3)酸;
【酸碱盐的性质】有蓝色絮状沉淀生成,溶液颜色变浅; CuSO4+2NaOH=Na2SO4+Cu(OH)2↓;
BaCl2+Na2CO3=BaCO3↓+2NaCl
【做出猜想】NaCl;
【实验探究】(2)Na2CO3、BaCl2; NaOH
(3)另取少量滤液于试管中,滴加BaCl2溶液;
【实验结论】NaCl、NaOH、Na2SO4
点评 本题考查了酸碱指示剂的使用以及酸碱盐物质的判别及其有关的反应,完成此题,可以依据已有的知识进行.要求同学们熟练掌握常见物质的性质以及反应时的有关现象,以便灵活应用.

(1)甲同学在实验室里发现一瓶敞口放置的氢氧化钠溶液,对其变质情况进行了如下探究.
【猜想与假设】该氢氧化钠溶液已部分变质.
【实验与结论】
| 实验步骤 | 实验现象 | 实验结论 |
| a.取少量该溶液于一支试管中,加入足量的氯化钙溶液 | 有白色沉淀生成 | 该氢氧化钠溶液已变质 |
| b.将步骤a所得的液体过滤,取滤液于另一支试管中,滴加无色酚酞试液 | 酚酞试液变红 | 该氢氧化钠溶液已部分变质 |
向该溶液中加入氢氧化钙,反应后,经过滤操作,即可除去该氢氧化钠溶液中含有的杂质,写出该反应的化学方程式Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
(2)乙同学在实验室里发现少量部分变质的氢氧化钠固体,尝试通过实验测定其中碳酸钠的质量分数.
【设计和进行实验】乙同学设计了如图所示的实验装置(铁架台、铁夹等固定用装置已略去,碱石灰是固体氢氧化钠和生石灰的混合物),取10.0g待测样品,进行实验.
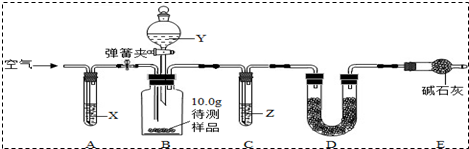
实验步骤如下:a.连接好装置,并检查气密性;b.打开弹簧夹,缓缓通入一段时间空气;c.称量装置D的质量为83.4g;d.关闭弹簧夹,慢慢滴加Y溶液,至不再产生气泡为止;e.打开弹簧夹,再次缓缓通入一段时间空气;f.再次称量装置D的质量为84.5g.
【交流讨论】
①试剂X、Y、Z依次最适宜选用C(选填字母).
A.氢氧化钠溶液浓盐酸浓硫酸B.澄清石灰水稀盐酸稀硫酸
C.氢氧化钠溶液稀硫酸浓硫酸D.浓硫酸稀硫酸氢氧化钠溶液
②步骤e中通入空气的作用是将B中产生的二氧化碳全部赶到D装置中.
③若没有装置C,则会导致测定结果偏大(选填“偏大”、“偏小”或“无影响”,下同);若没有装置E,则会导致测定结果偏大.
【数据处理】根据实验中测得的有关数据,计算部分变质的氢氧化钠固体中碳酸钠的质量分数26.5%.
| A. | 硝酸铵溶于水吸收大量的热,食盐溶于水也吸收大量的热 | |
| B. | 氮肥氯化铵与碱研磨可放出氨气,氮肥尿素(CO(NH2)2)与碱研磨也能放出氨气 | |
| C. | 因为燃烧需要同时满足三个条件,所以灭火也要同时控制这三个条件 | |
| D. | 氢气与空气混合点燃可能爆炸,一氧化碳与空气混合点燃也可能爆炸 |
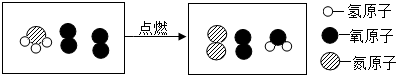
| A. | 该反应前的反应物中氮元素的化合价为-3价 | |
| B. | 该反应前后,分子的种类一定发生变化 | |
| C. | 该反应中参加反应的两种物质的质量比为17:23 | |
| D. | 该反应属于置换反应 |