题目内容
20.能源的合理利用与开发非常重要.(1)人们使用的燃料大多来自化石燃料,如煤、石油和天然气,它们是(填“可”或“不可”)不可再生资源.
(2)化石燃料主要含有碳、氢元素,大量使用化石燃料会产生过多的二氧化碳,能加剧温室效应.因燃料燃烧不充分而产生的空气污染物之一是一氧化碳.
(3)汽车常用石油分馏出来的石油或汽油做燃料,为减少汽车尾气污染,部分城市的公交车使用氢燃料电池,氢气被认为是清洁能源的原因是氢气燃烧产物只有水,不会造成污染.
分析 (1)天然气、煤、石油属于化石燃料,用完之后不能再产生,属于不可再生能源;
(2)根据化石燃料燃烧的产物分析;
(3)根据石油分馏出汽油、柴油等燃料分析;根据氢气燃烧的产物分析;
解答 解:(1)煤、石油、天然气都是化石燃料,属于不可再生能源,故填:天然气,不可再生;
(2)化石燃料燃烧时生成二氧化碳,能加剧温室效应,同时不完全燃烧还生成一氧化碳,造成空气污染;
(3)石油分馏出汽油、柴油等汽车燃料;氢气被认为是清洁能源的原因是它的燃烧产物只有水,不会造成污染;
故填:石油;不可;温室效应;一氧化碳;汽油;氢气燃烧产物只有水,不会造成污染.
点评 能源和环境问题是一个不能避免的问题,如何能够既实现了能源的合理利用,又能够不污染环境是目前人们需要解决的问题.

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目
10.在化学兴趣小组活动中,小山把一标有“生石灰 干燥剂”的小纸袋带到学校进行实验.干燥剂是否变质?小山设计并进行了如下实验,请你帮他完成实验报告.
(1)
(2))既然干燥剂中已有Ca(OH)2,小山又猜想还可能有另一种物质存在,原因是(用化学方程式表示)Ca(OH)2+CO2═CaCO3↓+H2O;如何检验这种物质的存在:取少量样品于试管中,滴入几滴稀盐酸,若有气泡产生则有CaCO3.
(1)
| 实验步骤 | 实验现象 | 结论 |
| ①取样于小试管中,加水,用手触摸试管外壁 | 试管发热 | 干燥剂中含有CaO |
| 取少量用样品制得的溶液于试管中,滴入几滴酚酞试液 | 溶液变红色 | 干燥剂中含有Ca(OH)2干燥剂部分变质 |
8.人体缺少某种元素会引起甲状腺肿大,该元素是( )
| A. | 锌 | B. | 碘 | C. | 钙 | D. | 硒 |
15.下列关于碳及其化合物的叙述,错误的是( )
| A. | 木炭具有吸附能力 | B. | 常温下碳的化学性质活泼 | ||
| C. | 一氧化碳具有可燃性 | D. | 二氧化碳作气体肥料 |
5. 如图是A、B、C三种物质(均不含结晶水)的溶解度曲线,下列说法错误的是( )
如图是A、B、C三种物质(均不含结晶水)的溶解度曲线,下列说法错误的是( )
 如图是A、B、C三种物质(均不含结晶水)的溶解度曲线,下列说法错误的是( )
如图是A、B、C三种物质(均不含结晶水)的溶解度曲线,下列说法错误的是( )| A. | t2℃时,C物质的饱和溶液能用降温的方法转化为不饱和溶液 | |
| B. | t1℃时,A、C物质饱和溶液中溶质的质量分数为25% | |
| C. | 分别将t2℃时A、B、C三种物质的饱和溶液降温至t1℃,此时溶液中溶质的质量分数由大到小的顺序是B>A>C | |
| D. | 当A中含有少量B时,可用降温结晶的方法提纯A |
9. 某班化学实验课进行酸碱盐的性质实验.
某班化学实验课进行酸碱盐的性质实验.
【实验一】自制酸碱指示剂
(1)取少量紫包菜和白菜叶剪碎后分别在研钵中捣烂,加入酒精溶液浸泡;用纱布将浸泡出的汁液滤出,观察到紫包菜汁液为紫色,白菜汁液为无色.分别装好待用.
(2)取四支试管分别用NaOH溶液和稀盐酸进行实验,观察到现象如图.
记录如下:
(3)再用苹果汁进行相同实验,紫包菜汁液变红色,白菜汁液变淡黄色.则苹果汁溶液显酸性.
【实验二】探究碱和盐的性质
第一组学生进行CuSO4、NaOH溶液的反应,观察到的现象是有蓝色絮状沉淀生成,溶液颜色变浅;该反应的化学方程式为CuSO4+2NaOH=Na2SO4+Cu(OH)2↓.
第二组学生进行BaCl2、Na2CO3溶液的反应,反应的化学方程式为BaCl2+Na2CO3=BaCO3↓+2NaCl.
【实验三】废液再探究
结束后,两组同学将全部的废液集中倒进一个废液缸中.兴趣小组同学对废液进行过滤,得到无色滤液.
【提出问题】滤液中含有什么溶质?
【做出猜想】滤液中一定含有NaCl,还可能含有BaCl2、NaOH、Na2CO3、Na2SO4中的一种或几种.
【实验探究】
(1)取少量滤液加入试管中,滴加紫包菜汁液,溶液显绿色.
(2)继续加入足量的稀硫酸,溶液变成红色,无气泡和沉淀产生,则滤液中一定没有Na2CO3、BaCl2.
根据(1)(2)判断滤液中一定含有NaOH.
(3)为最终确定该滤液的组成,还需补充的实验是:另取少量滤液于试管中,滴加BaCl2溶液,观察到白色沉淀.
【实验结论】该无色滤液的组成为NaCl、NaOH、Na2SO4.
 某班化学实验课进行酸碱盐的性质实验.
某班化学实验课进行酸碱盐的性质实验.【实验一】自制酸碱指示剂
(1)取少量紫包菜和白菜叶剪碎后分别在研钵中捣烂,加入酒精溶液浸泡;用纱布将浸泡出的汁液滤出,观察到紫包菜汁液为紫色,白菜汁液为无色.分别装好待用.
(2)取四支试管分别用NaOH溶液和稀盐酸进行实验,观察到现象如图.
记录如下:
| NaOH溶液 | 稀盐酸 | |
| 紫包菜汁液 | ①绿色 | ②红色 |
| 白菜汁液 | ③无色 | ④淡黄色 |
【实验二】探究碱和盐的性质
第一组学生进行CuSO4、NaOH溶液的反应,观察到的现象是有蓝色絮状沉淀生成,溶液颜色变浅;该反应的化学方程式为CuSO4+2NaOH=Na2SO4+Cu(OH)2↓.
第二组学生进行BaCl2、Na2CO3溶液的反应,反应的化学方程式为BaCl2+Na2CO3=BaCO3↓+2NaCl.
【实验三】废液再探究
结束后,两组同学将全部的废液集中倒进一个废液缸中.兴趣小组同学对废液进行过滤,得到无色滤液.
【提出问题】滤液中含有什么溶质?
【做出猜想】滤液中一定含有NaCl,还可能含有BaCl2、NaOH、Na2CO3、Na2SO4中的一种或几种.
【实验探究】
(1)取少量滤液加入试管中,滴加紫包菜汁液,溶液显绿色.
(2)继续加入足量的稀硫酸,溶液变成红色,无气泡和沉淀产生,则滤液中一定没有Na2CO3、BaCl2.
根据(1)(2)判断滤液中一定含有NaOH.
(3)为最终确定该滤液的组成,还需补充的实验是:另取少量滤液于试管中,滴加BaCl2溶液,观察到白色沉淀.
【实验结论】该无色滤液的组成为NaCl、NaOH、Na2SO4.
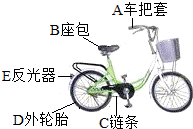 如图是同学们经常使用交通工具--自行车,请完成下列各题:
如图是同学们经常使用交通工具--自行车,请完成下列各题: