题目内容
4.玄武湖是南京著名的淡水湖.某同学对玄武湖的水样进行了相关的探究.(1)澄清透明的玄武湖水属于混合物(填“纯净物”或“混合物”).
(2)可以利用C(填字母)来测定湖水的酸碱度.
A.酚酞溶液 B.石蕊溶液 C.pH试纸
(3)检验湖水是软水还是硬水,可向水样中加入肥皂水,搅拌,观察现象.
(4)在日常生活中,常采用煮沸的方法降低水的硬度.
分析 区分硬水和软水的方法是:用肥皂水,加入肥皂水,泡沫多的是软水,泡沫少的是硬水;降低水的硬度的方法是:在生活中是加热煮沸,在实验室中是蒸馏.澄清透明的玄武湖水中也有可溶性杂质,属于混合物;可以利用pH试纸来测定湖水的酸碱度,
解答 解:(1)澄清透明的玄武湖水中也有可溶性杂质,属于混合物,故答案为:混合物;
(2)可以利用pH试纸来测定湖水的酸碱度,故答案为:C;
(3)区分硬水和软水的方法是:用肥皂水,加入肥皂水,泡沫多的是软水,泡沫少的是硬水,故答案为:肥皂水;
(4)降低水的硬度的方法是:在生活中是加热煮沸,故答案为:煮沸;
点评 本考点属于结合课本知识的信息,也体现了性质决定用途,用途反映性质的理念.还结合了新课标中的一个新的考点硬水与软水的区分,一定要加强记忆,综合应用.本考点主要出现在填空题和选择题中.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.下列关于碳及其化合物的叙述,错误的是( )
| A. | 木炭具有吸附能力 | B. | 常温下碳的化学性质活泼 | ||
| C. | 一氧化碳具有可燃性 | D. | 二氧化碳作气体肥料 |
19.下列化肥中,属于复合肥料的是( )
| A. | Ca(H2PO4)2 | B. | NH4NO3 | C. | K2SO4 | D. | NH4H2PO4 |
9. 某班化学实验课进行酸碱盐的性质实验.
某班化学实验课进行酸碱盐的性质实验.
【实验一】自制酸碱指示剂
(1)取少量紫包菜和白菜叶剪碎后分别在研钵中捣烂,加入酒精溶液浸泡;用纱布将浸泡出的汁液滤出,观察到紫包菜汁液为紫色,白菜汁液为无色.分别装好待用.
(2)取四支试管分别用NaOH溶液和稀盐酸进行实验,观察到现象如图.
记录如下:
(3)再用苹果汁进行相同实验,紫包菜汁液变红色,白菜汁液变淡黄色.则苹果汁溶液显酸性.
【实验二】探究碱和盐的性质
第一组学生进行CuSO4、NaOH溶液的反应,观察到的现象是有蓝色絮状沉淀生成,溶液颜色变浅;该反应的化学方程式为CuSO4+2NaOH=Na2SO4+Cu(OH)2↓.
第二组学生进行BaCl2、Na2CO3溶液的反应,反应的化学方程式为BaCl2+Na2CO3=BaCO3↓+2NaCl.
【实验三】废液再探究
结束后,两组同学将全部的废液集中倒进一个废液缸中.兴趣小组同学对废液进行过滤,得到无色滤液.
【提出问题】滤液中含有什么溶质?
【做出猜想】滤液中一定含有NaCl,还可能含有BaCl2、NaOH、Na2CO3、Na2SO4中的一种或几种.
【实验探究】
(1)取少量滤液加入试管中,滴加紫包菜汁液,溶液显绿色.
(2)继续加入足量的稀硫酸,溶液变成红色,无气泡和沉淀产生,则滤液中一定没有Na2CO3、BaCl2.
根据(1)(2)判断滤液中一定含有NaOH.
(3)为最终确定该滤液的组成,还需补充的实验是:另取少量滤液于试管中,滴加BaCl2溶液,观察到白色沉淀.
【实验结论】该无色滤液的组成为NaCl、NaOH、Na2SO4.
 某班化学实验课进行酸碱盐的性质实验.
某班化学实验课进行酸碱盐的性质实验.【实验一】自制酸碱指示剂
(1)取少量紫包菜和白菜叶剪碎后分别在研钵中捣烂,加入酒精溶液浸泡;用纱布将浸泡出的汁液滤出,观察到紫包菜汁液为紫色,白菜汁液为无色.分别装好待用.
(2)取四支试管分别用NaOH溶液和稀盐酸进行实验,观察到现象如图.
记录如下:
| NaOH溶液 | 稀盐酸 | |
| 紫包菜汁液 | ①绿色 | ②红色 |
| 白菜汁液 | ③无色 | ④淡黄色 |
【实验二】探究碱和盐的性质
第一组学生进行CuSO4、NaOH溶液的反应,观察到的现象是有蓝色絮状沉淀生成,溶液颜色变浅;该反应的化学方程式为CuSO4+2NaOH=Na2SO4+Cu(OH)2↓.
第二组学生进行BaCl2、Na2CO3溶液的反应,反应的化学方程式为BaCl2+Na2CO3=BaCO3↓+2NaCl.
【实验三】废液再探究
结束后,两组同学将全部的废液集中倒进一个废液缸中.兴趣小组同学对废液进行过滤,得到无色滤液.
【提出问题】滤液中含有什么溶质?
【做出猜想】滤液中一定含有NaCl,还可能含有BaCl2、NaOH、Na2CO3、Na2SO4中的一种或几种.
【实验探究】
(1)取少量滤液加入试管中,滴加紫包菜汁液,溶液显绿色.
(2)继续加入足量的稀硫酸,溶液变成红色,无气泡和沉淀产生,则滤液中一定没有Na2CO3、BaCl2.
根据(1)(2)判断滤液中一定含有NaOH.
(3)为最终确定该滤液的组成,还需补充的实验是:另取少量滤液于试管中,滴加BaCl2溶液,观察到白色沉淀.
【实验结论】该无色滤液的组成为NaCl、NaOH、Na2SO4.
16.下列有关“化学与生活”的说法中,正确的是( )
| A. | 二氧化硫等气体是造成酸雨的主要因素 | |
| B. | 用焚烧的方法处理废弃的塑料制品会造成“白色污染” | |
| C. | 用汽油洗涤衣服上的油渍是利用汽油的乳化功能 | |
| D. | 铝合金比铁制品耐腐蚀是因为铝的化学性质不如铁活泼 |
13.某阳离子Mn+的核外电子共有x个电子,核内有y个中子,则M的相对原子质量约为( )
| A. | x+y | B. | x+y+n | C. | x-n+y | D. | x+n-y |
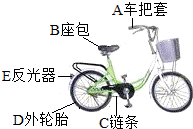 如图是同学们经常使用交通工具--自行车,请完成下列各题:
如图是同学们经常使用交通工具--自行车,请完成下列各题: