题目内容
14. 在一次用餐中,同学们对燃料“固体酒精”产生了好奇,于是对其成分进行研究.
在一次用餐中,同学们对燃料“固体酒精”产生了好奇,于是对其成分进行研究.【查阅资料】
(1)该固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成.
(2)氯化钙、氯化钡溶液均呈中性.
【提出问题】
(1)酒精中是否含有碳元素?
(2)固体酒精中的氢氧化钠是否变质?
【实验探究】
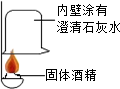
(1)按图实验,发现澄清石灰水变浑浊,可得出酒精中含有碳元素的结论.此结论合理(选填“合理”或“不合理”).
(2)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀.取沉淀与试管中加稀盐酸,有气泡产生.写出产生气体的化学方程式2NaOH+CO2═Na2CO3+H2O或CaCO3+2HCl=CaCl2+CO2↑+H2O
分析实验并结合资料得出氢氧化钠已变质.
(3)为进一步确定氢氧化钠的变质程度,分组探究.
①甲组取烧杯上层清夜于两支试管中,按如图探究.
| 方案 | 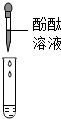 |  |
| 现象 | 溶液变红 | 产生白色沉淀 |
| 结论 | 清液有氢氧化钠 | 清液有碳酸钠 |
【实验结论】经讨论一致认为固体酒精中的氢氧化钠部分变质.
【反思交流】乙组实验中加足量氯化钡溶液的目的是除去碳酸钠,防止影响对NaOH的检验.
【拓展应用】要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的AC.
A.Ba(OH)2溶液 B.CaCl2溶液 C.Ca(OH)2溶液.
分析 【实验探究】
(1)酒精燃烧生成水和二氧化碳,二氧化碳能使澄清石灰水变浑浊;
(2)氢氧化钠能和空气中的二氧化碳反应生成碳酸钠和水,碳酸钠能和氯化钙反应生成碳酸钙沉淀和氯化钠,碳酸钙能和稀盐酸反应生成氯化钙、水和二氧化碳;
(3)氢氧化钠溶液和碳酸钠溶液都显碱性,都能够使酚酞试液变红色;
【实验结论】由实验现象分析;
【反思交流】为了使碳酸钠完全反应,应该加入过量的氯化钡溶液.
【拓展应用】根据碳酸钠能和氢氧化钡反应生成碳酸钡沉淀和氢氧化钠,碳酸钠能和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠进行分析.
解答 解:【实验探究】
(1)由质量守恒定律,发现澄清石灰水变浑浊,说明反应生成了二氧化碳,因为酒精燃烧时只有氧气参加,因此可得出酒精中含有碳元素的结论,此结论合理.
故填:合理.
(2)氢氧化钠易吸收空气中的水而潮解,吸收空气中的二氧化碳生成碳酸钠而变质,氢氧化钠变质的化学方程式:2NaOH+CO2═Na2CO3+H2O;
白色沉淀是碳酸钠和氯化钙反应生成的碳酸钙,碳酸钙和稀盐酸反应的化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O.
故填:2NaOH+CO2═Na2CO3+H2O或CaCO3+2HCl=CaCl2+CO2↑+H2O.
(3)①取烧杯上层清夜于两支试管中,其中一只试管中产生白色沉淀,说明清液中有碳酸钠.
故填:白色沉淀.
②乙组认为甲组实验不能证明清夜中一定有氢氧化钠,理由是:碳酸钠溶液显碱性,也能使酚酞试液变红色.
故填:碳酸钠溶液呈碱性;也能使酚酞溶液变红.
【实验结论】由实验现象可知滤液中含有氢氧化钠和碳酸钠,氢氧化钠部分变质
【反思交流】
乙组实验中加足量氯化钡溶液的目的是除去碳酸钠,防止影响对NaOH的检验.
故填:除去碳酸钠,防止影响对NaOH的检验.
【拓展应用】要除去部分变质的氢氧化钠溶液中的杂质,可选择适量的氢氧化钡溶液、氢氧化钙溶液,不能选择氯化钙溶液,因为碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,因此使用氯化钙时能够带入新杂质--氯化钠,故选:AC.
故答案为:AC.
点评 实验是化学的重要组成部分,正确的实验操作是得出科学结论的前提条件之一,因此要学会设计实验、进行实验、分析实验,为得出正确的结论奠定基础.

| A. | “湖面波光粼粼”是光的折射 | |
| B. | “花香随风飘散”是分子不停地做无规则运动的结果 | |
| C. | 露是水蒸气汽化而成的 | |
| D. | 湖面上的青山的倒影给九龙湖增加了更大的神韵,青山的倒影是光的反射 |
| A. | H2、O2 | B. | Mg(OH)2、Na2SO4 | C. | NaOH、FeCl3 | D. | BaSO4、Cu(NO3)2 |
| A. |  过滤 | B. |  点燃酒精灯 | C. |  收集CO2并验满 | D. |  取用液体 |
| A. | 该“塑化剂”中碳、氢、氧元素的个数比为12:19:2 | |
| B. | 该“塑化剂”中碳的质量分数为73.8% | |
| C. | 该“塑化剂”属有机物 | |
| D. | 食品添加剂要严格按照国家规定标准进行使用 |
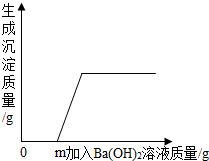 某溶液由氯化钾溶液、稀硝酸、稀硫酸和硝酸铜溶液中的一种或几种混合而成.取一定量该溶液,向其中滴加Ba(OH)2溶液,生成沉淀的质量与加入Ba(OH)2溶液质量的关系如图所示.
某溶液由氯化钾溶液、稀硝酸、稀硫酸和硝酸铜溶液中的一种或几种混合而成.取一定量该溶液,向其中滴加Ba(OH)2溶液,生成沉淀的质量与加入Ba(OH)2溶液质量的关系如图所示.