题目内容
11.在X2+2XY2=4XY中,1克X2与一定量的XY2反应能生成5克XY,则X2与XY的相对分子质量之比是4:5.分析 首先利用质量守恒定律,确定反应中化合物XY的质量,然后根据反应中三种物质的质量关系,判断物质X2与XY的相对分子质量之比.
解答 解:根据质量守恒定律,则
X2 +2XY2═4XY
Mr(X2) Mr(XY)×4
1g 5g
则X2与XY的相对分子质量之比=4:5;
故填:4:5.
点评 化学方程式中各物质的质量比等于反应中各物质的相对分子质量与参加反应的分子个数(化学计量数)乘积的比.

练习册系列答案
相关题目
1.水是生命之源,我们应该了解水、爱护水资源.下列说法错误的是( )
| A. | 为使水中的悬浮杂质沉降,可在水中加入适量的明矾 | |
| B. | 自来水厂常用ClO2消毒,ClO2中氯元素的化合价为+4 | |
| C. | 经过滤得到的水一定是纯水 | |
| D. | 5mL水和5mL酒精混合,溶液体积小于10mL,说明分子间有空隙 |
19.三毛同学在过生日时,发现妈妈在煮虾时,青色的生虾煮熟后颜色变成红色.他认为这种红色物质可能就像酸碱指示剂一样,遇到酸或碱颜色会发生改变.就三毛同学的看法而言应属于科学探究的( )
| A. | 实验 | B. | 假设 | C. | 观察 | D. | 做结论 |
2.用数轴表示某些化学知识直观、简明、易记.下列表示不正确的是( )
| A. | $→_{地壳中部分元素的含量}^{氧硅铝(小)}$ | |
| B. | $→_{硫元素的化合价}^{H_{2}S、S、SO_{2}、H_{2}SO_{4}(高)}$ | |
| C. | $→_{部分元素原子序数的关系}^{H、C、Na、Mg(大)}$ | |
| D. | $→_{粒子的体积关系}^{离子、原子、分子(大)}$ |

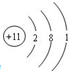 ,所以金属钠的化学性质很活泼,在空气中极易被氧化成氧化钠,用小刀一切,就露出它本来面目,银白色有金属光泽.钠还能与水反应,生成氢氧化钠(NaOH)和氢气.实验室中的金属钠通常保存在煤油中.
,所以金属钠的化学性质很活泼,在空气中极易被氧化成氧化钠,用小刀一切,就露出它本来面目,银白色有金属光泽.钠还能与水反应,生成氢氧化钠(NaOH)和氢气.实验室中的金属钠通常保存在煤油中.
