题目内容
4.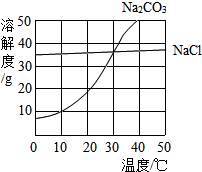 如图为氯化钠、碳酸钠在水中的溶解度曲线,请回答下列问题:
如图为氯化钠、碳酸钠在水中的溶解度曲线,请回答下列问题:(1)碳酸钠和氯化钠混合溶液的pH>7(填“<”或“>”或“=”);
(2)40℃时,碳酸钠的溶解度为50g.大于30℃时,碳酸钠的溶解度>氯化钠的溶解度(填“<”或“>”或“=”);
(3)40℃时,碳酸钠和氯化钠均饱和溶液,当温度降低到20℃时,析出的主要物质是Na2CO3(填化学式);
(4)为检验(3)中析出的物质,取少量样品于试管中加入足量的稀硝酸,完全溶解,并有气体产生,再加入几滴稀AgNO3(填化学式)溶液,有白色沉淀产生.
分析 根据题目信息和溶解度曲线可知:碳酸钠、氯化钠两种固体物质的溶解度,都是随温度升高而增大,而碳酸钠的溶解度随温度的升高变化比氯化钠大;碳酸钠和氯化钠混合溶液的pH大于7,因为碳酸钠溶液显碱性;40℃时,碳酸钠的溶解度为50g,大于30℃时,碳酸钠的溶解度大于氯化钠的溶解度;40℃时,碳酸钠和氯化钠均饱和溶液,当温度降低到20℃时,析出的主要物质是碳酸钠,因为碳酸钠的溶解度随温度的升高变化比氯化钠大;为检验(3)中析出的物质,取少量样品于试管中加入足量的稀硝酸,完全溶解,并有气体产生,再加入几滴稀AgNO3溶液,有白色沉淀产生,就证明还有氯化钠.
解答 解:(1)碳酸钠和氯化钠混合溶液的pH大于7,因为碳酸钠溶液显碱性;故答案为:>;
(2)由溶解度曲线可知:40℃时,碳酸钠的溶解度为50g,大于30℃时,碳酸钠的溶解度大于氯化钠的溶解度;故答案为:50;>;
(3)40℃时,碳酸钠和氯化钠均饱和溶液,当温度降低到20℃时,析出的主要物质是碳酸钠,因为碳酸钠的溶解度随温度的升高变化比氯化钠大;故答案为:Na2CO3;
(4)为检验(3)中析出的物质,取少量样品于试管中加入足量的稀硝酸,完全溶解,并有气体产生,再加入几滴稀AgNO3溶液,有白色沉淀产生,就证明还有氯化钠;故答案为:AgNO3;
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了碳酸钠的性质和氯离子的检验等,本考点主要出现在选择题和填空题中.

练习册系列答案
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案
相关题目
4.水是生命的源泉,关于水的说法不正确的是( )
| A. | 水的天然循环是通过水的三态变化实现的,是水分子运动的结果 | |
| B. | 电解水时生成氢气与氧气的质量比为2:1 | |
| C. | 生活中常用加热煮沸的方法将硬水转化为软水 | |
| D. | 过滤能除掉水中不溶性泥沙,是利用了水分子比泥沙颗粒小的原理 |
12.下列化学史的有关叙述中,不正确的是( )
| A. | 道尔顿和阿伏伽德罗等科学家的研究得到了重要的结论:物质是由原子或分子构成的 | |
| B. | 门捷列夫发现了元素周期律并编制出元素周期表 | |
| C. | 原子论和分子学说的创立,奠定了近代化学的基础 | |
| D. | 拉瓦锡用红磷燃烧实验测得空气由氮气和氧气组成 |
19.每年中招体育加试期间同学爱喝含有牛磺酸(C2H7NO3S)饮料以缓解肌肉和神经疲劳,下列关于牛磺酸的说法正确的( )
| A. | 牛磺酸中共有5种元素 | B. | 化合物中O、S元素的质量比为3:1 | ||
| C. | 牛磺酸分子中含有7个氢原子 | D. | 牛磺酸中含有臭氧(O3)分子 |
9.下列物质的化学式书写正确的是( )
| A. | 碳酸钠NaCO3 | B. | 氢氧化钠Na(OH)2 | C. | 氧化铁O3Fe2 | D. | 硫酸钾K2SO4 |
16.下列化学方程式正确的是( )
| A. | 4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | B. | 2Fe+6HCI═2FeCI3+3H2↑ | ||
| C. | KCIO3$\frac{\underline{\;\;△\;\;}}{\;}$KCI+O2↑ | D. | 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ |
14.《物质构成的奥秘》告诉我们:元素的种类、化学性质分别与下列粒子数密切相关.它们分别是( )
| A. | 质子数、中子数 | B. | 最外层电子数、质子数 | ||
| C. | 中子数、最外层电子数 | D. | 质子数、最外层电子数 |