题目内容
19.每年中招体育加试期间同学爱喝含有牛磺酸(C2H7NO3S)饮料以缓解肌肉和神经疲劳,下列关于牛磺酸的说法正确的( )| A. | 牛磺酸中共有5种元素 | B. | 化合物中O、S元素的质量比为3:1 | ||
| C. | 牛磺酸分子中含有7个氢原子 | D. | 牛磺酸中含有臭氧(O3)分子 |
分析 A、根据牛磺酸化学式的含义进行分析判断.
B、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
C、根据牛磺酸的微观构成进行分析判断.
D、根据牛磺酸的微观构成进行分析判断.
解答 解:A、牛磺酸是由碳元素、氢元素、氮元素、氧元素、硫元素五种元素组成的,故选项说法正确.
B、化合物中O、S元素的质量比为(16×3):32=3:2,故选项说法错误.
C、1个牛磺酸分子中含有7个氢原子,故选项说法错误.
D、牛磺酸是由牛磺酸分子构成的,不含臭氧(O3)分子,故选项说法错误.
故选:A.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.市场上有售“高钙牛奶”,这里的“钙”是指( )
| A. | 钙原子 | B. | 钙元素 | C. | 钙分子 | D. | 钙单质 |
20.在AgNO3和Cu(NO3)2的混合溶液中加入一定量的铁粉,充分反应后,过滤,下列情况不可能成立的是( )
| A. | 滤液成分为Fe2+,Ag+和Cu2+,滤渣成分为Ag | |
| B. | 滤液成分为Fe2+和Cu2+,滤渣成分为Ag和Cu | |
| C. | 滤液成分为Fe2+和Cu2+,滤渣成分为Ag,Cu和Fe | |
| D. | 滤液成分为Fe2+和cu2+,滤渣成分为Ag |
14.推理是化学学习中常用的思维方法.下列推理正确的是( )
| A. | 碱性溶液能使无色酚酞试液变红,而Na2CO3溶液也能使无色酚酞试液变红,故Na2CO3溶液是 碱性溶液 | |
| B. | CO2、SO2等非金属氧化物能与NaOH溶液反应,则非金属氧化物都能与NaOH溶液反应 | |
| C. | 一定温度下KNO3饱和溶液降低温度会析出晶体,则一定温度下物质的饱和溶液降温都会析出晶体 | |
| D. | 盐是由金属离子和酸根离子构成的,NH4NO3中没有金属离子,不属于盐 |
8.常温下,铜与稀硫酸几乎不反应,但在一定温度下,铜与浓硫酸反应生成硫酸铜、水和一种气体.小明很好奇,设计如下实验探究铜丝与浓硫酸反应后的产物.
【提出问题】生成的气体是什么?
【查阅资料】SO2能使品红溶液褪色;硫酸铜固体为白色,硫酸铜溶液为蓝色.
【猜想与假设】猜想一:氢气;猜想二:二氧化硫.
【设计实验】如图所示
【实验结论】该反应的化学方程式为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+2H2O+SO2↑,该气体可以用氢氧化钠溶液来吸收以防止大气污染.
【反思与评价】
(1)铜丝可以上下抽动的作用是便于控制反应的发生和停止.
(2)试管中出现白色固体的原因是有无水硫酸铜固体析出.
某研究小组利用如图装置探究铜与浓硫酸反应的产物.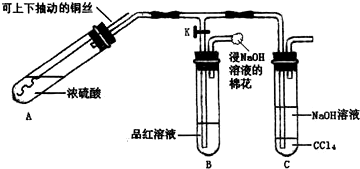
实验步骤与现象如下:
①检查装置气密性,向A中加入5mL浓硫酸,打开K,将铜丝伸入浓硫酸中,给A处加热,观察到B中品红溶液褪色,再关闭K.
②实验观察到A中液面下铜丝变黑,产生气泡,液面上方产生大量白雾,一段时间后溶液中有白色固体出现,拉出铜丝,停止加热.回答下列问题:
(1)溶液中白色固体是无水CuSO4 (填化学式),C中CCl4的作用是防止倒吸.
(2)取出铜丝,用蒸馏水洗净后伸入到稀硫酸中,铜丝变亮、溶液变蓝.写出A中可能发生反应的化学方程式:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+2H2O+SO2↑、Cu+H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O+SO2↑.
(3)分离出C中的上层液体,滴加过量稀盐酸和BaCl2溶液,有白色沉淀产生.
①分离的操作名称为:分液:
②白色沉淀为:硫酸钡;
③产生白色沉淀的原因可能是装置中的氧气参加了反应.
【提出问题】生成的气体是什么?
【查阅资料】SO2能使品红溶液褪色;硫酸铜固体为白色,硫酸铜溶液为蓝色.
【猜想与假设】猜想一:氢气;猜想二:二氧化硫.
【设计实验】如图所示
| 步骤 | 实验操作 | 实验现象 | 实验结论 |
| 1 | 向试管中加入5mL浓硫酸,将铜丝伸入浓硫酸中,给试管加热. | 有白色固体出现,产生气泡 | |
| 2 | 用燃着的木条引燃产生的气体 | 未听见爆鸣声 | 猜想一不成立. (填“成立”或“不成立”) |
| 3 | 猜想二成立 |
【反思与评价】
(1)铜丝可以上下抽动的作用是便于控制反应的发生和停止.
(2)试管中出现白色固体的原因是有无水硫酸铜固体析出.
某研究小组利用如图装置探究铜与浓硫酸反应的产物.

实验步骤与现象如下:
①检查装置气密性,向A中加入5mL浓硫酸,打开K,将铜丝伸入浓硫酸中,给A处加热,观察到B中品红溶液褪色,再关闭K.
②实验观察到A中液面下铜丝变黑,产生气泡,液面上方产生大量白雾,一段时间后溶液中有白色固体出现,拉出铜丝,停止加热.回答下列问题:
(1)溶液中白色固体是无水CuSO4 (填化学式),C中CCl4的作用是防止倒吸.
(2)取出铜丝,用蒸馏水洗净后伸入到稀硫酸中,铜丝变亮、溶液变蓝.写出A中可能发生反应的化学方程式:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+2H2O+SO2↑、Cu+H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O+SO2↑.
(3)分离出C中的上层液体,滴加过量稀盐酸和BaCl2溶液,有白色沉淀产生.
①分离的操作名称为:分液:
②白色沉淀为:硫酸钡;
③产生白色沉淀的原因可能是装置中的氧气参加了反应.
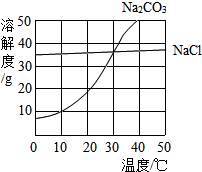 如图为氯化钠、碳酸钠在水中的溶解度曲线,请回答下列问题:
如图为氯化钠、碳酸钠在水中的溶解度曲线,请回答下列问题: