题目内容
16. 某化学课堂围绕“酸和碱的中和反应”,将学生分成若干小组开展探究活动.请你参与学习并填写空格.
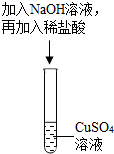
某化学课堂围绕“酸和碱的中和反应”,将学生分成若干小组开展探究活动.请你参与学习并填写空格.探究一:甲组同学设计了如图所示的实验,根据图示回答:
(1)在试管中加入约2mL硫酸铜溶液,然后滴入几滴氢氧化钠溶液,观察到的实验现象是产生蓝色沉淀.
(2)然后再向试管中加入稀盐酸,该实验通过稀盐酸与氢氧化铜(填物质名称)反应,观察到明显现象,验证了酸与碱能发生中和反应.
探究二:乙组同学将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中,一会儿后,发现忘记了滴加指示剂.于是他们从烧杯中取出少量反应后的溶液于试管中,滴入几滴酚酞溶液,振荡,观察到无明显现象.中和反应的化学方程式为H2SO4+2NaOH═Na2SO4+2H2O.
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质组成是什么?
【假设猜想】针对疑问,大家纷纷提出猜想
猜想一:只有Na2SO4
猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH
同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的是猜想三.
【实验探究】为了验证其余猜想,同学们利用烧杯中的溶液,进行如下方案的探究.
| 实验方案 | 实验现象 | 结论与解释 |
方案一:滴加Na2CO3溶液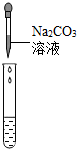 | 产生大量气泡 | 溶液中有H2SO4 |
方案二:滴加BaCl2溶液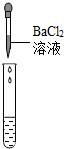 | 产生白色沉淀 | 溶液中有H2SO4 |
【评价反思】老师对同学们能用多种方法进行探究给予了肯定,同时指出实验方案中有一个是错误的,错误的原因是方案二只能证明溶液中含有SO42-,不能证明含有H2SO4.
分析 探究一(1)根据氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠进行分析;
(2)根据盐酸和氢氧化铜反应生成氯化铜和水进行分析;
探究二根据氢氧化钠和硫酸反应生成硫酸钠和水进行分析;
【假设猜想】根据氢氧化钠和稀硫酸反应生成硫酸钠和水,稀硫酸和氢氧化钠不能共存进行分析;
【实验探究】根据碳酸钠和硫酸反应生成硫酸钠和水进行分析;
【评价反思】根据稀硫酸、硫酸钠都能够和BaCl2溶液反应生成硫酸钡沉淀进行分析.
解答 解:探究一(1)氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,所以观察到的实验现象是:产生蓝色沉淀;
(2)盐酸和氢氧化铜反应生成氯化铜和水,所以该实验通过稀盐酸与氢氧化铜反应,观察到明显现象,验证了酸与碱能发生中和反应;
探究二 氢氧化钠和硫酸反应生成硫酸钠和水,化学方程式为:H2SO4+2NaOH═Na2SO4+2H2O;
【假设猜想】氢氧化钠和稀硫酸反应生成硫酸钠和水,稀硫酸和氢氧化钠不能共存,所以猜想三不成立;
【实验探究】碳酸钠和硫酸反应生成硫酸钠和水,所以实验现象是:产生大量气泡;
【评价反思】稀硫酸、硫酸钠都能够和BaCl2溶液反应生成硫酸钡沉淀,所以错误的原因是:方案二只能证明溶液中含有SO42-,不能证明含有H2SO4.
探究一(1)产生蓝色沉淀;
(2)氢氧化铜;
探究二 H2SO4+2NaOH═Na2SO4+2H2O;
【假设猜想】猜想三;
【实验探究】产生大量气泡;
【评价反思】方案二只能证明溶液中含有SO42-,不能证明含有H2SO4.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
1.张亭栋教授因发现砒霜(主要成分为三氧化二砷,分子式为As2O3)在治疗白血病方面的重要作用而荣获2015年度“求是杰出科学家奖”.下列有关As2O3的说法正确的是( )
| A. | As203中砷元素的化合价为+3 | |
| B. | As203为金属氧化物 | |
| C. | 一个As203分子中含有一个臭氧分子 | |
| D. | As203分子中砷与氧元素的质量比为2:3 |
8.乐乐想在妈妈生日那天为妈妈做一顿午餐,食谱为:米饭、鸡肉、蛋汤、大虾、鱼.为使营养均衡,你觉得最好还要补充( )
| A. | 青菜 | B. | 豆浆 | C. | 牛奶 | D. | 鸭肉 |
5.以下实验现象描述错误的是( )
| A. | 木炭在氧气中燃烧,发出白光,生成无色气体 | |
| B. | 向Na2CO3溶液中滴加澄清的石灰水,有白色沉淀产生 | |
| C. | CO还原Fe2O3的实验后,玻璃管中的粉末由红棕色变成黑色 | |
| D. | 用石蕊溶液染成的干燥的纸花放入CO2集气瓶中,纸花变红色 |
6. 小民同学在练习“金属的化学性质”实验操作时,发现几支试管中气泡有快有慢,于是他与小芳同学一起合作进行如下探究.
小民同学在练习“金属的化学性质”实验操作时,发现几支试管中气泡有快有慢,于是他与小芳同学一起合作进行如下探究.
【提出问题】金属与酸反应的快慢受哪些因素影响呢?
【猜想与假设】
A.可能与酸的浓度有关;
B.可能与金属的种类有关;
C.可能与金属的形状有关.
【设计并实验】小明和小芳进行如下实验.
(1)实验时需将镁片和铁片进行打磨,其目的是除去金属表面的氧化物.
(2)写出铁与稀盐酸反应的化学方程式:Fe+2HCl=FeCl2+H2↑.
【收集证据】
(3)要比较不同金属的种类对反应快慢的影响,应选择的实验编号是②③.
【得出结论】
(4)实验①中试管外壁发烫,说明镁与稀盐酸反应是放热反应.实验测得该反应中产生气体的速率(V)与时间(t)的关系如图所示,你认为在t2~t3时间段内反应速率逐渐减慢的主要原因由于镁与盐酸反应消耗了盐酸,盐酸的浓度变小,因此反应速率逐渐减慢.
【实验反思】本实验采用的定量比较气体产生速率的方法是收集相同体积的气体需要的时间.
 小民同学在练习“金属的化学性质”实验操作时,发现几支试管中气泡有快有慢,于是他与小芳同学一起合作进行如下探究.
小民同学在练习“金属的化学性质”实验操作时,发现几支试管中气泡有快有慢,于是他与小芳同学一起合作进行如下探究.【提出问题】金属与酸反应的快慢受哪些因素影响呢?
【猜想与假设】
A.可能与酸的浓度有关;
B.可能与金属的种类有关;
C.可能与金属的形状有关.
【设计并实验】小明和小芳进行如下实验.
| 实验编号 | 盐酸的浓度 (均取20mL) | 金属 (均取2g) | 金属的形状 | 收集50mL氢气所需要时间/s |
| ① | 10% | 镁 | 粉状 | 60 |
| ② | 10% | 铁 | 片状 | 120 |
| ③ | 10% | 镁 | 片状 | 102 |
| ④ | 20% | 铁 | 片状 | 110 |
(2)写出铁与稀盐酸反应的化学方程式:Fe+2HCl=FeCl2+H2↑.
【收集证据】
(3)要比较不同金属的种类对反应快慢的影响,应选择的实验编号是②③.
【得出结论】
(4)实验①中试管外壁发烫,说明镁与稀盐酸反应是放热反应.实验测得该反应中产生气体的速率(V)与时间(t)的关系如图所示,你认为在t2~t3时间段内反应速率逐渐减慢的主要原因由于镁与盐酸反应消耗了盐酸,盐酸的浓度变小,因此反应速率逐渐减慢.
【实验反思】本实验采用的定量比较气体产生速率的方法是收集相同体积的气体需要的时间.
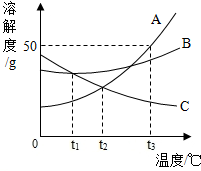 如图是物质A、B、C的溶解度曲线.试根据图象回答:
如图是物质A、B、C的溶解度曲线.试根据图象回答: