题目内容
5.以下实验现象描述错误的是( )| A. | 木炭在氧气中燃烧,发出白光,生成无色气体 | |
| B. | 向Na2CO3溶液中滴加澄清的石灰水,有白色沉淀产生 | |
| C. | CO还原Fe2O3的实验后,玻璃管中的粉末由红棕色变成黑色 | |
| D. | 用石蕊溶液染成的干燥的纸花放入CO2集气瓶中,纸花变红色 |
分析 A、根据碳和氧气在点燃的条件下生成二氧化碳,发出白光进行分析;
B、根据碳酸钠和氢氧化钙反应会生成白色的碳酸钙沉淀进行分析;
C、根据一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳进行分析;
D、根据石蕊遇酸变红色,二氧化碳是酸性氧化物,但不是酸,不显酸性,不能使紫色石蕊变色进行分析.
解答 解:A、碳和氧气在点燃的条件下生成二氧化碳,发出白光,故A正确;
B、碳酸钠和氢氧化钙反应会生成白色的碳酸钙沉淀,故B正确;
C、一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,所以玻璃管中的粉末由红棕色变成黑色,故C正确;
D、石蕊遇酸变红色,二氧化碳是酸性氧化物,但不是酸,不显酸性,不能使紫色石蕊变色,故D错误.
故选:D.
点评 实验现象的描述是化学实验考查的重点和热点,要注意反应条件,要能区分叙述产物与描述现象的不同.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
16. 某化学课堂围绕“酸和碱的中和反应”,将学生分成若干小组开展探究活动.请你参与学习并填写空格.
某化学课堂围绕“酸和碱的中和反应”,将学生分成若干小组开展探究活动.请你参与学习并填写空格.
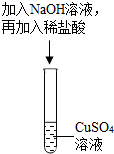
探究一:甲组同学设计了如图所示的实验,根据图示回答:
(1)在试管中加入约2mL硫酸铜溶液,然后滴入几滴氢氧化钠溶液,观察到的实验现象是产生蓝色沉淀.
(2)然后再向试管中加入稀盐酸,该实验通过稀盐酸与氢氧化铜(填物质名称)反应,观察到明显现象,验证了酸与碱能发生中和反应.
探究二:乙组同学将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中,一会儿后,发现忘记了滴加指示剂.于是他们从烧杯中取出少量反应后的溶液于试管中,滴入几滴酚酞溶液,振荡,观察到无明显现象.中和反应的化学方程式为H2SO4+2NaOH═Na2SO4+2H2O.
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质组成是什么?
【假设猜想】针对疑问,大家纷纷提出猜想
猜想一:只有Na2SO4
猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH
同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的是猜想三.
【实验探究】为了验证其余猜想,同学们利用烧杯中的溶液,进行如下方案的探究.
【得出结论】通过探究,同学们一致确定猜想二是正确的.
【评价反思】老师对同学们能用多种方法进行探究给予了肯定,同时指出实验方案中有一个是错误的,错误的原因是方案二只能证明溶液中含有SO42-,不能证明含有H2SO4.
 某化学课堂围绕“酸和碱的中和反应”,将学生分成若干小组开展探究活动.请你参与学习并填写空格.
某化学课堂围绕“酸和碱的中和反应”,将学生分成若干小组开展探究活动.请你参与学习并填写空格.探究一:甲组同学设计了如图所示的实验,根据图示回答:
(1)在试管中加入约2mL硫酸铜溶液,然后滴入几滴氢氧化钠溶液,观察到的实验现象是产生蓝色沉淀.
(2)然后再向试管中加入稀盐酸,该实验通过稀盐酸与氢氧化铜(填物质名称)反应,观察到明显现象,验证了酸与碱能发生中和反应.
探究二:乙组同学将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中,一会儿后,发现忘记了滴加指示剂.于是他们从烧杯中取出少量反应后的溶液于试管中,滴入几滴酚酞溶液,振荡,观察到无明显现象.中和反应的化学方程式为H2SO4+2NaOH═Na2SO4+2H2O.
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质组成是什么?
【假设猜想】针对疑问,大家纷纷提出猜想
猜想一:只有Na2SO4
猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH
同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的是猜想三.
【实验探究】为了验证其余猜想,同学们利用烧杯中的溶液,进行如下方案的探究.
| 实验方案 | 实验现象 | 结论与解释 |
方案一:滴加Na2CO3溶液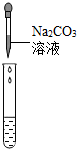 | 产生大量气泡 | 溶液中有H2SO4 |
方案二:滴加BaCl2溶液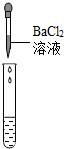 | 产生白色沉淀 | 溶液中有H2SO4 |
【评价反思】老师对同学们能用多种方法进行探究给予了肯定,同时指出实验方案中有一个是错误的,错误的原因是方案二只能证明溶液中含有SO42-,不能证明含有H2SO4.
20.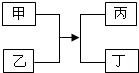 甲乙丙丁四种物质的转化关系如图所示.下列说法正确的是( )
甲乙丙丁四种物质的转化关系如图所示.下列说法正确的是( )
 甲乙丙丁四种物质的转化关系如图所示.下列说法正确的是( )
甲乙丙丁四种物质的转化关系如图所示.下列说法正确的是( )| A. | 若丙为沉淀,则甲、乙中一定有一种物质是碱 | |
| B. | 若甲、丁为单质,则该反应一定是置换反应 | |
| C. | 若丁为水,则该反应一定是复分解反应 | |
| D. | 若丙为气体,则甲、乙中一定有单质 |
14. 如图所示实验中,①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球.下列能说明密度大于空气且能与水反应的现象是( )
如图所示实验中,①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球.下列能说明密度大于空气且能与水反应的现象是( )
 如图所示实验中,①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球.下列能说明密度大于空气且能与水反应的现象是( )
如图所示实验中,①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球.下列能说明密度大于空气且能与水反应的现象是( )| A. | ①变红,③不变红 | B. | ④变红,③不变红 | ||
| C. | ①、④变红,②、③不变红 | D. | ④比①先变红,②、③不变红 |