题目内容
17.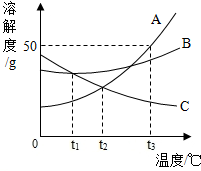 如图是物质A、B、C的溶解度曲线.试根据图象回答:
如图是物质A、B、C的溶解度曲线.试根据图象回答:(1)温度为t1℃时,三种物质的溶解度大小关系B=C>A;
(2)t2℃时,将30克A物质放入50克水中,其溶液的质量分数为33.3%.
分析 根据题目信息和溶解度曲线可知:a、b两种固体物质的溶解度,都是随温度升高而增大,而c的溶解度随温度的升高而减少;温度为t1℃时,三种物质的溶解度大小关系B=C>A;t2℃时,a的溶解度是50g,将30克A物质放入50克水中,其溶液的质量分数=$\frac{25g}{75g}×100%≈33.3%$.
解答 解:(1)由溶解度曲线可知:温度为t1℃时,三种物质的溶解度大小关系B=C>A,故答案为:B=C>A;
(2)t2℃时,a的溶解度是50g,将30克A物质放入50克水中,其溶液的质量分数=$\frac{25g}{75g}×100%≈33.3%$,故答案为:33.3%;
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液和溶质质量分数的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.某学习小组探究氢氧化钙溶液的化学性质,并作了延伸探究.
探究一:甲同学设计了如下实验方案,请你帮助完成实验报告.
【提出问题】实验方案(3)褪色后溶液中的溶质是什么?
【查阅资料】氯化钙溶液呈中性.
【作出猜想】乙同学从反应情况分析,溶液中除含少量酚酞外,溶质可能有以下三种情况:
①氯化钙②氯化钙和氯化氢③氯化钙和氢氧化钙
【分析讨论】丙同学从实验现象分析得出:猜想③肯定不合理,其理由稀盐酸加入滴有酚酞的石灰水中,红色褪为无色,说明溶液为中性或酸性,不可能有氢氧化钙.
探究二:丁同学为进一步验证乙同学的猜想,设计实验如下:将实验方案(3)褪色后溶液倒入烧杯中,向其中逐滴滴加稀碳酸钠溶液至过量,边滴加边振荡.实验后得出产生沉淀质量与碳酸钠溶液体积之间的关系,如图所示.写出实验过程中的现象滴加碳酸钠溶液,开始先产生气泡,随后才产生沉淀,溶液最终变红色.
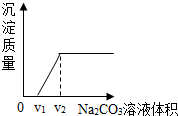
【得出结论】乙同学的猜想中,②(填序号)合理.
【反思讨论】学习小组结合图象,分析了丁同学实验过程中烧杯内溶液的变化.下列说法正确的是AB(填序号)
A.溶液质量逐渐增大 B.氯化钠质量逐渐增大,V2后不变
C.氯化钙的质量先增大后减小 D.溶液的pH一直增大.
探究一:甲同学设计了如下实验方案,请你帮助完成实验报告.
| 方案 | (1) | (2) | (3) |
| 实验操作 | 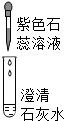 | 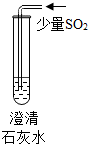 |  |
| 现象 | 溶液变为蓝色 | 澄清石灰水变浑浊 | 红色褪为无色 |
| 结论或解释 | 氢氧化钙溶液能使石蕊等酸碱指示剂变色 | 氢氧化钙溶液能与某些非金属氧化物反应生成盐和水.二氧化硫与澄清石灰水反应的化学方程式是SO2+Ca(OH)2═CaSO3↓+H2O. | 氢氧化钙溶液能与酸发生中和反应 |
【查阅资料】氯化钙溶液呈中性.
【作出猜想】乙同学从反应情况分析,溶液中除含少量酚酞外,溶质可能有以下三种情况:
①氯化钙②氯化钙和氯化氢③氯化钙和氢氧化钙
【分析讨论】丙同学从实验现象分析得出:猜想③肯定不合理,其理由稀盐酸加入滴有酚酞的石灰水中,红色褪为无色,说明溶液为中性或酸性,不可能有氢氧化钙.
探究二:丁同学为进一步验证乙同学的猜想,设计实验如下:将实验方案(3)褪色后溶液倒入烧杯中,向其中逐滴滴加稀碳酸钠溶液至过量,边滴加边振荡.实验后得出产生沉淀质量与碳酸钠溶液体积之间的关系,如图所示.写出实验过程中的现象滴加碳酸钠溶液,开始先产生气泡,随后才产生沉淀,溶液最终变红色.

【得出结论】乙同学的猜想中,②(填序号)合理.
【反思讨论】学习小组结合图象,分析了丁同学实验过程中烧杯内溶液的变化.下列说法正确的是AB(填序号)
A.溶液质量逐渐增大 B.氯化钠质量逐渐增大,V2后不变
C.氯化钙的质量先增大后减小 D.溶液的pH一直增大.
8.2015年9月29日,美国宇航局(NASA)宣布.有证据显示火星上存在流动的水和霜冻,下列关于水的说法正确的是( )
| A. | 水凝固成冰发生了化学变化 | |
| B. | 氢氧两种元素只能组成一种物质--水 | |
| C. | 冰水混合物中只含一种分子 | |
| D. | 火星和地球上的水具有不同的元素组成 |
5.下列各组离子,在溶液中能大量共存的是( )
| A. | Ca2+、Cl-、Na+、CO32- | B. | H+、K+、NO3-、OH- | ||
| C. | SO42-、CO32-、Na+、H+ | D. | K+、Na+、NO3-、SO42- |
2.汽车尾气净化装置中发生的反应为2CO+2NO$\frac{\underline{\;Pt\;}}{\;}$2CO2+N2,对于该反应,下列说法错误的( )
| A. | N元素化合价降低 | B. | 反应产物不污染环境 | ||
| C. | Pt作催化剂 | D. | 该反应属于置换反应 |
9.生活中的“加碘盐”、“含氟牙膏”、“加铁酱油”,其中“碘”、“氟”、“铁”指的是( )
| A. | 原子 | B. | 离子 | C. | 分子 | D. | 元素 |
16.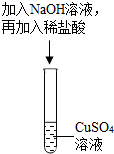 某化学课堂围绕“酸和碱的中和反应”,将学生分成若干小组开展探究活动.请你参与学习并填写空格.
某化学课堂围绕“酸和碱的中和反应”,将学生分成若干小组开展探究活动.请你参与学习并填写空格.
探究一:甲组同学设计了如图所示的实验,根据图示回答:
(1)在试管中加入约2mL硫酸铜溶液,然后滴入几滴氢氧化钠溶液,观察到的实验现象是产生蓝色沉淀.
(2)然后再向试管中加入稀盐酸,该实验通过稀盐酸与氢氧化铜(填物质名称)反应,观察到明显现象,验证了酸与碱能发生中和反应.
探究二:乙组同学将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中,一会儿后,发现忘记了滴加指示剂.于是他们从烧杯中取出少量反应后的溶液于试管中,滴入几滴酚酞溶液,振荡,观察到无明显现象.中和反应的化学方程式为H2SO4+2NaOH═Na2SO4+2H2O.
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质组成是什么?
【假设猜想】针对疑问,大家纷纷提出猜想
猜想一:只有Na2SO4
猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH
同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的是猜想三.
【实验探究】为了验证其余猜想,同学们利用烧杯中的溶液,进行如下方案的探究.
【得出结论】通过探究,同学们一致确定猜想二是正确的.
【评价反思】老师对同学们能用多种方法进行探究给予了肯定,同时指出实验方案中有一个是错误的,错误的原因是方案二只能证明溶液中含有SO42-,不能证明含有H2SO4.
 某化学课堂围绕“酸和碱的中和反应”,将学生分成若干小组开展探究活动.请你参与学习并填写空格.
某化学课堂围绕“酸和碱的中和反应”,将学生分成若干小组开展探究活动.请你参与学习并填写空格.探究一:甲组同学设计了如图所示的实验,根据图示回答:
(1)在试管中加入约2mL硫酸铜溶液,然后滴入几滴氢氧化钠溶液,观察到的实验现象是产生蓝色沉淀.
(2)然后再向试管中加入稀盐酸,该实验通过稀盐酸与氢氧化铜(填物质名称)反应,观察到明显现象,验证了酸与碱能发生中和反应.
探究二:乙组同学将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中,一会儿后,发现忘记了滴加指示剂.于是他们从烧杯中取出少量反应后的溶液于试管中,滴入几滴酚酞溶液,振荡,观察到无明显现象.中和反应的化学方程式为H2SO4+2NaOH═Na2SO4+2H2O.
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质组成是什么?
【假设猜想】针对疑问,大家纷纷提出猜想
猜想一:只有Na2SO4
猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH
同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的是猜想三.
【实验探究】为了验证其余猜想,同学们利用烧杯中的溶液,进行如下方案的探究.
| 实验方案 | 实验现象 | 结论与解释 |
方案一:滴加Na2CO3溶液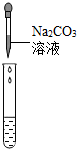 | 产生大量气泡 | 溶液中有H2SO4 |
方案二:滴加BaCl2溶液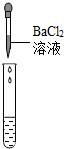 | 产生白色沉淀 | 溶液中有H2SO4 |
【评价反思】老师对同学们能用多种方法进行探究给予了肯定,同时指出实验方案中有一个是错误的,错误的原因是方案二只能证明溶液中含有SO42-,不能证明含有H2SO4.
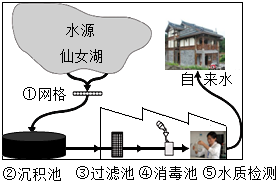 我市自来水的处理过程如图所示:
我市自来水的处理过程如图所示: