题目内容
9.下列离子组在强酸性和强碱性溶液中都能大量共存的是( )| A. | Ca2+、Cu2+、NO3-、Cl- | B. | Na+、Mg2+、SO42-、Cl-、 | ||
| C. | Na+、K+、CO32-、SO42- | D. | Na+、Ba2+、Cl-、NO3- |
分析 强酸性和强碱性溶液分别含有大量的H+、OH-.根据复分解反应发生的条件可知,若物质之间相互交换成分不能生成水、气体、沉淀,则能够在溶液中大量共存.
解答 解:强酸性和强碱性溶液分别含有大量的H+、OH-.
A、Cu2+和碱性溶液中的氢氧根离子能能结合生成氢氧化铜沉淀,在碱性溶液中不能大量共存,故选项错误.
B、Mg2+和碱性溶液中的氢氧根离子能能结合生成氢氧化镁沉淀,在碱性溶液中不能大量共存,故选项错误.
C、CO32-与酸性溶液中的氢离子能能结合生成水和二氧化碳,在酸性溶液中不能大量共存,故选项错误.
D、四种离子在溶液中相互交换成分不能生成沉淀、气体、水,能在酸性溶液和碱性溶液中大量共存,故选项正确.
故选:D.
点评 本题考查了离子共存的问题,判断各离子在溶液中能否共存,主要看溶液中的各离子之间能否发生反应生成沉淀、气体、水;还要注意是在酸性或碱性溶液中共存.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.下列可以作为溶质的是( )
| A. | 只有固体 | B. | 只有液体 | ||
| C. | 只有气体 | D. | 固体或液体或气体 |
1.根据常见酸碱盐的溶解性表的一部分信息填空.
表中物质都是由其对应行与列所表示的两种“成分”组成的,如物质④所在行为“Ca2+”,所在列为“NO3-”,则其化学式为Ca(NO3)2,说出物质③的一种用途是用于玻璃、造纸、纺织和洗涤剂的生产等,写出选用表中合适的两种“成分”组成物质来制备物质①的化学方程式Ba(OH)2+Na2SO4=BaSO4↓+2NaOH(合理即可).
| OH- | NO3- | SO42- | CO32- | |
| Ba2+ | 溶 | 溶 | 不① | 不 |
| Na+ | 溶 | 溶② | 溶 | 溶③ |
| Ca2+ | 溶 | 溶④ | 微 | 不 |
18.关于“舌尖上的化学”,下列说法不科学的是( )
| A. | 用甲醛溶液浸泡海产品,以延长保质期 | |
| B. | 为预防缺碘性疾病,可食用适量海带 | |
| C. | 食用“加铁酱油”,可补充铁元素,预防缺铁性贫血 | |
| D. | 为使发面食品松软可口,制作时可添加适量碳酸氢钠 |
19.有一包白色粉末,可能含有Ba(NO3)2、Na2SO4、Na2CO3、NaNO3中的一种或几种,为了确定其组成,实验小组设计并进行如表实验:
(1)实验中产生的气体是二氧化碳;
(2)通过探究,得出的结论是样品中一定有Ba(NO3)2、Na2CO3,一定没有Na2SO4,可能有NaNO3.
| 实验步骤 | 实验操作 | 实验现象 |
| 步骤1 | 取样品加入足量水,充分振荡,静置 | 有白色沉淀产生 |
| 步骤2 | 过滤后,往滤渣中加入过量的稀盐酸 | 沉淀全部溶解,并有气体产生 |
(2)通过探究,得出的结论是样品中一定有Ba(NO3)2、Na2CO3,一定没有Na2SO4,可能有NaNO3.
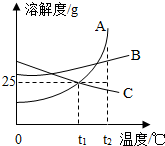 图中A、B、C分别表示三种不同的固体物质,其溶解度曲线如图所示.请回答下列问题:
图中A、B、C分别表示三种不同的固体物质,其溶解度曲线如图所示.请回答下列问题: