题目内容
19. 厉山中心学校的聪聪同学为了比较铁、铜和未知金属X的活动性大小,设计了如图所示实验.
厉山中心学校的聪聪同学为了比较铁、铜和未知金属X的活动性大小,设计了如图所示实验.(1)实验中可以观察到:金属丝X表面无明显现象,铁丝表面出现红色物质.写出有关反应的化学方程式Fe+CuS04=FeS04+Cu.
(2)三种金属的活动性大小由强到弱的顺序是Fe>Cu>X(未知金属用X表示).
分析 在金属活动性顺序中,位于前面的金属能把排在它后面的金属从其盐溶液中置换出来,据此判断能否发生反应,进而可确定三种金属活动性由强到弱的顺序.
解答 解:(1)金属丝X表面无明显现象,铁丝表面出现红色物质,说明X的金属活动性比铜弱,铁的金属活动性比铜强,铁能与硫酸铜溶液反应生成硫酸亚铁溶液和铜,反应的化学方程式为:Fe+CuS04=FeS04+Cu.
(2)金属丝X表面无明显现象,铁丝表面出现红色物质,说明X的金属活动性比铜弱,铁的金属活动性比铜强,即三种金属的活动性大小由强到弱的顺序是Fe>Cu>X.
故答案为:(1)Fe+CuS04=FeS04+Cu;(2)Fe>Cu>X.
点评 本题难度不大,考查金属活动性应用,掌握金属活动性应用“反应则活泼、不反应则不活泼”是正确解答此类题的关键.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
9.如图是工业上制备氢气的微观示意图,其中不同的“球”代表不同种原子.下列说法中不正确的是( )

| A. | 图中能表示氢分子的是 | |
| B. | 该反应中共涉及四种分子和三种原子 | |
| C. | 化学反应前后各元素化合价都不变 | |
| D. | 化学反应前后原子的种类和个数不变 |
7.实验室里用如图所示装置还原氧化铁,关于该实验下列说法正确的是( )

| A. | 玻璃管中发生的反应属于置换反应 | |
| B. | 该实验只说明了一氧化碳具有还原性 | |
| C. | 实验观察到的现象为红棕色固体变黑,澄清石灰水变浑浊 | |
| D. | 实验时,通入纯净一氧化碳的同时,点燃酒精喷灯给玻璃管加热 |
14.KNO3和KCl在不同温度时的溶解度如下表所示.请回答下列问题:
(1)10℃时,131g KCl饱和溶液,蒸发10g水后再降温到10℃,可析出KCl晶体的质量为3.1g.
(2)将一瓶接近饱和的硝酸钾溶液变成饱和溶液,可采用的方法是②④(填序号).
①升高温度 ②加溶质KNO3 ③加水 ④恒温蒸发水
(3)KNO3溶液中含有少量NaCl时,可通过冷却热饱和溶液的方法提纯.对上述提纯后析出的晶体和剩余溶液描述正确的是A(填序号).
A.剩余溶液一定是KNO3饱和溶液 B.剩余溶液一定是NaCl不饱和溶液
C.上述方法可以将两者完全分离 D.析出的晶体中只含有KNO3
(4)氯化钾是一种钾肥.20℃时,欲测定某KCl溶液的pH,若先将pH试纸用蒸馏水润湿再进行测定,则所测得溶液的pH会不受影响(填“偏大”、“偏小”或“不受影响”).
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
| KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 | |
(2)将一瓶接近饱和的硝酸钾溶液变成饱和溶液,可采用的方法是②④(填序号).
①升高温度 ②加溶质KNO3 ③加水 ④恒温蒸发水
(3)KNO3溶液中含有少量NaCl时,可通过冷却热饱和溶液的方法提纯.对上述提纯后析出的晶体和剩余溶液描述正确的是A(填序号).
A.剩余溶液一定是KNO3饱和溶液 B.剩余溶液一定是NaCl不饱和溶液
C.上述方法可以将两者完全分离 D.析出的晶体中只含有KNO3
(4)氯化钾是一种钾肥.20℃时,欲测定某KCl溶液的pH,若先将pH试纸用蒸馏水润湿再进行测定,则所测得溶液的pH会不受影响(填“偏大”、“偏小”或“不受影响”).
4.下列变化属于化学变化的是( )
| A. | 将石油炼制成汽油等 | B. | 将煤变成焦炭 | ||
| C. | 干冰气化 | D. | 加热法除去食盐中的碘 |
11.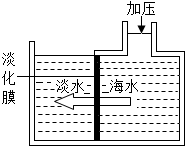 淡化海水可采用膜分离技术(如图),水分子可以透过膜(海水中其他粒子不能透过)进入左侧的池子,从而得到淡水.以下分析中正确的是( )
淡化海水可采用膜分离技术(如图),水分子可以透过膜(海水中其他粒子不能透过)进入左侧的池子,从而得到淡水.以下分析中正确的是( )
 淡化海水可采用膜分离技术(如图),水分子可以透过膜(海水中其他粒子不能透过)进入左侧的池子,从而得到淡水.以下分析中正确的是( )
淡化海水可采用膜分离技术(如图),水分子可以透过膜(海水中其他粒子不能透过)进入左侧的池子,从而得到淡水.以下分析中正确的是( )| A. | 这种膜可用滤纸代替 | B. | 左侧池中的淡水属于混合物 | ||
| C. | 右侧池中溶剂的质量减少 | D. | 右侧池中海水的溶质质量分数不变 |

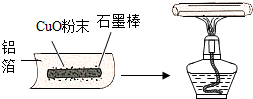 小洋和他的课外兴趣小组对碳还原氧化铜的实验进行了如下创新探究,取一根洁净的石墨棒,置于一张大小适宜的铝箱内,在其表面均匀撒上适量氧化铜粉末,将其包紧,置于酒精灯上加热(如图),几分钟后,冷却,拆开铝箱,发现氧化铜由黑色变为红色.
小洋和他的课外兴趣小组对碳还原氧化铜的实验进行了如下创新探究,取一根洁净的石墨棒,置于一张大小适宜的铝箱内,在其表面均匀撒上适量氧化铜粉末,将其包紧,置于酒精灯上加热(如图),几分钟后,冷却,拆开铝箱,发现氧化铜由黑色变为红色.