题目内容
8.某纯碱样品中混有少量的氯化钠,为了测定样品的纯度,小明做了如下实验:准确称取样品12.0g,向其中加入57.9g稀盐酸,恰好完全反应,共产生气体4.4g,请回答下列问题:(1)小明向纯碱样品中滴加稀盐酸,当观察倒恰好不再产生气泡时,说明所加盐酸与样品恰好完全反应.
(2)纯碱样品中的Na2CO3的质量分数是多少?(精确到0.1%)
(3)求反应后所得溶液溶质的质量分数是多少?
分析 (1)根据纯碱与盐酸反应分析;
(2)根据二氧化碳的质量利用化学方程式计算碳酸钠的质量,进而求质量分数;
(3)反应后所得溶液中NaCl包括原混合物中的氯化钠和反应生成的氯化钠.
解答 解:(1)向纯碱样品中滴加稀盐酸,当观察到恰好不再产生气泡时,说明所加盐酸与样品恰好完全反应;故答案为:恰好不再产生气泡;
(2)解:设12g纯碱样品中含Na2CO3的质量为x,生成NaCl 的质量为y
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 117 44
x y 4.4g
$\frac{106}{44}=\frac{x}{4.4g}$,
解得:x=10.6g,
$\frac{117}{44}=\frac{y}{4.4g}$,
解得:y=11.7g,
该纯碱样品中含Na2CO3的质量分数为:$\frac{106g}{12g}×100%=88.3%$;
(3)反应后所得溶液中NaCl 的质量为:12g-10.6g+11.7g=13.1g;
溶液中NaCl的质量分数为:$\frac{13.1g}{57.9g+12g-4.4g}×100%=20%$;
答:溶液中NaCl的质量分数为20%.
点评 反应后所得溶液中NaCl包括原混合物中的氯化钠和反应生成的氯化钠.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
18.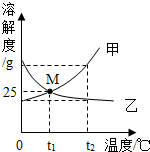 如图为甲、乙两物质(均不含结晶水)的溶解度曲线,下列说法错误的是( )
如图为甲、乙两物质(均不含结晶水)的溶解度曲线,下列说法错误的是( )
 如图为甲、乙两物质(均不含结晶水)的溶解度曲线,下列说法错误的是( )
如图为甲、乙两物质(均不含结晶水)的溶解度曲线,下列说法错误的是( )| A. | 乙的饱和溶液由t2℃降温到t1℃时,溶质的质量分数不变 | |
| B. | 除去甲中含有的少量乙,可以用冷却热饱和溶液的方法 | |
| C. | t1℃时,50g水中分别加入25g的甲、乙,均可得到75g的饱和溶液 | |
| D. | t1℃时,等质量甲、乙两物质的饱和溶液蒸发等质量的水,所得溶液中溶质的质量一定相等 |
16.向质量为m克的CaCO3和KHCO3的混合物中,加入质量分数为a%的稀盐酸n克,恰好完全反应后,得到二氧化碳的质量是w克.下列说法正确的是( )
| A. | 混合物中CaCO3和KHCO3的质量比一定是1:1 | |
| B. | 混合物充分反应后,所得溶液的质量是(m+n-w)克 | |
| C. | 混合物中CaCO3和KHCO3无论以任何比例混合,消耗稀盐酸的总质量均为n克 | |
| D. | 混合物中CaCO3和KHCO3无论以任何比例混合,生成二氧化碳的总质量均为w克 |
5.下列变化属于化学变化的是( )
| A. | 用醋除去暖水瓶中的水垢 | B. | 干冰致冷 | ||
| C. | 用玻璃刀刻划玻璃 | D. | 用木炭除去电冰箱中的异味 |
 厉山中心学校的聪聪同学为了比较铁、铜和未知金属X的活动性大小,设计了如图所示实验.
厉山中心学校的聪聪同学为了比较铁、铜和未知金属X的活动性大小,设计了如图所示实验.