题目内容
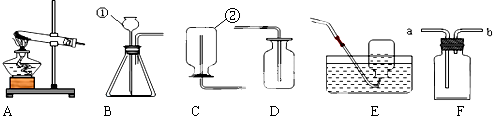
20.实验室常用的制取气体的发生装置如下:
①仪器a的名称是试管;搭建B装置时,酒精灯应在固定仪器a之前(选填“前”或“后”)放置.
②实验室用过氧化氢溶液和二氧化锰混合制取氧气,反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
③在实验室制取二氧化碳的研究中,进行了如下实验:
| 试验编号 药品 | 甲 | 乙 | 丙 | 丁 |
| 大理石 | mg,块状 | mg,块状 | mg,粉末状 | mg,粉末状 |
| 盐酸(过量) | wg,稀盐酸 | wg,浓盐酸 | wg,稀盐酸 | wg,浓盐酸 |
Ⅱ.若要研究盐酸浓度大小对反应的影响,可选择实验甲与乙对照(选填实验编号)
Ⅲ.除盐酸的浓度外,上述实验研究的另一个影响反应的因素是固体反应物的颗粒大小(或反应物的接触面积).
Ⅳ.研究发现酸的浓度越大,产生气体的速度越快,与甲比较,对丁分析正确的是ab(选填编号)
a.反应更为剧烈
b.最终剩余溶液的质量更小
c.产生二氧化碳的质量更大
d.粉末状大理石利用率更高
④下表中的两个实验,尽管在原料状态、发生装置等方面存在差异,却都能控制气体较平稳的产生.请从实验目的、原理、原料、装置、操作等方面思考后,具体阐述每个实验中气体较平稳产生的最主要的一个原因.
| 目的 | 原料 | 发生装置 | 气体较平稳产生的最主要的一个原因 |
| 制取二氧化碳 | 块状大理石 稀盐酸 | A | 反应物的接触面积较小 |
| 制取氧气 | 粉末状二氧化锰 3%的过氧化氢溶液 | C | 通过分液漏斗控制液体滴加速度 |
分析 ①根据常用仪器的名称以及组装仪器的顺序来分析;
②根据反应的原理来分析解答;
③大理石的主要成分是碳酸钙,与稀盐酸反应生成氯化钙、水和二氧化碳;根据实验数据分析比较解答;
④从反应物之间的接触面积和分液漏斗的特点来分析.
解答 解:①仪器a是试管,在组装B装置时,应先放好酒精灯,然后根据酒精灯的高度来安装试管,故填:试管;前;
②在二氧化锰的催化作用下,过氧化氢分解为氧气和水;故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
③Ⅰ、碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳;故填:CaCO3+2HCl═CaCl2+H2O+CO2↑;
Ⅱ、对比实验数据可见,甲和乙均为mg块状大理石,wg盐酸,但是盐酸的浓度不同,故填:乙;
Ⅲ、甲和丙对比,乙和丁对比可知,实验研究的另一个影响反应的因素是固体反应物的颗粒大小(或反应物的接触面积);故填:固体反应物的颗粒大小(或反应物的接触面积);
Ⅳ、甲和丁对比可知,丁中反应之间的接触面积大,盐酸浓度大,所以反应的速率更快;
丁为浓盐酸,具有挥发性,所以溶液的质量更小;
因为并不知道大理石与盐酸是否完全反应还是哪一种物质有剩余,故无法判断产生二氧化碳的质量粉末状大理石利用率.
故填:ab;
④用块状大理石与稀盐酸反应来较平稳的产生二氧化碳,是因为块状大理石与稀盐酸的接触面积较小;用过氧化氢来制取氧气时,用分液漏斗滴加过氧化氢溶液,这样就可以控制液体滴加的速度,从而得到了较平稳的氧气流.故填:反应物的接触面积较小;通过分液漏斗控制液体滴加速度.
点评 本题考查了对影响实验速率的因素的探究、化学方程式的书写以及仪器的组装,难度适中.

练习册系列答案
相关题目
15.鉴别物质的方法错误的是( )
| A. | 用酚酞鉴别食盐水和稀醋酸 | B. | 用水鉴别生石灰和石灰石 | ||
| C. | 用燃着的木条鉴别空气和二氧化碳 | D. | 用氯化钡溶液鉴别稀盐酸和稀硫酸 |
5.为了获取“铁的金属活动性比铜强”的证据,可以采用( )
| A. | 比较铁的利用范围是否比铜广 | |
| B. | 观察铁是否能置换硫酸铜溶液中的铜 | |
| C. | 观察铁表面的锈迹是否比铜多 | |
| D. | 比较铁的相对原子质量是否比铜小 |
12.法拉第曾以《蜡烛的故事》为题为青少年连续开展了多次报告.下列列举了报告中涉及的问题及对问题的回答,其中“对问题的回答”属于“设计实验方案”的是( )
| 选项 | 问题 | 对问题的回答 |
| A | 吹灭蜡烛时产生的白烟是什么? | 主要成分是烛油蒸气 |
| B | 火焰为什么向上? | 热气流上升,形成对流 |
| C | 火焰明亮的原因是什么? | 与火焰中有碳颗粒有关,碳颗粒会影响火焰明亮程度 |
| D | 火焰不同部位温度高低如何比较? | 用一张纸在火焰中心一掠,观察纸上留下的火痕特点 |
| A. | A | B. | B | C. | C | D. | D |
9.对下列事实的说明中,有错误的是( )
| A. | 氢气能还原氧化铜,说明氢气具有还原性 | |
| B. | 常温下氯酸钾能溶于水而难溶于酒精,说明氯酸钾的溶解性跟溶剂有关 | |
| C. | 相同条件下,湿衣服摊开比堆着干得快,说明水蒸发快慢与水的表面积有关 | |
| D. | 铁丝能在氧气中剧烈燃烧,说明氧气和铁丝都具有可燃性 |
10.小明最近腹泻,医生建议他暂时不要吃富含蛋白质和油脂的食物.所以小明应该选择的早餐是( )
| A. | 馒头和稀饭 | B. | 红烧肉盖饭和菜汤 | ||
| C. | 火腿三明治和牛奶 | D. | 奶油面包和酸奶 |
 1926年,我国著名化学家侯德榜先生创立了侯氏制碱法,促进了我国民族工业的发展和世界制碱技术的进步,其生产过程中有下列反应:
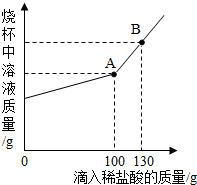
1926年,我国著名化学家侯德榜先生创立了侯氏制碱法,促进了我国民族工业的发展和世界制碱技术的进步,其生产过程中有下列反应: 学习了金属的有关知识后,同学们知道了如何鉴别黄金和黄铜(铜锌合金,俗名“愚人金”),为进一步定量分析黄铜的成分,某同学进行了如下实验,称量黄铜样品20g放入锥形瓶中,向其中不断加入稀硫酸,收集生成的气体与所加稀硫酸的质量关系如图所示,求:
学习了金属的有关知识后,同学们知道了如何鉴别黄金和黄铜(铜锌合金,俗名“愚人金”),为进一步定量分析黄铜的成分,某同学进行了如下实验,称量黄铜样品20g放入锥形瓶中,向其中不断加入稀硫酸,收集生成的气体与所加稀硫酸的质量关系如图所示,求: