题目内容
10.某学习小组利用下列装置进行气体的制取研究,请回答下列问题.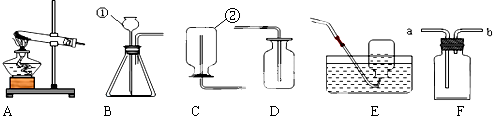
(1)写出有标号的仪器名称 ①长颈漏斗 ②集气瓶.
(2)选用高锰酸钾制取氧气的文字表达式高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气,该反应的基本反应类型是分解反应;选择的发生装置是A(填字母,下问如下),收集方法是D或E;若A、E连接,制取的氧气不纯的原因可能是刚产生气泡就收集,或刚开始集气瓶中未装满水(写一点即可).
(3)选用B装置制取氧气,用过氧化氢溶液和二氧化锰混合,其中二氧化锰的作用是催化作用,为了控制该反应速率,可将标号①仪器换成分液漏斗(或注射器).
(4)若将F装置收集氧气,则气体应从a端通入(填“a”或“b”).
若用F装置充满水收集氧气,则气体应从b端通入(填“a”或“b”).
分析 (1)熟练掌握常见的化学仪器及名称;
(2)高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;
如果操作不当,会导致收集的气体不纯;
(3)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
分液漏斗或注射器能够控制液体药品的流量,从而可以控制反应速率;
(4)氧气的密度比空气大,比水的密度小.
解答 解:(1)装置中标号仪器的名称:a试管;b集气瓶;
故填:试管;集气瓶;
(2)用高锰酸钾制氧气的发生装置特点属于固体加热型,所以应选择的发生装置是A;高锰酸钾受热分解为锰酸钾、二氧化锰和氧气,发生反应的文字表达式是:高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气,该反应属于分解反应;氧气的密度大于空气的密度,而且不易溶于水,所以用向上排空气法或排水法收集;
A、E连接,制取的氧气不纯的原因可能是刚产生气泡就收集,或刚开始集气瓶中未装满水.
故答案为:高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气;分解反应;A;D或E;刚产生气泡就收集,或刚开始集气瓶中未装满水.
(3)用过氧化氢溶液和二氧化锰混合,其中二氧化锰的作用是催化作用;为了控制该反应速率,可将标号①仪器换成分液漏斗或注射器.
故填:催化作用;分液漏斗(或注射器).
(4)若将F装置收集氧气,由氧气的密度比空气的密度大,则气体应从a端通入;氧气密度比水的密度小应从b通入.
故填:a;b.
点评 本题要熟练掌握根据反应物状态和反应条件选取气体的制取装置,根据气体的水溶性和密度选择收集装置及检验氧气的方法.

练习册系列答案
 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目
7. 如表是NaCl、NH4Cl在不同温度时的溶解度.
如表是NaCl、NH4Cl在不同温度时的溶解度.
(1)如图表示氯化铵溶解度曲线的是甲(填甲或者乙).
(2)t1的范围为0~20.
(3)将t2℃等质量的两种物质的饱和溶液降温至t1℃,对所得溶液的叙述正确的是③④⑤(填序号)
①溶质质量分数:甲>乙;
②溶液质量:甲>乙;
③所含溶剂质量:甲<乙;
④甲、乙都是饱和溶液;
⑤溶质质量:甲<乙.
 如表是NaCl、NH4Cl在不同温度时的溶解度.
如表是NaCl、NH4Cl在不同温度时的溶解度. | 温度/℃ | 0 | 20 | 40 | 60 | 80 | |
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | |
(2)t1的范围为0~20.
(3)将t2℃等质量的两种物质的饱和溶液降温至t1℃,对所得溶液的叙述正确的是③④⑤(填序号)
①溶质质量分数:甲>乙;
②溶液质量:甲>乙;
③所含溶剂质量:甲<乙;
④甲、乙都是饱和溶液;
⑤溶质质量:甲<乙.
8.属于物理变化的是( )
| A. | 冰川融化 | B. | 铁钉生锈 | C. | 蜡烛燃烧 | D. | 食物变质 |
5. 化学与我们的生活息息相关,它不仅为人类生活创造了丰厚的物质基础,而且为人类社会可持续发展作出了巨大贡献.
化学与我们的生活息息相关,它不仅为人类生活创造了丰厚的物质基础,而且为人类社会可持续发展作出了巨大贡献.
(1)市场上有些食品装在充满气体的塑料袋内,显得鼓鼓的.经询问得知:这样充气的包装,主要是为了使食品能较长时间保鲜、保质和不易压碎.那么,这是什么气体呢?
大明猜想是二氧化碳,小明猜想是氮气.
①假设大明的猜想正确,请你用实验方法证明.
②假如你是商家,你对食品包装袋中的气体有什么要求呢?(至少说出两点)无毒、不与物品反应、来源广、便宜等
(2)右图是化学中“有名”的装置,有如下用途:
①可以用做向上排空气法收集氧气,从a端进氧气.
②可以用做排水法收集氧气,在集气瓶中装满水,从b端进氧气.
③医院里给病人输氧为了给氧气加湿和观察氧气的输出速度也可以在氧气瓶和病人之间连接该装置,在集气瓶装半瓶水,将a端接氧气钢瓶,通过观察导管口向水中冒出的气泡的速度就知道氧气的输出速度.
 化学与我们的生活息息相关,它不仅为人类生活创造了丰厚的物质基础,而且为人类社会可持续发展作出了巨大贡献.
化学与我们的生活息息相关,它不仅为人类生活创造了丰厚的物质基础,而且为人类社会可持续发展作出了巨大贡献.(1)市场上有些食品装在充满气体的塑料袋内,显得鼓鼓的.经询问得知:这样充气的包装,主要是为了使食品能较长时间保鲜、保质和不易压碎.那么,这是什么气体呢?
大明猜想是二氧化碳,小明猜想是氮气.
①假设大明的猜想正确,请你用实验方法证明.
| 验证方法及操作 | 可能看到的现象 | 结论 |
(2)右图是化学中“有名”的装置,有如下用途:
①可以用做向上排空气法收集氧气,从a端进氧气.
②可以用做排水法收集氧气,在集气瓶中装满水,从b端进氧气.
③医院里给病人输氧为了给氧气加湿和观察氧气的输出速度也可以在氧气瓶和病人之间连接该装置,在集气瓶装半瓶水,将a端接氧气钢瓶,通过观察导管口向水中冒出的气泡的速度就知道氧气的输出速度.
20.实验室常用的制取气体的发生装置如下:

①仪器a的名称是试管;搭建B装置时,酒精灯应在固定仪器a之前(选填“前”或“后”)放置.
②实验室用过氧化氢溶液和二氧化锰混合制取氧气,反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
③在实验室制取二氧化碳的研究中,进行了如下实验:
Ⅰ.上述实验中反应的化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑.
Ⅱ.若要研究盐酸浓度大小对反应的影响,可选择实验甲与乙对照(选填实验编号)
Ⅲ.除盐酸的浓度外,上述实验研究的另一个影响反应的因素是固体反应物的颗粒大小(或反应物的接触面积).
Ⅳ.研究发现酸的浓度越大,产生气体的速度越快,与甲比较,对丁分析正确的是ab(选填编号)
a.反应更为剧烈
b.最终剩余溶液的质量更小
c.产生二氧化碳的质量更大
d.粉末状大理石利用率更高
④下表中的两个实验,尽管在原料状态、发生装置等方面存在差异,却都能控制气体较平稳的产生.请从实验目的、原理、原料、装置、操作等方面思考后,具体阐述每个实验中气体较平稳产生的最主要的一个原因.

①仪器a的名称是试管;搭建B装置时,酒精灯应在固定仪器a之前(选填“前”或“后”)放置.
②实验室用过氧化氢溶液和二氧化锰混合制取氧气,反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
③在实验室制取二氧化碳的研究中,进行了如下实验:
| 试验编号 药品 | 甲 | 乙 | 丙 | 丁 |
| 大理石 | mg,块状 | mg,块状 | mg,粉末状 | mg,粉末状 |
| 盐酸(过量) | wg,稀盐酸 | wg,浓盐酸 | wg,稀盐酸 | wg,浓盐酸 |
Ⅱ.若要研究盐酸浓度大小对反应的影响,可选择实验甲与乙对照(选填实验编号)
Ⅲ.除盐酸的浓度外,上述实验研究的另一个影响反应的因素是固体反应物的颗粒大小(或反应物的接触面积).
Ⅳ.研究发现酸的浓度越大,产生气体的速度越快,与甲比较,对丁分析正确的是ab(选填编号)
a.反应更为剧烈
b.最终剩余溶液的质量更小
c.产生二氧化碳的质量更大
d.粉末状大理石利用率更高
④下表中的两个实验,尽管在原料状态、发生装置等方面存在差异,却都能控制气体较平稳的产生.请从实验目的、原理、原料、装置、操作等方面思考后,具体阐述每个实验中气体较平稳产生的最主要的一个原因.
| 目的 | 原料 | 发生装置 | 气体较平稳产生的最主要的一个原因 |
| 制取二氧化碳 | 块状大理石 稀盐酸 | A | 反应物的接触面积较小 |
| 制取氧气 | 粉末状二氧化锰 3%的过氧化氢溶液 | C | 通过分液漏斗控制液体滴加速度 |
 对知识的及时整理与归纳是学习科学的重要方法,某同学在学习了硫酸的化学性质后,初步归纳出稀硫酸与其他物质相互反应的关系,如图所示(“-”表示相连的两种物质间发生的反应,五个圈中的物质属于不同的类别).
对知识的及时整理与归纳是学习科学的重要方法,某同学在学习了硫酸的化学性质后,初步归纳出稀硫酸与其他物质相互反应的关系,如图所示(“-”表示相连的两种物质间发生的反应,五个圈中的物质属于不同的类别).