题目内容
4.氢氧化钙俗称熟石灰,在生产和生活中有广泛的用途.(1)熟石灰可由生石灰溶于水制得,反应的化学方程式是:CaO+H2O═Ca(OH)2.测量其溶液的pH时,可以用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,再用标准比色卡比较试纸显示的颜色,读取该溶液的pH.
(2)用石灰浆粉刷墙壁,干燥后墙面变硬,反应的化学方程式是CO2+Ca(OH)2═CaCO3↓+H2O;
(3)用熟石灰来改良酸性土壤,反应的化学方程式是:Ca(OH)2+H2SO4═CaSO4+2H2O
(以土壤中含有硫酸为例).
(4)用熟石灰粉与草木灰(主要成分是K2CO3)按一定比例混合可制得高效环保农药“黑白粉”.使用时,选择在有露水的早晨,把“黑白粉”撒在植物茎叶上,可消除忌碱虫体.“黑白粉”比熟石灰更高效,是由于生成了碱性更强的KOH,反应的化学方程式是Ca(OH)2+K2CO3=CaCO3↓+2KOH.
分析 (1)根据生石灰溶于水生成熟石灰和溶液pH 的操作方法分析;
(2)石灰浆刷墙壁,涉及到的反应是氢氧化钙和二氧化碳反应;
(3)氢氧化钙与硫酸反应生成硫酸钙和水;
(4)氢氧化钙与碳酸钾反应生成碳酸钙和氢氧化钾.
解答 解:(1)生石灰与水反应生成氢氧化钙,反应的化学方程式为:CaO+H2O═Ca(OH)2.用pH试纸测定未知溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH.
(2)石灰浆中的主要成分是氢氧化钙,能与空气中的二氧化碳反应生成碳酸钙和水;碳酸钙是一种不溶于水的白色的坚硬的物质,干燥后墙面变得既白又硬,反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O.
(3)氢氧化钙与硫酸反应生成硫酸钙和水,反应的化学方程式为:Ca(OH)2+H2SO4═CaSO4+2H2O.
(4)氢氧化钙与碳酸钾反应生成碳酸钙和氢氧化钾,化学方程式为Ca(OH)2+K2CO3=CaCO3↓+2KOH;
故答案为:(1)CaO+H2O═Ca(OH)2;用玻璃棒蘸取少量待测液滴在干燥的pH试纸上;
(2)CO2+Ca(OH)2═CaCO3↓+H2O;
(3)Ca(OH)2+H2SO4═CaSO4+2H2O;
(4)Ca(OH)2+K2CO3=CaCO3↓+2KOH.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力等,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.如表所示的表格中列出了硝酸钾在不同温度下的溶解度:
(1)从表中能得到什么信息:硝酸钾的溶解度随着温度的升高逐渐增大.
(2)20℃时,将15克硝酸钾放入50克水中,充分溶解,得到的溶液是不饱和(填饱和或不饱和)溶液,若20克硝酸钾放入50克水中,所得溶液中溶质的质量分数13%.
| 温度℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度(克) | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
(2)20℃时,将15克硝酸钾放入50克水中,充分溶解,得到的溶液是不饱和(填饱和或不饱和)溶液,若20克硝酸钾放入50克水中,所得溶液中溶质的质量分数13%.
19.下列物质溶于水时,溶液温度明显降低的是( )
| A. | NH4NO3固体 | B. | 生石灰 | C. | 熟石灰 | D. | 食盐 |
9.“绿色化学”的主要内容之一是指从技术、经济上设计可行的化学反应,使原子充分利用,不产生污染物.下列化学反应符合“绿色化学”理念的是( )
| A. | 制CuSO4:Cu+2H2SO4(浓)═CuSO4+SO2↑+2H2O | |
| B. | 制CuSO4:2Cu+O2═2CuO; Cu+H2SO4(稀)═CuSO4+H2O | |
| C. | 制Cu(NO3)2:Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O | |
| D. | 制Cu(NO3)2:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O |
16.某同学在实验室进行有关浓硫酸的实验,观察到瓶上的标签所示,欲配制1000g质量分数为10%的稀硫酸,求(计算结果保留一位小数)
(1)1000g质量分数为10%的稀硫酸中含溶质硫酸多少克?
(2)需要多少mL浓硫酸?
(3)在配制1000g质量分数为10%的稀硫酸中,需要多少mL水?
(4)如取10mL10%稀硫酸加水稀释至20mL,则所得稀硫酸的质量分数为多少?(假设在此过程中,溶液的密度变化可忽略)
| 浓硫酸(H2SO4)500ml | |
| 溶质的质量分数 | 60% |
| 密度 | 1.5g/cm3 |
(2)需要多少mL浓硫酸?
(3)在配制1000g质量分数为10%的稀硫酸中,需要多少mL水?
(4)如取10mL10%稀硫酸加水稀释至20mL,则所得稀硫酸的质量分数为多少?(假设在此过程中,溶液的密度变化可忽略)
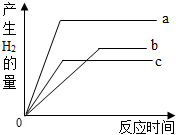 图是a、b、c三种金属在相同条件下与相同浓度的盐酸反应的图象,试回答:
图是a、b、c三种金属在相同条件下与相同浓度的盐酸反应的图象,试回答: