题目内容
17.下列化学方程式与事实相符的是( )| A. | 生石灰放置在空气中的质量增加:Ca(OH)2+CO2═CaCO3↓+H2O | |
| B. | 湿法冶铜的原理:Fe+CuSO4═Cu+FeSO4 | |
| C. | 氧氧化铝治疗胃酸过多:Al(OH)2+2HCI═AlCl2+2H2O | |
| D. | 木炭还原氧化铁:C+2FeO$\frac{\underline{\;高温\;}}{\;}$2Fe+C02↑ |
分析 根据化学方程式判断正误的方法需考虑:应用的原理是否正确;化学式书写是否正确;是否配平;反应条件是否正确;↑和↓的标注是否正确.
解答 解:A、生石灰放置在空气中的质量增加,是因为生石灰与水反应生成氢氧化钙,氢氧化钙与空气中的二氧化碳反应生成碳酸钙沉淀和水,反应的化学方程式分别为CaO+H2O═Ca(OH)2、Ca(OH)2+CO2═CaCO3↓+H2O,故选项错误.
B、该化学方程式书写完全正确.
C、该化学方程式中氢氧化铝与氯化铝的化学式书写错误,正确的化学方程式应为:Al(OH)3+3HCl═AlCl3+3H2O.
D、该化学方程式中氧化铁的化学式书写错误,正确的化学方程式应为3C+2Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe+3C02↑.
故选:B.
点评 本题难度不大,在解此类题时,首先分析应用的原理是否正确,然后再根据方程式的书写规则进行判断;化学方程式正误判断方法是:先看化学式是否正确,再看配平,再看反应条件,再看气体和沉淀,最后短线改成等号.

练习册系列答案
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案
相关题目
7.用含杂质(杂质不与酸作用,也不溶于水)的铁10克与50克稀硫酸完全反应后,滤去杂质,所得液体质量55.4克,则隔绝氧气蒸干后所得固体的质量为( )
| A. | 45.6g | B. | 15.2g | C. | 27.1g | D. | 77.6 |
8.下列变化中,属于化学变化的是( )
| A. | 海水晒盐 | B. | 冬天河水结冰 | ||
| C. | 分离空气制氧气 | D. | 煅烧石灰石制生石灰 |
12.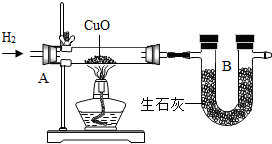 为了进一步测定水中的元素组成的质量比,某科技小组的同学设计了下列实验,通过称量反应前后装置A、B的质量,结果测得m(H):m(O)>1:8,比理论值偏高,其原因不可能是( )
为了进一步测定水中的元素组成的质量比,某科技小组的同学设计了下列实验,通过称量反应前后装置A、B的质量,结果测得m(H):m(O)>1:8,比理论值偏高,其原因不可能是( )
 为了进一步测定水中的元素组成的质量比,某科技小组的同学设计了下列实验,通过称量反应前后装置A、B的质量,结果测得m(H):m(O)>1:8,比理论值偏高,其原因不可能是( )
为了进一步测定水中的元素组成的质量比,某科技小组的同学设计了下列实验,通过称量反应前后装置A、B的质量,结果测得m(H):m(O)>1:8,比理论值偏高,其原因不可能是( )| A. | 通入的氢气未经过净化干燥 | |
| B. | 装置A内管口有水凝结 | |
| C. | 氧化铜没有完全还原 | |
| D. | 装置B同时吸收了空气中的水蒸气和CO2 |
2.已知IO3- 与I-可发生反应:IO3-+I-+6H+═3I2+3H2O,根据此反应,可用试纸和一些生活中常见的物质进行试验,证明加碘食盐中存在IO3-.可供选用的物质有:①自来水②蓝色石蕊试纸③碘化钾淀粉试纸④淀粉⑤食盐⑥食醋⑦白酒,进行上述实验时必须用到的物质是( )
| A. | ①③ | B. | ③⑥ | C. | ②④⑥ | D. | ①②④⑤⑦ |
9.下列的描述不属于所描述物质的物理性质的是( )
①将金属钠放入水中,发现金属钠能浮在水面并熔化成银白色的小球
②碳酸钠晶体受热易失去结晶水
③水垢能溶于醋酸中
④银白色的铁丝放在空气中会变成棕红色.
①将金属钠放入水中,发现金属钠能浮在水面并熔化成银白色的小球
②碳酸钠晶体受热易失去结晶水
③水垢能溶于醋酸中
④银白色的铁丝放在空气中会变成棕红色.
| A. | ①②③④ | B. | ①③④ | C. | ②③④ | D. | ②③ |
6. 如图是同学们经常使用的修正液包装标签.请你结合自己的生活经验和所学知识,推测下列说法不合理的是( )
如图是同学们经常使用的修正液包装标签.请你结合自己的生活经验和所学知识,推测下列说法不合理的是( )
 如图是同学们经常使用的修正液包装标签.请你结合自己的生活经验和所学知识,推测下列说法不合理的是( )
如图是同学们经常使用的修正液包装标签.请你结合自己的生活经验和所学知识,推测下列说法不合理的是( )| A. | 修正液是一种溶液,均一、透明 | B. | 修正液对环境有污染 | ||
| C. | 修正液的成分对纸张不具有腐蚀性 | D. | 修正液的溶剂易挥发 |
7.如图是KNO3和NaCl的溶解度曲线.下列说法中正确的是( )


| A. | NaCl的溶解度受温度的影响较大 | |
| B. | t1℃时,KNO3饱和溶液中溶质的质量分数是20% | |
| C. | 在温度高于t2℃范围内,KNO3的溶解度始终大于NaCl的溶解度 | |
| D. | t2℃时,NaCl饱和溶液与KNO3饱和溶液中,溶质的质量分数不一定相等 |
 南宋诗人赵师秀有诗“黄梅时节家家雨,青草池塘处处蛙.有约不来过夜半,闲敲棋子落灯花.”诗中“灯花”是蜡烛不完全燃烧产生的炭附着在蜡烛芯上的现象.
南宋诗人赵师秀有诗“黄梅时节家家雨,青草池塘处处蛙.有约不来过夜半,闲敲棋子落灯花.”诗中“灯花”是蜡烛不完全燃烧产生的炭附着在蜡烛芯上的现象.