题目内容
7.如图是KNO3和NaCl的溶解度曲线.下列说法中正确的是( )
| A. | NaCl的溶解度受温度的影响较大 | |
| B. | t1℃时,KNO3饱和溶液中溶质的质量分数是20% | |
| C. | 在温度高于t2℃范围内,KNO3的溶解度始终大于NaCl的溶解度 | |
| D. | t2℃时,NaCl饱和溶液与KNO3饱和溶液中,溶质的质量分数不一定相等 |
分析 根据题目信息和溶解度曲线可知:硝酸钾、氯化钠两种固体物质的溶解度,都是随温度升高而增大,而硝酸钾的溶解度随温度的升高变化比氯化钠大;t1℃时,KNO3饱和溶液中溶质的质量分数=$\frac{20g}{120g}×100%≈16.7%$,不是20%;在温度高于t2℃范围内,KNO3的溶解度始终大于NaCl的溶解度正确;t2℃时,NaCl饱和溶液与KNO3饱和溶液中,溶质的质量分数一定相等,因为在该温度下,它们的溶解度相等.
解答 解:A、硝酸钾的溶解度随温度的升高变化比氯化钠大,因此NaCl的溶解度受温度的影响较大是错误的,故选项错误;
B、t1℃时,KNO3饱和溶液中溶质的质量分数=$\frac{20g}{120g}×100%≈16.7%$,不是20%;故选项错误;
C、由溶解度曲线可知:在温度高于t2℃范围内,KNO3的溶解度始终大于NaCl的溶解度正确,故选项正确;
D、t2℃时,NaCl饱和溶液与KNO3饱和溶液中,溶质的质量分数一定相等,因为在该温度下,它们的溶解度相等,原叙述错误,故选项错误;
故选C
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液和溶质质量分数的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目
17.下列化学方程式与事实相符的是( )
| A. | 生石灰放置在空气中的质量增加:Ca(OH)2+CO2═CaCO3↓+H2O | |
| B. | 湿法冶铜的原理:Fe+CuSO4═Cu+FeSO4 | |
| C. | 氧氧化铝治疗胃酸过多:Al(OH)2+2HCI═AlCl2+2H2O | |
| D. | 木炭还原氧化铁:C+2FeO$\frac{\underline{\;高温\;}}{\;}$2Fe+C02↑ |
15.某校学习小组准备探究气体的测定和数据处理方法.
【提出问题】如何利用石灰石(主要成分为CaCO3)与稀盐酸反应来测定生成CO2的质量和体积,并处理数据.
【实验设计】通过如图1两个实验分别测定CO2的质量和体积:
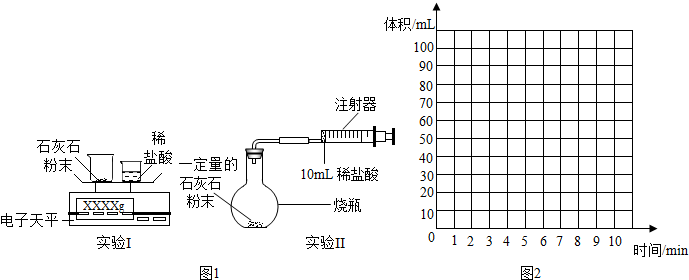
【分析与表达】
(1)实验I中,将小烧杯中的稀盐酸分几次加入到大烧杯中,并不断搅拌,判断石灰石中CaCO3完全反应的实验现象是最后一次加入稀盐酸,仍没有气泡产生.
(2)实验II中,先连接好装置,再检查装置的气密性(填操作名称),然后装好药品,最后将10ml稀盐酸快速推入烧瓶中.若稀盐酸是缓慢推入的,则可能造成的后果是烧瓶内气压增大,稀盐酸难以完全推入烧瓶中或仪器连接处脱落
【记录与处理】
(3)已知实验I反应前的总质量[m(大烧杯+石灰石粉末)+m(小烧杯+稀盐酸)],要计算生成CO2的质量,至少还需要的数据是AC.
A.m(小烧杯) B.m(大烧杯) C.m(大烧杯+反应后剩余物)
(4)实验II的实验记录如下(表中数据在相同温度、相同压强条件下测定):
①根据以上实验过程和数据综合分析,最终生成CO2的体积是80mL.
②根据你的认识,在坐标图中绘制出0~10min生成CO2体积随时间变化的曲线.
【反思与评价】
(5)经过分析,小明认为实验I的优点是实验操作简单或便于读数;你认为实验II的优点是在密闭体系内反应更加环保.
【提出问题】如何利用石灰石(主要成分为CaCO3)与稀盐酸反应来测定生成CO2的质量和体积,并处理数据.
【实验设计】通过如图1两个实验分别测定CO2的质量和体积:

【分析与表达】
(1)实验I中,将小烧杯中的稀盐酸分几次加入到大烧杯中,并不断搅拌,判断石灰石中CaCO3完全反应的实验现象是最后一次加入稀盐酸,仍没有气泡产生.
(2)实验II中,先连接好装置,再检查装置的气密性(填操作名称),然后装好药品,最后将10ml稀盐酸快速推入烧瓶中.若稀盐酸是缓慢推入的,则可能造成的后果是烧瓶内气压增大,稀盐酸难以完全推入烧瓶中或仪器连接处脱落
【记录与处理】
(3)已知实验I反应前的总质量[m(大烧杯+石灰石粉末)+m(小烧杯+稀盐酸)],要计算生成CO2的质量,至少还需要的数据是AC.
A.m(小烧杯) B.m(大烧杯) C.m(大烧杯+反应后剩余物)
(4)实验II的实验记录如下(表中数据在相同温度、相同压强条件下测定):
| 时间/min | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 注射器读数/ml | 60.0 | 85.0 | 88.0 | 89.0 | 89.5 | 89.8 | 89.9 | 90.0 | 90.0 | 90.0 |
②根据你的认识,在坐标图中绘制出0~10min生成CO2体积随时间变化的曲线.
【反思与评价】
(5)经过分析,小明认为实验I的优点是实验操作简单或便于读数;你认为实验II的优点是在密闭体系内反应更加环保.
19.下列实验操作能达到实验目的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 验证 NaCl 溶液中混有盐酸 | 取少量溶液,滴加无色酚酞溶液 |
| B | 除去粗盐中的难溶性杂质 | 将粗盐研碎、溶解、过滤、蒸发 |
| C | 除去铁制品上的铁锈 | 将铁制品长时间浸泡在过量的稀硫酸中 |
| D | 比较 Fe、Cu、Al 的金属活动性 | 铁丝浸入 CuSO4 溶液,铜丝浸入 AgNO3 溶液 |
| A. | A | B. | B | C. | C | D. | D |
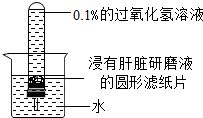 陈奇同学为研究肝脏研磨液中过氧化氢酶对过氧化氢分解的
陈奇同学为研究肝脏研磨液中过氧化氢酶对过氧化氢分解的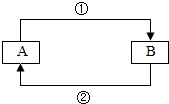 A、B是同学们在初中阶段学习化学过程中常会遇到的物质,在一定的条件下,它们之间相互转化的关系可用如图表示.
A、B是同学们在初中阶段学习化学过程中常会遇到的物质,在一定的条件下,它们之间相互转化的关系可用如图表示.