题目内容
6. 如图是同学们经常使用的修正液包装标签.请你结合自己的生活经验和所学知识,推测下列说法不合理的是( )
如图是同学们经常使用的修正液包装标签.请你结合自己的生活经验和所学知识,推测下列说法不合理的是( )| A. | 修正液是一种溶液,均一、透明 | B. | 修正液对环境有污染 | ||
| C. | 修正液的成分对纸张不具有腐蚀性 | D. | 修正液的溶剂易挥发 |
分析 A、根据使用前要摇匀考虑;
B、根据严禁食用考虑;
C、根据修正液是往纸上涂的考虑;
D、根据用完及时盖上帽考虑.
解答 解:A、使用前要摇匀说明不均一、不稳定,溶液是均一稳定的混合物,所以修正液不属于溶液,故A不合理;
B、修正液严禁食用,说明修正液中含有的化学物质可能有毒,会污染环境,故B说法合理;
C、修正液是往纸上涂的,所以说修正液的成分对纸张不具有腐蚀性,故C合理;
D、用完及时盖上帽,说明修正液的溶剂易挥发,盖上帽防止挥发,故D合理.
故选A.
点评 解答本题关键是要根据修改液标签中所提供的信息去分析和解决问题.

练习册系列答案
 优百分课时互动系列答案
优百分课时互动系列答案
相关题目
16.下列有关微粒的说法不正确的是( )
| A. | 分子、原子、离子都呈电中性 | |
| B. | 分子、原子和离子都能直接构成物质 | |
| C. | 原子由原子核与核外电子构成 | |
| D. | 原子与离子可以通过得失电子相互转化 |
17.下列化学方程式与事实相符的是( )
| A. | 生石灰放置在空气中的质量增加:Ca(OH)2+CO2═CaCO3↓+H2O | |
| B. | 湿法冶铜的原理:Fe+CuSO4═Cu+FeSO4 | |
| C. | 氧氧化铝治疗胃酸过多:Al(OH)2+2HCI═AlCl2+2H2O | |
| D. | 木炭还原氧化铁:C+2FeO$\frac{\underline{\;高温\;}}{\;}$2Fe+C02↑ |
14.石灰石是我省的主要矿产之一.学校研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数,取来了一些矿石样品50g,平均分成4份.进行实验,结果如下:
(1)哪几次反应中矿石有剩余?
(2)表中m和数值是多少?
(3)试计算这种石灰石矿中碳酸钙的质量分数.
(相对原子质量:H:1,Cl:35.5、O:16、Ca:40 C:12 )
| 实验 | 1 | 2 | 3 | 4 |
| 加入盐酸的质量/g | 50 | 100 | 150 | 200 |
| 生成CO2的质量/g | 1.76 | 3.52 | 4.4 | m |
(2)表中m和数值是多少?
(3)试计算这种石灰石矿中碳酸钙的质量分数.
(相对原子质量:H:1,Cl:35.5、O:16、Ca:40 C:12 )
11.下列所示实验操作中,正确的是( )
| A. |  | B. |  | C. |  | D. |  |
15.某校学习小组准备探究气体的测定和数据处理方法.
【提出问题】如何利用石灰石(主要成分为CaCO3)与稀盐酸反应来测定生成CO2的质量和体积,并处理数据.
【实验设计】通过如图1两个实验分别测定CO2的质量和体积:
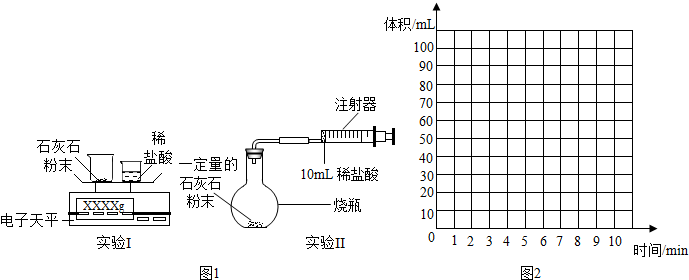
【分析与表达】
(1)实验I中,将小烧杯中的稀盐酸分几次加入到大烧杯中,并不断搅拌,判断石灰石中CaCO3完全反应的实验现象是最后一次加入稀盐酸,仍没有气泡产生.
(2)实验II中,先连接好装置,再检查装置的气密性(填操作名称),然后装好药品,最后将10ml稀盐酸快速推入烧瓶中.若稀盐酸是缓慢推入的,则可能造成的后果是烧瓶内气压增大,稀盐酸难以完全推入烧瓶中或仪器连接处脱落
【记录与处理】
(3)已知实验I反应前的总质量[m(大烧杯+石灰石粉末)+m(小烧杯+稀盐酸)],要计算生成CO2的质量,至少还需要的数据是AC.
A.m(小烧杯) B.m(大烧杯) C.m(大烧杯+反应后剩余物)
(4)实验II的实验记录如下(表中数据在相同温度、相同压强条件下测定):
①根据以上实验过程和数据综合分析,最终生成CO2的体积是80mL.
②根据你的认识,在坐标图中绘制出0~10min生成CO2体积随时间变化的曲线.
【反思与评价】
(5)经过分析,小明认为实验I的优点是实验操作简单或便于读数;你认为实验II的优点是在密闭体系内反应更加环保.
【提出问题】如何利用石灰石(主要成分为CaCO3)与稀盐酸反应来测定生成CO2的质量和体积,并处理数据.
【实验设计】通过如图1两个实验分别测定CO2的质量和体积:

【分析与表达】
(1)实验I中,将小烧杯中的稀盐酸分几次加入到大烧杯中,并不断搅拌,判断石灰石中CaCO3完全反应的实验现象是最后一次加入稀盐酸,仍没有气泡产生.
(2)实验II中,先连接好装置,再检查装置的气密性(填操作名称),然后装好药品,最后将10ml稀盐酸快速推入烧瓶中.若稀盐酸是缓慢推入的,则可能造成的后果是烧瓶内气压增大,稀盐酸难以完全推入烧瓶中或仪器连接处脱落
【记录与处理】
(3)已知实验I反应前的总质量[m(大烧杯+石灰石粉末)+m(小烧杯+稀盐酸)],要计算生成CO2的质量,至少还需要的数据是AC.
A.m(小烧杯) B.m(大烧杯) C.m(大烧杯+反应后剩余物)
(4)实验II的实验记录如下(表中数据在相同温度、相同压强条件下测定):
| 时间/min | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 注射器读数/ml | 60.0 | 85.0 | 88.0 | 89.0 | 89.5 | 89.8 | 89.9 | 90.0 | 90.0 | 90.0 |
②根据你的认识,在坐标图中绘制出0~10min生成CO2体积随时间变化的曲线.
【反思与评价】
(5)经过分析,小明认为实验I的优点是实验操作简单或便于读数;你认为实验II的优点是在密闭体系内反应更加环保.
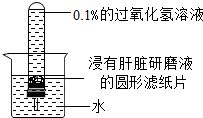 陈奇同学为研究肝脏研磨液中过氧化氢酶对过氧化氢分解的
陈奇同学为研究肝脏研磨液中过氧化氢酶对过氧化氢分解的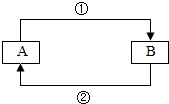 A、B是同学们在初中阶段学习化学过程中常会遇到的物质,在一定的条件下,它们之间相互转化的关系可用如图表示.
A、B是同学们在初中阶段学习化学过程中常会遇到的物质,在一定的条件下,它们之间相互转化的关系可用如图表示.