题目内容
过碳酸钠(2Na2CO3?3H2O2)广泛用于洗涤、纺织、医疗、造纸等.某兴趣小组展开了深入的学习:
【资料卡片】:
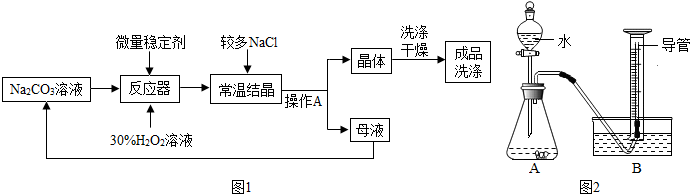
I、制备研究:如图1是制备过碳酸钠的工艺流程.
(1)过碳酸钠具有碳酸钠和过氧化氢的双重性质,不稳定,受热,遇水易分解;
(2)过碳酸钠分解的化学方程式为2(2Na2CO3?3H2O2)=4Na2CO3+6H2O+3O2↑
(3)H2O2分解放出热量,Na2CO3受热不分解;
请回答问题:
(1)操作A的名称是 ,若在实验室完成此操作,需要的玻璃仪器是烧杯、玻璃棒和 .
(2)生产中,反应及干燥均需在较低温度下进行,原因是 .
(3)加入较多的氯化钠的作用是 .
Ⅱ、纯度测定:测定过碳酸钠样品(杂质不溶于水)中2Na2CO3?3H2O2的质量分数.小组同学设计了如图2所示实验装置(部分仪器略去),并进行实验.
【实验步骤】
①连接仪器,检查装置的气密性;
②将过碳酸钠样品(2.20g)和少许黑色粉末均匀混合后置于装置A中,在量筒中加满水;
③连接仪器,打开分液漏斗活塞,缓缓滴入水;
④待装置A中不再产生气泡时,停止加水,并关闭活塞;
⑤待量筒中水面不再变化时,记录其中水面刻度;
⑥根据数据进行计算.
【实验分析及数据处理】
(4)实验中, ,则开始收集气体.
A.刚开始出现气泡时
B.当气泡均匀连续出现时
C.若用带火星木条放在导管口部,复燃时
(5)若量筒中收集到气体的体积是224mL(换算后质量约为0.32g),计算过碳酸钠样品中2Na2CO3?3H2O2的质量分数为多少?[已知:Mr(2Na2CO3?3H2O2)=314,保留到0.1%】
【反思】
(6)量筒中长导管的作用是 .
【资料卡片】:

I、制备研究:如图1是制备过碳酸钠的工艺流程.
(1)过碳酸钠具有碳酸钠和过氧化氢的双重性质,不稳定,受热,遇水易分解;
(2)过碳酸钠分解的化学方程式为2(2Na2CO3?3H2O2)=4Na2CO3+6H2O+3O2↑
(3)H2O2分解放出热量,Na2CO3受热不分解;
请回答问题:
(1)操作A的名称是
(2)生产中,反应及干燥均需在较低温度下进行,原因是
(3)加入较多的氯化钠的作用是
Ⅱ、纯度测定:测定过碳酸钠样品(杂质不溶于水)中2Na2CO3?3H2O2的质量分数.小组同学设计了如图2所示实验装置(部分仪器略去),并进行实验.
【实验步骤】
①连接仪器,检查装置的气密性;
②将过碳酸钠样品(2.20g)和少许黑色粉末均匀混合后置于装置A中,在量筒中加满水;
③连接仪器,打开分液漏斗活塞,缓缓滴入水;
④待装置A中不再产生气泡时,停止加水,并关闭活塞;
⑤待量筒中水面不再变化时,记录其中水面刻度;
⑥根据数据进行计算.
【实验分析及数据处理】
(4)实验中,
A.刚开始出现气泡时
B.当气泡均匀连续出现时
C.若用带火星木条放在导管口部,复燃时
(5)若量筒中收集到气体的体积是224mL(换算后质量约为0.32g),计算过碳酸钠样品中2Na2CO3?3H2O2的质量分数为多少?[已知:Mr(2Na2CO3?3H2O2)=314,保留到0.1%】
【反思】
(6)量筒中长导管的作用是
考点:物质的相互转化和制备,实验探究物质的组成成分以及含量,过滤的原理、方法及其应用,结晶的原理、方法及其应用,常用气体的收集方法,根据化学反应方程式的计算
专题:物质的制备,科学探究
分析:(1)根据过碳酸钠的溶解度大小考虑;
(2)根据不溶于液体的固体和液体分离的方法和过滤操作用到的仪器考虑;
(3)根据过碳酸钠的溶解度大小考虑;
(4)根据开始锥形瓶中有空气,最后锥形瓶中留有制取的气体考虑;
(5)先将氧气的体积换算成质量,再根据氧气的质量计算出过碳酸钠的质量,再除以样品的质量;
(6)根据如果使用短导管造成的后果考虑;
(2)根据不溶于液体的固体和液体分离的方法和过滤操作用到的仪器考虑;
(3)根据过碳酸钠的溶解度大小考虑;
(4)根据开始锥形瓶中有空气,最后锥形瓶中留有制取的气体考虑;
(5)先将氧气的体积换算成质量,再根据氧气的质量计算出过碳酸钠的质量,再除以样品的质量;
(6)根据如果使用短导管造成的后果考虑;
解答:解:
(1)过碳酸钠在NaCl溶液中溶解度较小,所以生产过程中,加入较多的NaCl,以便过碳酸钠晶体析出;
(2)不溶于液体的固体和液体分离的方法是过滤,过滤时要用到铁架台、漏斗、烧杯、玻璃棒,所以需要的玻璃仪器是烧杯、漏斗、玻璃棒;
(3)过碳酸钠在NaCl溶液中溶解度较小,所以生产过程中,加入较多的NaCl,以便过碳酸钠晶体析出;
(4)开始锥形瓶中有空气,最后锥形瓶中留有制取的氧气,两者体积相同,所以一开始就应当收集,故选A;
(5)过碳酸钠分解产生氧气质量为224mL×10-3×1.43g?L-1=0.32g
2(2Na2CO3?3H2O2)═4Na2CO3+6H2O+3O2↑
628 96
X 0.32g
根据
=
,解得X=2.09g
则样品中,2Na2CO3?3H2O2的质量分数为:
×100%=95.0%
(6)如果使用短导管由于温度降低后会使水沿着导管倒吸入锥形瓶内,所以量筒中长导管的作用是起缓冲作用,防止温度降低至室温时,测量结果产生偏差(或防倒吸).
故答案为:
(1)过滤;漏斗;(2)过碳酸钠受热易分解,从而影响产量和产率;
(3)过碳酸钠在NaCl溶液中溶解度较小,易析出晶体;(4)A;
(5)95.0%;(6)起缓冲作用,防止温度降低至室温时,测量结果产生偏差(或防倒吸).
(1)过碳酸钠在NaCl溶液中溶解度较小,所以生产过程中,加入较多的NaCl,以便过碳酸钠晶体析出;
(2)不溶于液体的固体和液体分离的方法是过滤,过滤时要用到铁架台、漏斗、烧杯、玻璃棒,所以需要的玻璃仪器是烧杯、漏斗、玻璃棒;
(3)过碳酸钠在NaCl溶液中溶解度较小,所以生产过程中,加入较多的NaCl,以便过碳酸钠晶体析出;
(4)开始锥形瓶中有空气,最后锥形瓶中留有制取的氧气,两者体积相同,所以一开始就应当收集,故选A;
(5)过碳酸钠分解产生氧气质量为224mL×10-3×1.43g?L-1=0.32g
2(2Na2CO3?3H2O2)═4Na2CO3+6H2O+3O2↑
628 96
X 0.32g
根据
| 628 |
| 96 |
| X |
| 0.32g |
则样品中,2Na2CO3?3H2O2的质量分数为:
| 2.09g |
| 2.20g |
(6)如果使用短导管由于温度降低后会使水沿着导管倒吸入锥形瓶内,所以量筒中长导管的作用是起缓冲作用,防止温度降低至室温时,测量结果产生偏差(或防倒吸).
故答案为:
(1)过滤;漏斗;(2)过碳酸钠受热易分解,从而影响产量和产率;
(3)过碳酸钠在NaCl溶液中溶解度较小,易析出晶体;(4)A;
(5)95.0%;(6)起缓冲作用,防止温度降低至室温时,测量结果产生偏差(或防倒吸).
点评:本题考查了过碳酸钠、碳酸钠的化学性质及有关溶液及化学方程式的计算,注重考查学生的分析能力和基本计算能力.

练习册系列答案
相关题目
每年5月31日为世界无烟日,吸烟有害健康,烟气中一定含有的有毒气体是( )
| A、O2 |
| B、N2 |
| C、CO2 |
| D、CO |
下列变化属于化学变化的是( )
| A、洗衣服晾干 |
| B、自行车爆胎 |
| C、燃放烟花爆竹 |
| D、冰棒融化 |

