题目内容
下列是酸、碱、盐的一些用途,写出相关的化学方程式:
(1)用含氢氧化铝的胃舒平治疗胃酸过多的患者: .
(2)某些工厂用稀硫酸清洗铁制品表面的铁锈(主要成分氧化铁): ;溶液由无色变为 色.
(3)用烧碱溶液吸收工业废气中的SO2,以减少污染: ,该反应 (是不是)复分解反应.
(4)将少量硫酸铵晶体与熟石灰混合研磨: ;研磨一段时间后,在研钵中可看到的现象是 .
(5)工业生产通过电解饱和食盐水得到烧碱、氯气、氢气: .
(1)用含氢氧化铝的胃舒平治疗胃酸过多的患者:
(2)某些工厂用稀硫酸清洗铁制品表面的铁锈(主要成分氧化铁):
(3)用烧碱溶液吸收工业废气中的SO2,以减少污染:
(4)将少量硫酸铵晶体与熟石灰混合研磨:
(5)工业生产通过电解饱和食盐水得到烧碱、氯气、氢气:
考点:书写化学方程式、文字表达式、电离方程式,反应类型的判定
专题:化学用语和质量守恒定律
分析:首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可
解答:解:(1)氢氧化铝与胃液中的盐酸反应生成氯化铝和水,反应的化学方程式为:Al(OH)3+3HCl═AlCl3+3H2O.
(2)铁锈的主要成分是氧化铁,与硫酸反应生成硫酸铁和水,反应的化学方程式是:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;溶液由无色变为黄色.
(3)用烧碱溶液吸收工业废气中的SO2生成亚硫酸钠和水,反应的化学方程式是:2NaOH+SO2=Na2SO3+H2O;该反应不是两种化合物相互交换成分生成两种新的化合物的反应,不属于复分解反应.
(4)硫酸铵晶体与熟石灰混合研磨生成氨气、水和硫酸钙,反应的化学方程式为:(NH4)2SO4+Ca(OH)2=CaSO4+2NH3↑+2H2O;该反应有水生成,研磨一段时间后,在研钵中可看到研钵内固体变潮(变湿).
(5)工业生产通过电解饱和食盐水得到烧碱、氯气、氢气,反应的化学方程式为:2NaCl+2H2O
2NaOH+H2↑+Cl2↑.
故答案为:(1)Al(OH)3+3HCl═AlCl3+3H2O;
(2)Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;黄;
(3)2NaOH+SO2=Na2SO3+H2O;不是;
(4)(NH4)2SO4+Ca(OH)2=CaSO4+2NH3↑+2H2O;研钵内固体变潮(变湿);
(5)2NaCl+2H2O
2NaOH+H2↑+Cl2↑.
(2)铁锈的主要成分是氧化铁,与硫酸反应生成硫酸铁和水,反应的化学方程式是:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;溶液由无色变为黄色.
(3)用烧碱溶液吸收工业废气中的SO2生成亚硫酸钠和水,反应的化学方程式是:2NaOH+SO2=Na2SO3+H2O;该反应不是两种化合物相互交换成分生成两种新的化合物的反应,不属于复分解反应.
(4)硫酸铵晶体与熟石灰混合研磨生成氨气、水和硫酸钙,反应的化学方程式为:(NH4)2SO4+Ca(OH)2=CaSO4+2NH3↑+2H2O;该反应有水生成,研磨一段时间后,在研钵中可看到研钵内固体变潮(变湿).
(5)工业生产通过电解饱和食盐水得到烧碱、氯气、氢气,反应的化学方程式为:2NaCl+2H2O
| ||
故答案为:(1)Al(OH)3+3HCl═AlCl3+3H2O;
(2)Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;黄;
(3)2NaOH+SO2=Na2SO3+H2O;不是;
(4)(NH4)2SO4+Ca(OH)2=CaSO4+2NH3↑+2H2O;研钵内固体变潮(变湿);
(5)2NaCl+2H2O
| ||
点评:本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
相关题目
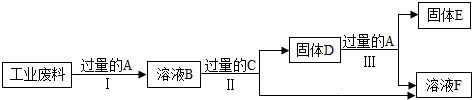
 已知A、B、C、D是初中化学常见的物质.它们之间的转化关系如图所示(部分物质和反应条件略去),其中A被看作是理想的“绿色能源”,B在常温下是无色液体,C可用于灭火.请回答下列问题:
已知A、B、C、D是初中化学常见的物质.它们之间的转化关系如图所示(部分物质和反应条件略去),其中A被看作是理想的“绿色能源”,B在常温下是无色液体,C可用于灭火.请回答下列问题:
 儿童缺锌会引起食欲不振、发育不良.如图为某种补锌口服液说明书的一部分,请回答:
儿童缺锌会引起食欲不振、发育不良.如图为某种补锌口服液说明书的一部分,请回答: A、B、C、D、E是初中常见的物质.它们的转化关系如图所示(部分物质已略去),其中A、B、C中均含有相同的金属元素,D、E是植物进行光合作用的物质.
A、B、C、D、E是初中常见的物质.它们的转化关系如图所示(部分物质已略去),其中A、B、C中均含有相同的金属元素,D、E是植物进行光合作用的物质.