题目内容
3.有一包固体粉末,可能由CuSO4、CaCO3 和Na2SO4 中的一种或几种所组成.华雪为了确定它的成分,进行了如下实验: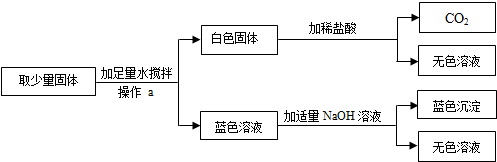
(1)操作a的名称是过滤(填“蒸发”或“过滤”),其中必须要用到的玻璃仪器有烧杯、玻璃棒和漏斗.
(2)写出蓝色沉淀的化学式:Cu(OH)2.
(3)白色固体是CaCO3,它与稀盐酸反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑,该反应所属基本反应类型为复分解反应.
(4)华雪通过实验后认为:这包固体粉末中只有两种物质.他的判断是错误(填“正确”或“错误”)的,理由是无法判断是否存在Na2SO4.
分析 (1)根据结果操作a得到固体和液体两种状态的物质分析操作及需要的仪器;
(2)根据蓝色沉淀是蓝色溶液和氢氧化钠反应产生的,可知含有硫酸铜,产生氢氧化铜蓝色沉淀;
(3)根据物质溶于水得到白色沉淀,可知是原有的难溶性碳酸钙,没有两两反应产生的沉淀,故只有碳酸钙,和稀盐酸反应产生氯化钙、水和二氧化碳,写出反应的方程式并判断反应类型;
(4)根据推断的物质一定含有碳酸钙、硫酸铜,可能含有硫酸钠分析
解答 解:(1)经过操作a得到难溶性固体和蓝色溶液,可知是过滤,需要的仪器有:铁架台、烧杯、玻璃棒和漏斗,其中缺少的玻璃仪器是漏斗;
(2)溶液呈现蓝色的是硫酸铜,和氢氧化钠反应产生的氢氧化铜是蓝色的沉淀,化学式为:Cu(OH)2;
(3)白色固体是难溶性的碳酸钙,化学式为:CaCO3;稀盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,故反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;该反应是酸和盐发生的复分解反应;
(4)经过推断一定含有的物质是碳酸钙、硫酸铜,而硫酸钠不影响实验的现象,所以可能含有硫酸钠,因此认为这包固体粉末中只有两种物质的判断是错误的,因为无法判断是否存在Na2SO4.
故答案为(1)过滤,漏斗;
(2)Cu(OH)2;
(3)CaCO3,CaCO3+2 HCl═CaCl2+H2O+CO2↑,复分解;
(4)错误,无法判断Na2SO4是否存在.
点评 在解此类题时,首先从物质的颜色、物质之间的关系,然后根据现象推出可以确定存在或不存在的物质,对于现象不能确定的只能再设计实验进行验证.

练习册系列答案
相关题目
8.下列解释不合理的是( )
| A. | 常温下双氧水能分解而水不分解-二者中水分子的数量不同 | |
| B. | 空气是混合物-空气由很多不同的分子聚集而成 | |
| C. | 湿衣服在夏天比在冬天容易干-温度越高分子运动速率越快 | |
| D. | 在一定条件下氧气变成臭氧-在化学变化中分子发生改变 |
15.下列反应中不属于化合反应的是( )
| A. | 硫+氧气$\stackrel{点燃}{→}$ 二氧化硫 | B. | 镁+氧气$\stackrel{点燃}{→}$氧化镁 | ||
| C. | 红磷+氧气$\stackrel{点燃}{→}$ 五氧化二磷 | D. | 石蜡+氧气$\stackrel{点燃}{→}$ 二氧化碳+水 |