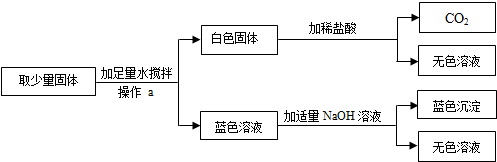
题目内容
11.质量守恒定律是物质科学中的一条重要规律,具体表述为:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和.某科学兴趣小组的同学设计了如下实验装置(天平略)来验证质量守恒律,请回答下列问题:(1)天辰同学将橡皮塞上的细玻璃管下端放到酒精灯火焰上灼烧至红热后,迅速用橡皮塞将锥形瓶塞紧,并引燃白磷(白磷着火点为40℃),实验过程如图所示.
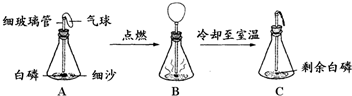
①写出锥形瓶中白磷燃烧反应的方程式4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
②实验中气球的作用是防止气体逸出;
③实验观察到A、C中气球的大小不同,用理化知识解释产生此现象的原因是红磷燃烧消耗氧气,生成固体五氧化二磷,使瓶中压强变小,小于外界大气压,在大气压的作用下,C中气球变小,A内压强等于外界大气压,所以A、C中气球大小不同;
(2)吴洋同学设计了如下图A和B的实验来验证质量守恒定律,志强同学立即反对,认为这两套装置都不能用来验证质量守恒.志强同学认为A实验不行的理由是酒精和水混合不会发生化学变化,所以不能用质量守恒定律解释,认为B实验不行的理由是盐酸和碳酸钙反应生成二氧化碳气体,生成的二氧化碳气体逸出,所以B实验也不适用于验证质量守恒定律;
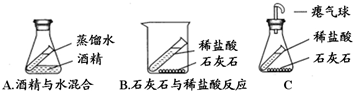
(3)昊鑫同学将B装置进行改进,如图C所示:
①C中发生的化学反应方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
②待完全反应后,将装置C置于天平上称量,所得数据较反应前的小.若整个操作过程无任何差错,装置气密性也良好,则造成上述实验误差的原因是气球变大后,受到空气的浮力,方向竖直向上,导致天平称量反应后物质质量的读数偏小.
分析 (1)①根据化学方程式的书写方法进行分析解答;
②根据白磷燃烧放出热量使瓶内压强变大进行解答;
③根据气球的大小与锥形瓶内气体的压强大小有关,若外界大气压大于锥形瓶内气体压强,气球将变小.可根据反应后气体的体积的变化结合压强有关知识进行分析解答;
(2)根据质量守恒定律适用于化学反应以及盐酸和碳酸钙反应生成二氧化碳气体,生成的二氧化碳气体逸出进行解答;
(3)根据盐酸和碳酸钙反应生成氯化钙、水和二氧化碳进行解答.
解答 解:(1)①白磷被引燃后,生成五氧化二磷,发生反应的方程式是4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;故答案为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
②白磷燃烧放出热量使瓶内压强变大,大于外界大气压,从而气球变大,所以气球的作用是防止气体逸出;故填:防止气体逸出;
③观察到A、C中气球的大小不同,解释产生此现象的原因是:内外产生了压强差;即红磷燃烧消耗氧气,生成固体五氧化二磷,使瓶中压强变小,小于外界大气压,在大气压的作用下,C中气球变小,A内压强等于外界大气压,所以A、C中气球大小不同.故答案为:红磷燃烧消耗氧气,生成固体五氧化二磷,使瓶中压强变小,小于外界大气压,在大气压的作用下,C中气球变小,A内压强等于外界大气压,所以A、C中气球大小不同;故
(2)质量守恒定律适用于化学反应,酒精和水混合不会发生化学变化,所以不能用质量守恒定律解释,而盐酸和碳酸钙反应生成二氧化碳气体,生成的二氧化碳气体逸出,所以B实验也不适用于验证质量守恒定律;故填:酒精和水混合不会发生化学变化,所以不能用质量守恒定律解释;盐酸和碳酸钙反应生成二氧化碳气体,生成的二氧化碳气体逸出,所以B实验也不适用于验证质量守恒定律;
(3)①盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,发生的化学反应方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;故填:CaCO3+2HCl═CaCl2+H2O+CO2↑;
②由于气球体积比较大受到的浮力就比较大,所以气球变大后,受到空气的浮力,方向竖直向上,导致天平称量反应后物质质量的读数偏小.故填:气球变大后,受到空气的浮力,方向竖直向上,导致天平称量反应后物质质量的读数偏小.
点评 本题考查质量守恒定律的实验验验证和实验装置的选择,所以正确理解质量守恒定律和根据反应特点,即反应物和生成物中是否有气体或者烟雾,选择什么样的装置是解决本题的关键.

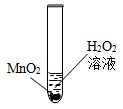 小红想研究影响过氧化氢(H2O2)分解速度的因素.在四支试管中分别加入0.2g二氧化锰粉末,然后加入等量的不同溶质质量分数的过氧化氢溶液,观察气泡产生的速度,记录如下:
小红想研究影响过氧化氢(H2O2)分解速度的因素.在四支试管中分别加入0.2g二氧化锰粉末,然后加入等量的不同溶质质量分数的过氧化氢溶液,观察气泡产生的速度,记录如下:| 实验次数 | 1 | 2 | 3 | 4 |
| H2O2溶液的溶质质量分数 | 1% | 5% | 10% | 15% |
| MnO2质量 | 0.2g | 0.2g | 0.2g | 0.2g |
| 气泡产生的速度 | + | ++ | +++ | ++++ |
(2)为了检验产生的气体是否为氧气,请你写出检验的方法:将带火星的木条伸入试管中,如果木条复燃,则证明该气体为氧气.
(3)实验完毕,可利用过滤法回收剩余溶液中的二氧化锰粉末.在过滤过程中,下列仪器不需要的有B.要完成该实验还缺少的一种玻璃仪器的名称为漏斗.
A.玻璃棒 B.酒精灯 C. 托盘天平 D.烧杯.
| A. | 在反应前后化学性质不变 | B. | 在反应前后质量不变 | ||
| C. | 在反应中使氧气的量增多 | D. | 在反应中加快反应速率 |
(1)收集竹子中的气体.
小华提出:将一节竹子浸没在水中,在竹子上钻孔,用排水法收集气体.
小刚提出:可用注射器从竹子中抽取气体.
大家认为两人的想法都可行,于是分为A、B两组,在相同的条件下,A组采用小华的取气方法,B组采用小刚的取气方法,分别完成下面的实验.
(2)检验气体中是否含有二氧化碳气体.
| 实验步骤 | 实验现象 | 实验结论及解释 |
| 向所取气体中加入 澄清石灰水,振荡. | 有二氧化碳,化学反应文字表达式为: 氢氧化钙+二氧化碳→碳酸钙+水. |
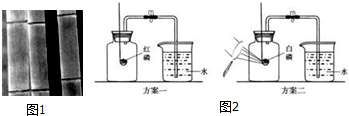
【设计实验】同学们设计了如图2所示的方案一和方案二来测定氧气含量.
【进行实验】按上述两个方案进行多次实验.
反思与评价】
a.实验中磷的量应为足量,原因是将集气瓶中的氧气消耗完.
b.两个方案的测定结果不同,大家认为方案二测定结果比较准确,原因是在实验过程中装置一直密封,可以避免白烟或空气受热膨胀逸出.
c.经过A、B两组同学的实验,A组测得的含氧量总是大于B组,你认为原因是燃烧匙中燃烧的红磷进入集气瓶时,一部分空气受热膨胀溢出.
| A. | m | B. | 2m | C. | $\frac{m}{2}$ | D. | 4m |
| A. | 两个氮原子N2 | B. | 两个氢分子2H | C. | 两个铁离子2Fe2+ | D. | 氨气NH3 |