题目内容
7.实验室用如图1所示裝置的部分或全部组合后完成如下实验,请回答下列问题.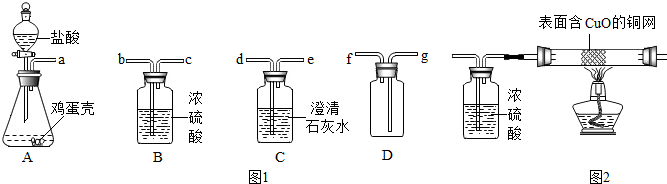
(1)鸡蛋壳的主要成分是碳酸钙,A装置中发生反置的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑,A与C相连后C中的现象为澄清的石灰水变浑浊.
(2)若将A装置中的药品换成稀硫酸和锌粒,产生的H2经干燥后用D装置收集,当D装置的瓶口向下时,导管口的连接顺序应是a→b→c→g.
(3)若将A装置中的药品换成硫酸铜溶液和铁粉,发现生成红色固体物质的同时有较多的气泡放出.老师提示,该反应生成的气体只有一种.
【猜想】放出的气体可能是SO2、O2、H2中的一种,提出猜想的依据是质量守恒定律.
【资料】S02易溶于水,化学性质与二氧化碳相似,能使澄清石灰水变浑浊,生成CaS03.
【方案】依据上述猜想,实验小组同学分别设计了如下方案.
①甲同学认为是O2,则检验方法是带火星的木条检验,看木条是否复燃.
②乙同学认为是S02,则只需将装置A、C相连,看澄清石灰水是否变浑浊即可.写出SO2与Ca(OH)2反应的化学方程式:SO2+Ca(OH)2=CaSO3↓+H2O.
③丙同学在乙同学实验装置的基础上增加了如图2所示的装置,观察到试管中产生的现象是铜网表面的黑色物质变红.
【结论】经过实验,得出结论:放出的气体为H2.
(4)在氢气还原氧化铜的实验中,向50g氧化铜粉末中通氢气,加热一段时间后,测得反应后生成水的质量为9g.求已反应掉的氧化铜的质量.
分析 (1)检验碳酸盐的具体方法是,先取少量的待检物于试管中,再向其中滴加少量的稀盐酸,振荡,若有气泡生成,将气体通入澄清的石灰水后,澄清的石灰水变浑浊;则证明该盐中含有CO32-,是一种碳酸盐,通入石灰水是用长导管,让气体与石灰水充分反应;
(2)氢气的密度比空气小,所以将D瓶口向下时,应从长导管进气;
(3)提出猜想:进行猜想要考虑到反应前后元素种类不变;根据氧气支持燃烧的性质解答;
(4)根据题中信息结合化学方程式的进行计算考虑.
解答 解:(1)小明要证明鸡蛋壳的主要成分是碳酸盐,应将A装置中的导气管a与C装置中的导气管d连接,让生成的气体与石灰水充分接触反应,若C中澄清的石灰水变浑浊,说明鸡蛋壳的主要成分是碳酸盐;碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,反应方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)氢气的密度比空气小,所以将D瓶口向下时,应从长导管进气;
(3)【猜想】铁粉投入硫酸铜溶液中,反应前含有S、O、H、Cu元素,依据质量守恒定律可以得出猜想;
【方案】①氧气具有助燃性,可以通过检验气体的助燃效果进行判断;
故答案为:用带火星的木条检验,看木条是否复燃;
②二氧化硫和氢氧化钙反应会生成亚硫酸钙和水,反应的化学方程式:SO2+Ca(OH)2=CaSO3↓+H2O;
③丙同学在乙同学实验装置的基础上增加了如图2所示的装置,观察到试管中产生的现象是铜网表面的黑色物质变红;
(4):(1)设参加反应的氧化铜的质量为x,消耗氢气质量为y,
H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O
80 18
x 9g
$\frac{80}{x}=\frac{18}{9g}$
x=40g
答案:
(1)CaCO3+2HCl═CaCl2+H2O+CO2↑;澄清的石灰水变浑浊;
(3)g;
(3)【猜想】质量守恒定律;
【方案】①带火星的木条检验,看木条是否复燃;
②SO2+Ca(OH)2=CaSO3↓+H2O;
③铜网表面的黑色物质变红;
(4)已反应掉的氧化铜的质量为40g.
点评 本题主要考查化学实验的方案设计与评价,在解此类题时,首先分析题中考查的问题,然后结合所给的知识和学过的知识进行分析解答.

 阅读快车系列答案
阅读快车系列答案| A. | 水在自然界不断循环,取之不尽,用之不竭 | |
| B. | 工厂排放的废水直接通入地下,避免污染地表水 | |
| C. | 公园浇花采用喷灌和滴灌 | |
| D. | 为了节约用水,将工厂排放的废水直接浇灌庄稼 |
| 实验次数 | 一 | 二 | 三 | 四 | 五 | 六 |
| 加入镁粉的质量/g | 1 | 2 | 3 | 4 | 5 | 6 |
| 生成硫酸镁的质量/g | 5 | 15 | 18 | 18 |
(2)上表中两个空格内的数据分别是10和18.
(3)第一次反应结束后,消耗硫酸质量(x)的比例式为$\frac{98}{x}=\frac{120}{5g}$.
(4)这种稀硫酸中溶质的质量分数为9.8%.
(5)若第四次反应完成后,把所得溶液蒸发掉3.3g水(此过程没有晶体析出),则最终所得溶液溶质的质量分数为3%.
(6)若用98%的浓硫酸配制上述实验中所需的稀硫酸,则需要加蒸馏水的质量为802g.
 如下表格是元素周期表的一部分,等质量的四种元素中所含原子个数由多到少的顺序是Si、P、S、Cl,硅与碳位于同一主族,同族元素性质相似,则二氧化硅与NaOH溶液反应的化学方程式为2NaOH+SiO2=Na2SiO3+H2O.
如下表格是元素周期表的一部分,等质量的四种元素中所含原子个数由多到少的顺序是Si、P、S、Cl,硅与碳位于同一主族,同族元素性质相似,则二氧化硅与NaOH溶液反应的化学方程式为2NaOH+SiO2=Na2SiO3+H2O.

