题目内容
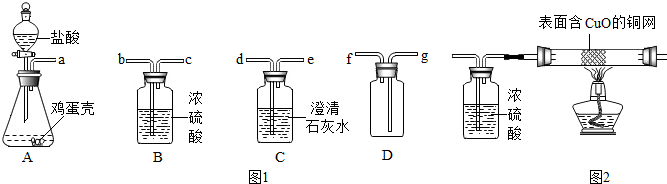
15.如图中A、B、C、D是四种粒子的结构示意图,请回答下列问题:
(1)微粒A中x=2;
(2)微粒B在化学反应中容易失(填“得”或“失”)电子;
(3)由C粒子的结构示意图可知,C粒子的名称是氧原子;
(4)以上四种结构示意图所表示的粒子中,表示离子的是AD(填字母代号).
分析 (1)根据核外电子排布规律,进行解答;
(2)根据最外层电子数<4时,在化学反应中易失去最外层电子来分析解答;
(3)根据核内质子数=核外电子数为原子进行解答;
(4)根据核内质子数≠核外电子数时,表示离子进行解答.
解答 解:(1)由核外电子排布规律可知,排满第一个电子层,才排第二个电子层,第一个电子层上最多排2个电子,故x=2;
(2)当最外层电子数<4时,在化学反应中易失去最外层电子,故微粒B在化学反应中容易失电子;
(3)由C粒子的结构示意图可知,核内质子数为8,故为氧元素,核外电子数为8,故该微粒为氧原子;
(4)当核内质子数≠核外电子数时,表示离子,故以上四种结构示意图表示离子的是AD;
故答案为:(1)2;(2)失;(3)氧原子;(4)AD;
点评 本题难度不大,考查学生对粒子结构示意图及其意义的理解,了解粒子结构示意图的意义等知识是正确解题的关键.

练习册系列答案
相关题目
3.现有一定量的NaHCO3固体,将其加热一段时间后得13.7g固体,将固体加水充分溶解,得无色透明溶液,再向其中加入100g7.3%稀盐酸,充分反应后,所得溶液恰好为中性,请计算在加热过程中分解了得NaHCO3得占原固体中NaHCO3得质量分数为(NaHCO3受热分解生成Na2CO3、H2O、CO2)( )
| A. | 50% | B. | 60% | C. | 70% | D. | 80% |
10.下列实验现象描述不正确的是( )
| A. | 点燃氢气,产生淡蓝色火焰 | |
| B. | 打开浓盐酸试剂瓶的瓶塞,瓶口上方出现白雾 | |
| C. | 向土豆片上滴几滴碘水,土豆片变蓝色 | |
| D. | 点燃一块棉纤维,产生烧焦羽毛的气味 |
20.在生产、生活中下列做法,你认为不合理的是( )
| A. | 胃酸过少的病人可服用食醋缓解 | |
| B. | 园林工人将含有硫磺粉的石灰浆涂刷在树上用于防止虫蛀 | |
| C. | 碳酸钡悬浊液用于医疗上作为检查胃病的钡餐 | |
| D. | 二氧化碳可用作气体肥料 |
5.KNO3和NaCl在不同温度时的溶解度如下表:
请回答下列问题:
(1)依据上表数据,绘制出KNO3和NaCl的溶解度曲线如图1,图中能表示KNO3溶解度曲线的是A(填“A”或“B”);
(2)由表中数据分析可知,KNO3和NaCl在某一温度时具有相同的溶解度,则温度的取值范围是20℃~30℃;
(3)某兴趣小组做了以下实验(如图2):
上述实验过程中得到的溶液一定属于不饱和溶液的是①③④(填数字序号).
将⑤继续冷却至10℃,过滤,共可回收得到KNO3固体59.1g,所得滤液中KNO3的溶质质量分数为17.3%.(计算结果保留小数点后1位,不考虑实验过程中水的蒸发)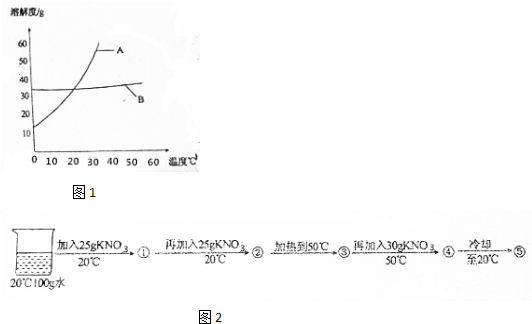
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | |
(1)依据上表数据,绘制出KNO3和NaCl的溶解度曲线如图1,图中能表示KNO3溶解度曲线的是A(填“A”或“B”);
(2)由表中数据分析可知,KNO3和NaCl在某一温度时具有相同的溶解度,则温度的取值范围是20℃~30℃;
(3)某兴趣小组做了以下实验(如图2):
上述实验过程中得到的溶液一定属于不饱和溶液的是①③④(填数字序号).
将⑤继续冷却至10℃,过滤,共可回收得到KNO3固体59.1g,所得滤液中KNO3的溶质质量分数为17.3%.(计算结果保留小数点后1位,不考虑实验过程中水的蒸发)