题目内容
6. 实验室有一瓶标签残缺并且瓶盖没有完全密封的无色溶液(如图),为确认其中的溶质,同学们进行了如下的探究活动.请你参与到其中去,回答有关问题.
实验室有一瓶标签残缺并且瓶盖没有完全密封的无色溶液(如图),为确认其中的溶质,同学们进行了如下的探究活动.请你参与到其中去,回答有关问题.【进行猜想】猜想Ⅰ:该溶液的溶质是NaCl;
猜想Ⅱ:该溶液的溶质是NaOH;
猜想Ⅲ:该溶液的溶质是Na2CO3;
猜想 IV:该溶液的溶质是NaHCO3.
【查阅资料】常温下物质的相关信息如表:
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
| 常温下稀溶液的pH | 7 | 13 | 11 | 9 |
8.8%(精确到01.%).
【进行实验】(1)测定溶液的pH大于7,该溶液的溶质不是NaCl(填化学式).
(2)同学们又进行了如下实验,实验过程如图:
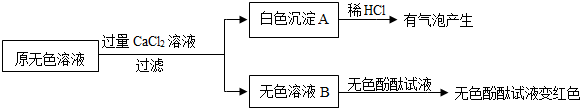
①产生白色沉淀的化学方程式是Na2CO3+CaCl2=CaCO3↓+2NaCl.
②实验可以判断原无色溶液中含有的溶质有NaOH、Na2CO3.
【获得结论】
该瓶原来装的无色溶液的溶质是NaOH,并且部分(填“没有”、“部分”或“全部”)变质.
【拓展】
提纯该无色溶液的步骤是:先向无色溶液中加入适量的Ca(OH)2,然后过滤.反应化学方程式是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
分析 【查阅资料】根据III中所给数据可以求出在20℃时各物质的饱和溶液的质量分数,可以做出判断;
【进行实验】(1)氯化钠溶液呈中性,pH等于7;
(2)根据碳酸钠可以和氯化钙反应生成碳酸钙沉淀和氯化钠解答;可以设计实验来验证碳酸钠的存在;
【获得结论】根据实验现象分析解答;
【拓展】根据Ca(OH)2可以和碳酸钠反应生成碳酸钙沉淀和氢氧化钠解答.
解答 解:
【查阅资料】根据计算可以知道在20℃时饱和碳酸氢钠的质量分数为:$\frac{9.6g}{9.6g+100g}$×100%=8.8%<10%,所以能够排除碳酸氢钠;
【进行实验】(
(1)测定溶液的pH大于7,该溶液的溶质不是,而氯化钠溶液呈中性,pH等于7所以不可能是氯化钠,故本题答案为:NaCl;
(2)①过量的氯化钙可以检验并除尽碳酸钠,碳酸钠可以和氯化钙反应生成碳酸钙沉淀和氯化钠,产生白色沉淀的化学方程式是Na2CO3+CaCl2=CaCO3↓+2NaCl;
②滴加无色酚酞,滤液变红,说明溶液呈碱性,还有氢氧化钠,实验可以判断原无色溶液中含有的溶质有NaOH、Na2CO3;
【获得结论】该瓶原来装的无色溶液的溶质是NaOH,并且部分变质;
【拓展】提纯该无色溶液的步骤是:先向无色溶液中加入适量的Ca(OH)2,然后过滤.反应化学方程式是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
答案:
【查阅资料】8.8%;
【进行实验】(1)NaCl;
(2)①Na2CO3+CaCl2=CaCO3↓+2NaCl; ②NaOH、Na2CO3;
【获得结论】部分;Ca(OH)2 Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
点评 本题综合利用了物质的组成、物质的溶解性、溶液的酸碱性及物质的变化规律对未知物质进行鉴别,还考查学生利用化学方程式和溶质质量分数公式进行计算的能力,难度不大,可依据相关物质的性质逐渐分析得出结论.

| A. | 1:1 | B. | 2:1 | C. | 4:1 | D. | 5:1 |
| A. | NO3- | B. | SO42- | C. | CO32- | D. | Cl- |
| 选项 | 物质(括号内为杂质) | 试剂 | 操作方法 |
| A | CO2气体(CO) | 过量的氧气 | 点燃 |
| B | Fe2O3(Fe) | 足量的盐酸 | 过滤 |
| C | FeSO4溶液(CuSO4) | 足量的锌 | 过滤 |
| D | O2(H2O) | 浓硫酸 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 在雾霾治理过程中,可注重空气中氨气的检测及控制氨气的排放 | |
| B. | PM2.5专用口罩中使用了活性炭,是利用了活性炭的吸附性 | |
| C. | 为有效控制雾霾,应禁止使用氮肥 | |
| D. | 该反应原理中所有元素化合价都不变 |
| A. | 只能是固体 | B. | 只能是液体 | ||
| C. | 只能是气体 | D. | 可能是气体、液体或固体 |