题目内容
11.某溶液中大量存在的离子仅有Ba2+、Ag+和X离子,则X离子可能是( )| A. | NO3- | B. | SO42- | C. | CO32- | D. | Cl- |
分析 根据复分解反应的条件,离子间若能互相结合成沉淀、气体或水,则离子不能共存,据此进行分析判断即可.
解答 解:A、NO3-和Ba2+、Ag+不能结合成沉淀、气体或水,能大量共存,故选项正确;
B、Ba2+、SO42-两种离子能结合成硫酸沉淀,不能大量共存,故选项错误;
C、Ba2+、Ag+和CO32-结合产生碳酸钡沉淀和碳酸银沉淀,不能大量共存,故选项错误;
D、Cl-和Ag+结合成氯化银沉淀,不能大量共存,故选项错误;
故选:A.
点评 本题考查了离子共存的问题,判断各离子在溶液中能否共存,主要看溶液中的各离子之间能否发生反应生成沉淀、气体、水.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
2.如表是当涂县江心中学化学兴趣小组的四位同学分别设计的实验方案,用于区分各组物质.
在设计的四组方案中,两种方案都正确的是( )
在设计的四组方案中,两种方案都正确的是( )
| 选项 | 需要鉴别的物质 | 方案一 | 方案二 |
| A | 碳酸钠溶液和氢氧化钠溶液 | 加食醋溶液 | 加硝酸钡溶液 |
| B | 水和过氧化氢溶液 | 观察颜色 | 加酚酞溶液 |
| C | 空气和人呼出的气体 | 用带火星木条 | 加石灰水 |
| D | 生石灰(CaO)与石灰石(主要成分CaCO3) | 加稀盐酸 | 高温煅烧 |
| A. | A | B. | B | C. | C | D. | D |
19.下列有关水的说法正确的是( )
| A. | 电解水时产生的气体的质量比是1:2 | |
| B. | 可用水区分CaO和CaCO3 | |
| C. | 硬水经过活性炭吸附变为纯净水 | |
| D. | 海洋有大量的水,所以不必节约用水 |
6.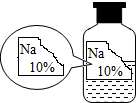 实验室有一瓶标签残缺并且瓶盖没有完全密封的无色溶液(如图),为确认其中的溶质,同学们进行了如下的探究活动.请你参与到其中去,回答有关问题.
实验室有一瓶标签残缺并且瓶盖没有完全密封的无色溶液(如图),为确认其中的溶质,同学们进行了如下的探究活动.请你参与到其中去,回答有关问题.
【进行猜想】猜想Ⅰ:该溶液的溶质是NaCl;
猜想Ⅱ:该溶液的溶质是NaOH;
猜想Ⅲ:该溶液的溶质是Na2CO3;
猜想 IV:该溶液的溶质是NaHCO3.
【查阅资料】常温下物质的相关信息如表:
从物质的相关信息可知,该溶液的溶质不是NaHCO3,因为常温下NaHCO3溶液溶质的质量分数最大是
8.8%(精确到01.%).
【进行实验】(1)测定溶液的pH大于7,该溶液的溶质不是NaCl(填化学式).
(2)同学们又进行了如下实验,实验过程如图:
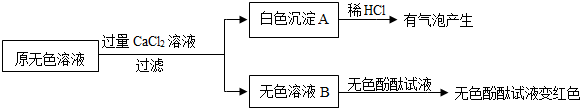
①产生白色沉淀的化学方程式是Na2CO3+CaCl2=CaCO3↓+2NaCl.
②实验可以判断原无色溶液中含有的溶质有NaOH、Na2CO3.
【获得结论】
该瓶原来装的无色溶液的溶质是NaOH,并且部分(填“没有”、“部分”或“全部”)变质.
【拓展】
提纯该无色溶液的步骤是:先向无色溶液中加入适量的Ca(OH)2,然后过滤.反应化学方程式是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
 实验室有一瓶标签残缺并且瓶盖没有完全密封的无色溶液(如图),为确认其中的溶质,同学们进行了如下的探究活动.请你参与到其中去,回答有关问题.
实验室有一瓶标签残缺并且瓶盖没有完全密封的无色溶液(如图),为确认其中的溶质,同学们进行了如下的探究活动.请你参与到其中去,回答有关问题.【进行猜想】猜想Ⅰ:该溶液的溶质是NaCl;
猜想Ⅱ:该溶液的溶质是NaOH;
猜想Ⅲ:该溶液的溶质是Na2CO3;
猜想 IV:该溶液的溶质是NaHCO3.
【查阅资料】常温下物质的相关信息如表:
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
| 常温下稀溶液的pH | 7 | 13 | 11 | 9 |
8.8%(精确到01.%).
【进行实验】(1)测定溶液的pH大于7,该溶液的溶质不是NaCl(填化学式).
(2)同学们又进行了如下实验,实验过程如图:

①产生白色沉淀的化学方程式是Na2CO3+CaCl2=CaCO3↓+2NaCl.
②实验可以判断原无色溶液中含有的溶质有NaOH、Na2CO3.
【获得结论】
该瓶原来装的无色溶液的溶质是NaOH,并且部分(填“没有”、“部分”或“全部”)变质.
【拓展】
提纯该无色溶液的步骤是:先向无色溶液中加入适量的Ca(OH)2,然后过滤.反应化学方程式是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
16. 牙膏是和牙刷一起用于清洁牙齿,保护口腔卫生,是对人体安全的一种日用必需品.某化学兴趣小组对某种牙膏的成分进行了如下探究:
牙膏是和牙刷一起用于清洁牙齿,保护口腔卫生,是对人体安全的一种日用必需品.某化学兴趣小组对某种牙膏的成分进行了如下探究:
探究一:牙膏的酸碱性
实验1:取少量牙膏放入烧杯中,加入足量的水溶解,静置,取上层清液,测定溶液的 pH,pH>7(填”>”或”<”),牙膏呈碱性.
探究二:牙膏摩擦剂的成分
小明同学发现实验1烧杯底部有沉淀,便想探究其成分.
【查阅资料】牙膏成分中的固体原料为磨擦剂,它是擦去牙齿表面牙垢,减轻牙渍的成分.常见的摩擦剂有碳酸钙、二氧化硅(SiO2)等.
【猜想与假设】该牙膏摩擦剂成分可能是:①为碳酸钙;②二氧化硅;③你的猜想是碳酸钙和二氧化硅混合物.
实验2:【设计方案和实验】
请你写出步骤①的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑.
 牙膏是和牙刷一起用于清洁牙齿,保护口腔卫生,是对人体安全的一种日用必需品.某化学兴趣小组对某种牙膏的成分进行了如下探究:
牙膏是和牙刷一起用于清洁牙齿,保护口腔卫生,是对人体安全的一种日用必需品.某化学兴趣小组对某种牙膏的成分进行了如下探究:探究一:牙膏的酸碱性
实验1:取少量牙膏放入烧杯中,加入足量的水溶解,静置,取上层清液,测定溶液的 pH,pH>7(填”>”或”<”),牙膏呈碱性.
探究二:牙膏摩擦剂的成分
小明同学发现实验1烧杯底部有沉淀,便想探究其成分.
【查阅资料】牙膏成分中的固体原料为磨擦剂,它是擦去牙齿表面牙垢,减轻牙渍的成分.常见的摩擦剂有碳酸钙、二氧化硅(SiO2)等.
【猜想与假设】该牙膏摩擦剂成分可能是:①为碳酸钙;②二氧化硅;③你的猜想是碳酸钙和二氧化硅混合物.
实验2:【设计方案和实验】
| 步骤 | 现象 | 结论 |
| ①取少量沉淀,加入适量稀盐酸 | 沉淀完全溶解,有气泡产生 | 假设①正确(填序号) |
| ②将产生的气体通入澄清的石灰水 | 澄清石灰水变浑浊 |
20.下列物质间的转化能一步实现的是( )
| A. | Cu→CuSO4 | B. | H2SO4→HCl | C. | KNO3→KCl | D. | Fe→Fe2(SO4)3 |
 A~F是初中化学常见的物质,已知C物质是一种常用的建筑材料,常用来砌砖和粉刷墙壁.六种物质之间的关系如右图所示,图中“→”表示物质间的转化关系,“-”表示两端物质能相互反应(部分反应物、生成物及反应条件未标出),E和F反应生成白色沉淀且沉淀不溶于稀硝酸.
A~F是初中化学常见的物质,已知C物质是一种常用的建筑材料,常用来砌砖和粉刷墙壁.六种物质之间的关系如右图所示,图中“→”表示物质间的转化关系,“-”表示两端物质能相互反应(部分反应物、生成物及反应条件未标出),E和F反应生成白色沉淀且沉淀不溶于稀硝酸.