题目内容
1.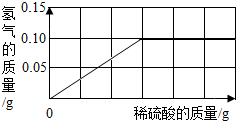 商店门牌上装潢的鎏金大字,金光灿烂,似金非金,不少是由黄铜质料做的.我国古代南北朝时期就能铸造黄铜.黄铜是铜和锌的合金,它可用来制造机器、电子零件及日常用品.为了测定黄铜(铜、锌合金)的组成,某研究性学习小组称取该样品10g,向其中逐滴加入稀硫酸至刚好不再产生气体为止,共用去稀硫酸50克.反应过程中生成的气体与所用硫酸溶液的质量关系如图所示.试计算:
商店门牌上装潢的鎏金大字,金光灿烂,似金非金,不少是由黄铜质料做的.我国古代南北朝时期就能铸造黄铜.黄铜是铜和锌的合金,它可用来制造机器、电子零件及日常用品.为了测定黄铜(铜、锌合金)的组成,某研究性学习小组称取该样品10g,向其中逐滴加入稀硫酸至刚好不再产生气体为止,共用去稀硫酸50克.反应过程中生成的气体与所用硫酸溶液的质量关系如图所示.试计算:(1)样品中铜的质量分数;
(2)稀硫酸溶液的溶质质量分数.
分析 锌和稀硫酸反应生成硫酸锌和氢气,根据氢气质量可以计算锌的质量和反应的硫酸质量,进一步可以计算样品中铜的质量分数和稀硫酸溶液的溶质质量分数.
解答 解:(1)设锌的质量为x,反应的硫酸质量为y,
Zn+H2SO4═ZnSO4+H2↑,
65 98 2
x y 0.10g
$\frac{65}{x}$=$\frac{98}{y}$=$\frac{2}{0.10g}$,
x=3.25g,y=4.9g,
样品中铜的质量分数为:$\frac{10g-3.25g}{10g}$×100%=67.5%,
答:样品中铜的质量分数为67.5%.
(2)稀硫酸溶液的溶质质量分数为:$\frac{4.9g}{50g}$×100%=9.8%,
答:稀硫酸溶液的溶质质量分数为9.8%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
17.下列物质中不属于复合材料的是( )
| A. | 钢筋混凝土 | B. | 玻璃钢 | C. | 铁锅 | D. | 轮胎 |
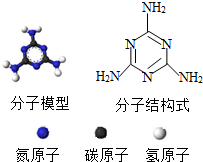 2008年9月份曝光的引起国人共愤的“结石宝宝”事件,与婴幼儿服用含有三聚氰胺的奶粉有关.已知三聚氰胺为白色晶体,将它用作食品添加剂可提高食品中蛋白质的检测值,俗称“蛋白精”.其分子模型与分子结构式如图所示,三聚氰胺的化学式为C3H6N6.
2008年9月份曝光的引起国人共愤的“结石宝宝”事件,与婴幼儿服用含有三聚氰胺的奶粉有关.已知三聚氰胺为白色晶体,将它用作食品添加剂可提高食品中蛋白质的检测值,俗称“蛋白精”.其分子模型与分子结构式如图所示,三聚氰胺的化学式为C3H6N6.