题目内容
14. 我们知道,每次做完实验后,剩余废液不能直接倾倒入排污管,必须回收处理.某班同学实验后收集到含有碳酸钠和氢氧化钠的混合废液5.11Kg,一个兴趣小组用废弃的溶质质量分数为19.6%的硫酸来处理,并回收处理后的溶液.他们向废液中加入稀硫酸时,所得溶液pH与加入的稀硫酸质量的关系曲线如图所示.求:
我们知道,每次做完实验后,剩余废液不能直接倾倒入排污管,必须回收处理.某班同学实验后收集到含有碳酸钠和氢氧化钠的混合废液5.11Kg,一个兴趣小组用废弃的溶质质量分数为19.6%的硫酸来处理,并回收处理后的溶液.他们向废液中加入稀硫酸时,所得溶液pH与加入的稀硫酸质量的关系曲线如图所示.求:(1)通过如图可知,当反应进行至图中B点时(填“A”、“B”或“C”),废液恰好处理完(即碳酸钠和氢氧化钠混合废液刚好完全转化成硫酸钠溶液).
(2)当向混合液中加入稀硫酸至N点时,加入的稀硫酸质量为5Kg,此时溶液总质量为10Kg,求此时生成的二氧化碳的质量为0.11Kg
(3)求所得溶液中溶质的质量分数(写出计算过程,溶于水的气体忽略不计)
分析 (1)根据图象分析在B时,溶液的PH等于7,溶液呈中性,废液恰好处理完;
(2)根据质量守恒定律分析;
(3)根据碳酸钠和氢氧化钠与硫酸反应的方程式,找出硫酸与硫酸钠的关系式,由硫酸的质量可求出硫酸钠的质量,在根据溶液中溶质的质量分数计算.
解答 解:(1)由于生成的硫酸钠溶液显中性,由图示可知,当反应进行至图中B点时,pH=7,然后又下降,说明此时恰好将废液处理完;
(2)生成的二氧化碳的质量为5.11kg+5kg-10kg=0.11kg;
(3)设生成的硫酸钠的质量为x
由H2SO4+2NaOH═Na2SO4+2H2O、Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
得:H2SO4~Na2SO4
98 142
5kg×19.6% x
$\frac{98}{5kg×19.6%}=\frac{142}{x}$
解得:x=1.42kg
所得溶液中溶质的质量分数是:$\frac{1.42kg}{10kg}×100%$=14.2%.
答:(1)B;(2)0.11;(3)所得溶液中溶质的质量分数是14.2%.
点评 在解此类题时,首先分析反应应用的原理,然后结合图象中的转折点,以及方程式中的比例关系进行解答.

练习册系列答案
相关题目
4.下列实验操作正确的是( )
| A. |  CO2验满 | B. | 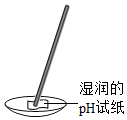 测溶液酸碱度 | C. | 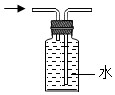 收集O2 | D. | 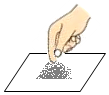 取用固体药品 |
5.下列四个实验方案设计不合理的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 鉴别氯化铵和尿素 | 分别加入熟石灰粉末研磨,闻气味 |
| B | 鉴别硝酸铵和氯化钠 | 分别加适量水,用手触摸容器壁 |
| C | 鉴别硫酸铜溶液和稀盐酸 | 分别观察溶液颜色 |
| D | 鉴别烧碱溶液和石灰水 | 分别滴加酚酞试液,观察颜色变化 |
| A. | A | B. | B | C. | C | D. | D |
6. 如图是镨元素在元素周期表中的部分信息,下列说法正确的是( )
如图是镨元素在元素周期表中的部分信息,下列说法正确的是( )
 如图是镨元素在元素周期表中的部分信息,下列说法正确的是( )
如图是镨元素在元素周期表中的部分信息,下列说法正确的是( )| A. | 镨元素的元素符号为Pr | B. | 镨的相对原子质量为140.9g | ||
| C. | 镨原子的核内中子数为59 | D. | 镨元素是非金属元素 |
3.下列化学符号中的数字“2”表示的意义不正确的是( )
| A. | 2Na:“2”表示两个钠元素 | |
| B. | NO2:“2”表示一个二氧化氮分子含有两个氧原子 | |
| C. | 2OH-:“2”表示两个氢氧根离子 | |
| D. | $\stackrel{+2}{Mg}$O:“+2”表示镁元素的化合价为+2价 |
4.下列各组溶液,不外加试剂就能鉴别出来的是( )
| A. | Na2CO3、HCl、BaCl2、NaCl | B. | NaOH、FeCl3、HCl、HNO3 | ||
| C. | Na2CO3、NaCl、Na2SO4、Ba(OH)2 | D. | NaOH、Ba(NO3)2、NaCl、MgSO4 |
