题目内容
9.某同学用过氧化氢溶液和二氧化锰制取氧气,该同学将50g过氧化氢溶液和1g 二氧化锰混合,完全反应后,称量剩余的混合物质量为49.4g.请列式计算该同学所用过氧化氢溶液的溶质质量分数是多少?分析 过氧化氢在二氧化锰催化下分解生成水和氧气,由于气体放出而使反应后剩余物质的质量减小,利用质量守恒定律,反应前后物质总质量的差即为放出氧气的质量;根据分解反应的化学方程式,由放出氧气的质量计算出分解的过氧化氢的质量,然后求出过氧化氢溶液的溶质质量分数即可.
解答 解:根据质量守恒定律,反应产生氧气的质量=50g+1g-49.4g=1.6g
设产生1.6g氧气需要H2O2的质量为x
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
x 1.6g
$\frac{68}{x}=\frac{32}{1.6g}$
x=3.4g
所用过氧化氢溶液的溶质质量分数=$\frac{3.4g}{50g}$×100%=6.8%
答:所用过氧化氢溶液的溶质质量分数是6.8%.
点评 解答本题时需要首先使用质量守恒定律,找出题中隐含条件,然后再由化学方程式及溶液的溶质质量分数进行计算,有较强的综合性,需要有清晰的解题思路.

练习册系列答案
相关题目
20.化学用语是学习化学的重要工具.下列化学用语表示正确的是( )
| A. | 两个氯原子:Cl2 | B. | 氧化铝:AlO | C. | 钙离子:Ca+2 | D. | 钾元素:K |
17.向盛有10g某Cu-Al合金样品的烧杯中加入100g稀硫酸,恰好完全反应,反应结束后,测得烧杯内物质的总质量为109.4g.则该合金样品中铜的质量分数是( )
| A. | 73% | B. | 54% | C. | 46% | D. | 27% |
19.世界是物质的,物质是变化的.以下不属于化学变化的是( )
| A. | 燃放鞭炮 | B. | 矿石粉碎 | C. | 植物光合作用 | D. | 酒精燃烧 |
 如图是初中化学中常见的物质:铁、一氧化碳、二氧化碳、氧化铜、四氧化三铁、硫酸.图中“→”表示转换关系,“--”表示相互能反应.其中E、F组成元素相同.
如图是初中化学中常见的物质:铁、一氧化碳、二氧化碳、氧化铜、四氧化三铁、硫酸.图中“→”表示转换关系,“--”表示相互能反应.其中E、F组成元素相同. 我们知道,每次做完实验后,剩余废液不能直接倾倒入排污管,必须回收处理.某班同学实验后收集到含有碳酸钠和氢氧化钠的混合废液5.11Kg,一个兴趣小组用废弃的溶质质量分数为19.6%的硫酸来处理,并回收处理后的溶液.他们向废液中加入稀硫酸时,所得溶液pH与加入的稀硫酸质量的关系曲线如图所示.求:
我们知道,每次做完实验后,剩余废液不能直接倾倒入排污管,必须回收处理.某班同学实验后收集到含有碳酸钠和氢氧化钠的混合废液5.11Kg,一个兴趣小组用废弃的溶质质量分数为19.6%的硫酸来处理,并回收处理后的溶液.他们向废液中加入稀硫酸时,所得溶液pH与加入的稀硫酸质量的关系曲线如图所示.求: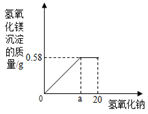 某粗盐样品仅含NaCl和MgCl2,为探究粗盐中NaCl的质量分数,某研究性小组取了10g样品,加适量水使其完全溶解后,加入20g5%的氢氧化钠溶液,测得相关数据如图.
某粗盐样品仅含NaCl和MgCl2,为探究粗盐中NaCl的质量分数,某研究性小组取了10g样品,加适量水使其完全溶解后,加入20g5%的氢氧化钠溶液,测得相关数据如图.