题目内容
17.溶液的碱性强弱与溶液中OH-数量有关.一定体积的溶液中OH-数量越多,则溶液的碱性越强.取10%的NaOH溶液(密度为1.1g/cm3)与10%的KOH(溶液密度也为1.1g/cm3)各30克相比较,碱性更强的是( )| A. | NaOH | B. | KOH | C. | 一样强 | D. | 无法比较 |
分析 计算等体积的10%的NaOH溶液与10%的KOH溶液中OH-数量,根据一定体积的溶液中OH-数量越多溶液碱性越强,判断10%的NaOH溶液与10%的KOH溶液碱性的强弱关系.
解答 解:假设两种溶液的体积都为vmL,
vmL10%的NaOH溶液中所含OH-数量=(vmL×1.1g/cm3×10%)×$\frac{17}{40}$×100%=0.04675v
vmL10%的KOH溶液中所含OH-数量=(vmL×1.1g/cm3×10%)×$\frac{17}{57}$×100%=0.03282v
0.04675>0.03282,所以,10%的NaOH溶液的碱性比10%的KOH溶液的碱性强;
故选:A.
点评 利用化合物中组成元素的质量分数=$\frac{相对原子质量×分子中原子个数}{相对分子质量}$×100%,把NaOH、KOH中的氢氧根看成一个整体(或一种元素),可计算其中氢氧根离子的质量分数.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.下列各组物质的溶液混合后,如果酸过量,最后仍有沉淀生成的是( )
| A. | NaOH,Mg(OH)2,HCl | B. | BaCl2,AgNO3,HNO3 | ||
| C. | CaCl2,K2CO3,HCl | D. | CuSO4,NaOH,H2SO4 |
2.锂元素(元素符号为Li)及其所形成的化合物,在通讯和航空航天领域中具有极其重要的用途.它的化合物氢氧化锂(LiOH)是一种易溶于水的白色固体,有辣味,具有强碱性和腐蚀性.
(1)氢氧化锂属于碱(填“酸”、“碱”、“盐”或金属氧化物).
(2)写出氢氧化锂与硫酸(H2SO4)反应的化学方程式2LiOH+H2SO4═Li2SO4+2H2O;
(3)上表是部分物质的溶解性表,运用此溶解性表并结合你对复分解反应发生条件的理解,从表中选出一种盐,该盐能和LiOH发生复分解反应,请你写出该反应的化学方程式:2LiOH+CuSO4═Li2SO4+Cu(OH)2↓.
(1)氢氧化锂属于碱(填“酸”、“碱”、“盐”或金属氧化物).
(2)写出氢氧化锂与硫酸(H2SO4)反应的化学方程式2LiOH+H2SO4═Li2SO4+2H2O;
| OH- | CO32- | SO42- | NO3- | |
| Ba2+ | 溶 | 不 | 不 | 溶 |
| Cu2+ | 不 | 不 | 溶 | 溶 |
| Li+ | 溶 | 微溶 | 溶 | 溶 |
9.下列各组物质中,俗名、化学名称和化学式表示的不是同一种物质的是( )
| A. | 熟石灰、氢氧化钙、Ca(OH)2 | B. | 烧碱、碳酸钠、Na2CO3 | ||
| C. | 盐酸、氯化氢水溶液、HCl | D. | 食盐、氯化钠、NaCl |
6.下列转化能由一步反应实现的是( )
| A. | FeO→Fe(OH)2 | B. | CuO→Cu(OH)2 | C. | CaCO3→Ca(OH)2 | D. | BaCl2→Ba(NO3)2 |
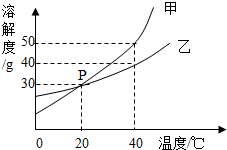 甲、乙两种固体物质的溶解度曲线如图所示.
甲、乙两种固体物质的溶解度曲线如图所示.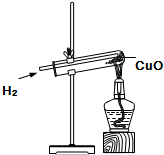 如图所示是氢气和氧化铜反应的实验装置图.请分析回答:
如图所示是氢气和氧化铜反应的实验装置图.请分析回答: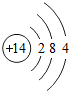 .(举一例)
.(举一例)