题目内容
7.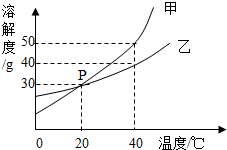 甲、乙两种固体物质的溶解度曲线如图所示.
甲、乙两种固体物质的溶解度曲线如图所示.(1)图中P点的含义是20℃甲乙物质的溶解度相同.
(2)40℃时,饱和溶液中溶质的质量分数:甲>乙(填“>”、“=”或“<”).20℃时,将50g乙物质放入100g水中,升温至40℃,溶液中溶质和溶剂的质量比为2:5(用最简整数比表示).
分析 (1)根据溶解度曲线可知,图中P点的含义是20℃甲乙物质的溶解度相同进行解答;
(2)根据40℃时甲物质的溶解度大于乙物质的溶解度以及40℃乙物质的溶解度为40g进行解答.
解答 解:(1)根据溶解度曲线可知,图中P点的含义是20℃甲乙物质的溶解度相同;故填:20℃甲乙物质的溶解度相同;
(2)40℃时甲物质的溶解度大于乙物质的溶解度,所以40℃时,饱和溶液中溶质的质量分数:甲大于乙;40℃乙物质的溶解度为40g,即在40℃100g水中最多溶解40g乙物质,所以20℃时,将50g乙物质放入100g水中,升温至40℃,溶液中溶质和溶剂的质量比为=40g:100g=2:5.故填:>;2:5.
点评 本题难度不是很大,主要考查了固体溶解度曲线的作用,根据溶解度曲线可以解决什么问题,从而加深学生对固体溶解度概念的理解,培养学生灵活的运用有关溶解度的知识的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
15.常见金属活动性顺序如图.下列各组物质间能发生反应的是( )
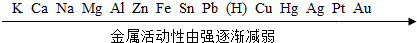
| A. | 铜和硝酸钠溶液 | B. | 铝和硫酸铜溶液 | C. | 锌和氯化钾溶液 | D. | 银和稀硫酸 |
2.现有生活中常见的四种未知白色粉末,它们分别是食盐、纯碱、去污粉(主要成分为碳酸钠和碳酸钙)和使用过的生石灰干燥剂.化学小组为了确定每种未知固体的成分,将它们分别标记为①、②、③、④后进行实验,实验现象记录如下:
根据以上实验现象,回答下列问题:
(1)实验1中,物质①发生反应的化学方程式是CaO+H2O═Ca(OH)2.
(2)物质②为食盐,试剂A为稀盐酸(合理即可).
(3)实验3中,试剂A与物质④发生反应的化学方程式是Na2CO3+2HCl=2NaCl+H2O+CO2↑、CaCO3+2HCl=CaCl2+H2O+CO2↑.
| 实验过程 | 实验现象 |
| 实验1:分别取样于四支试管中,加入足量的水充分溶解 | ②、③完全溶解,①、④均在试管底部有白色固体,且①中有明显放热 |
| 实验2:静置一段时间后,分别取上层清液,加入试剂A | ③、④均有气泡产生 |
| 实验3:分别取样于四支试管中,加入足量试剂A | 白色固体均消失;①③④均有气泡产生 |
(1)实验1中,物质①发生反应的化学方程式是CaO+H2O═Ca(OH)2.
(2)物质②为食盐,试剂A为稀盐酸(合理即可).
(3)实验3中,试剂A与物质④发生反应的化学方程式是Na2CO3+2HCl=2NaCl+H2O+CO2↑、CaCO3+2HCl=CaCl2+H2O+CO2↑.
19.下列那些物质能造成酸雨( )
| A. | CO和CO2 | B. | SO2和CO | C. | SO2和NO2 | D. | SO3和H2 |
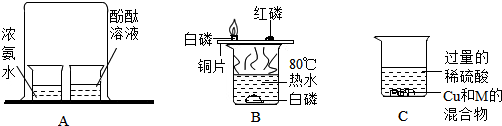
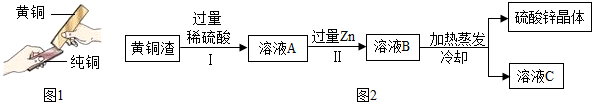
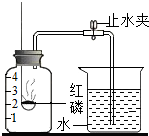 某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:
某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下: