题目内容
7.a粒子是+1价的阳离子,其核外电子排布与氖原子相同,b粒子最外层电子数是次外层的2倍,c是地壳中含量最多的元素,d原子不含中子,R在RO2中占50%.(1)a粒子的元素符号为Na+.
(2)与b化学性质相似的粒子结构图为
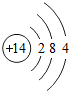 .(举一例)
.(举一例)(3)a、b、c、d组成化合物的化学式NaHCO3,举一例对应用途为制作糕点.
(4)a、c、d组成化合物,与RO2反应的化学方程式2NaOH+SO2=Na2SO3+H2O.
分析 根据a粒子是+1价的阳离子,其核外电子排布与氖原子相同,氖原子核外有10个电子,所以a是钠离子,b粒子最外层电子数是次外层的2倍,次外层只能是2个电子,所以b是碳原子,c是地壳中含量最多的元素,所以c是氧元素,d原子不含中子,所以d是氢原子,R在RO2中占50%,所以R是硫元素,然后将推出的元素进行验证即可.
解答 解:a粒子是+1价的阳离子,其核外电子排布与氖原子相同,氖原子核外有10个电子,所以a是钠离子,b粒子最外层电子数是次外层的2倍,次外层只能是2个电子,所以b是碳原子,c是地壳中含量最多的元素,所以c是氧元素,d原子不含中子,所以d是氢原子,R在RO2中占50%,所以R是硫元素,经过验证,推导正确,所以
(1)a粒子是钠离子,元素符号为:Na+;
(2)b是碳原子,最外层电子数相同,具有相同的化学性质,所以硅的化学性质与碳相似,表示为: ;
;
(3)钠元素、碳元素、氧元素、氢元素组成的化合物是碳酸氢钠,化学式为:NaHCO3,可以用来制作糕点;
(4)钠元素、氧元素、氢元素组成的化合物是氢氧化钠,氢氧化钠和二氧化硫反应生成亚硫酸钠和水,化学方程式为:2NaOH+SO2=Na2SO3+H2O.
故答案为:(1)Na+;
(2) ;
;
(3)NaHCO3,制作糕点;
(4)2NaOH+SO2=Na2SO3+H2O.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
相关题目
17.溶液的碱性强弱与溶液中OH-数量有关.一定体积的溶液中OH-数量越多,则溶液的碱性越强.取10%的NaOH溶液(密度为1.1g/cm3)与10%的KOH(溶液密度也为1.1g/cm3)各30克相比较,碱性更强的是( )
| A. | NaOH | B. | KOH | C. | 一样强 | D. | 无法比较 |
18.下列化学方程式正确的是( )
| A. | Mg+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$ MgSO4+H2 | |
| B. | 2KMnO4 $\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | |
| C. | 4P+5O2$\frac{\underline{\;点燃\;}}{\;}$ 2P2O5 | |
| D. | 2NaNO3+K2CO3$\frac{\underline{\;\;△\;\;}}{\;}$ 2KNO3+Na2CO3 |
12.恩施州盛产富硒茶,除了硒含量高以外,茶叶中含有茶氨酸(化学式为C7H14O3N2,又称谷氨酰乙胺)具有降低血压、提高记忆力、减肥等功效.下列有关茶氨酸的说法正确的是( )
| A. | 茶氨酸由C、H、O、N四种元素组成 | B. | 茶氨酸分子中氧的质量分数为12% | ||
| C. | 茶氨酸的相对分子质量为184 | D. | 茶氨酸中含有1个氮分子 |
19.下列有关水的说法正确的是( )
| A. | 用肥皂水可以检验硬水和软水 | |
| B. | 电解水生成氢气和氧气,说明水是由氢气和氧气组成的 | |
| C. | 尽可能多地开发利用地下水 | |
| D. | 过滤可以除去水中的可溶性杂质 |