题目内容
7.石灰岩因其坚硬致密,可用作建筑石材,还可用于生产水泥和生石灰.(1)高温煅烧石灰石可得到生石灰和二氧化碳,生石灰可用作干燥剂的原因是生石灰能与水发生反应.在炼铁高炉中,二氧化碳与碳在高温下反应得到一氧化碳,在此反应中作为还原剂的是碳(C).
(2)石灰石与稀盐酸反应制取二氧化碳,写出反应的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑.
分析 (1)根据生石灰具有吸水性解答;根据在炼铁高炉中,二氧化碳与碳在高温下反应得到一氧化碳,在此反应中作为还原剂的是碳解答;
(2)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可.
解答 解:
(1)生石灰可用作干燥剂的原因是生石灰能与水发生反应;在炼铁高炉中,二氧化碳与碳在高温下反应得到一氧化碳,在此反应中作为还原剂的是碳;
(2)石灰石与稀盐酸反应制取二氧化碳,同时生成氯化钙、水,反应的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑.
答案:
(1)生石灰能与水发生反应; 碳(C);
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
相关题目
17.市售加碘盐是在食益中加入一定量的碘酸钾(KIO3),KIO3中碘元素的化合价是( )
| A. | +5 | B. | -1 | C. | +3 | D. | +1 |
15. 某化学实验室产生的废液中含有FeCl3、CuCl2、BaCl2三种物质,现设计下列方案对废液进行处理,以回收金属并制备氯化钡、氯化铁晶体下列说法不正确的是( )
某化学实验室产生的废液中含有FeCl3、CuCl2、BaCl2三种物质,现设计下列方案对废液进行处理,以回收金属并制备氯化钡、氯化铁晶体下列说法不正确的是( )
 某化学实验室产生的废液中含有FeCl3、CuCl2、BaCl2三种物质,现设计下列方案对废液进行处理,以回收金属并制备氯化钡、氯化铁晶体下列说法不正确的是( )
某化学实验室产生的废液中含有FeCl3、CuCl2、BaCl2三种物质,现设计下列方案对废液进行处理,以回收金属并制备氯化钡、氯化铁晶体下列说法不正确的是( )| A. | 沉淀1中的单质为铁和铜 | |
| B. | 氧化方程式为2FeCl2+H2O2+2HCl═2FeCl3+2 H2O | |
| C. | “过滤3”到“氧化”是为了充分回收铁元素 | |
| D. | 试剂X应为NaOH |
2.在CuO和Fe的混合物中加入一定量的稀硫酸,微热,待反应停止后过滤,滤出不溶物后再往滤液中加入一根铁钉,若铁钉无变化,则下列叙述不正确的是( )
| A. | 不溶物中一定有铜 | B. | 不溶物可能全部是铁 | ||
| C. | 滤液是硫酸亚铁溶液 | D. | 滤液中含有硫酸铜和硫酸亚铁 |
16.在研究性学习中同学们了解到氢气具有还原性.他们用氢气还原氧化铜的方法测定某氧化铜样品的纯度(杂质不与氢气反应),同学们设计了以下实验装置,准确称取15克干燥样品进行实验.

(1)在实验中,乙装置的作用是检验水是否除尽;
(2)准确称取完全反应前后装置丙和丁的质量如表:
甲同学想根据装置丁的质量变化进行计算,请帮甲同学求出氧化铜样品的纯度(写出计算过程).
乙同学根据装置丙减少的质量就是氧元素质量,求得氧化铜的质量为11.5克,纯度为76.7%.
(3)比较两种计算结果,请分析导致这一结果的原因可能是
A.装置的气密性不好 B.空气中的水分被丁处浓硫酸吸收
C.通入的氢气量不足 D.空气中的二氧化碳被丁处浓硫酸吸收.
在针对这一结果,对实验装置提出你的一条改进建议在丁的后面增加一个盛有碱石灰的干燥管.

(1)在实验中,乙装置的作用是检验水是否除尽;
(2)准确称取完全反应前后装置丙和丁的质量如表:
| 装置丙 | 装置丁 | |
| 反应前 | 48.8克 | 161.2克 |
| 反应后 | 46.5克 | 163.9克 |
乙同学根据装置丙减少的质量就是氧元素质量,求得氧化铜的质量为11.5克,纯度为76.7%.
(3)比较两种计算结果,请分析导致这一结果的原因可能是
A.装置的气密性不好 B.空气中的水分被丁处浓硫酸吸收
C.通入的氢气量不足 D.空气中的二氧化碳被丁处浓硫酸吸收.
在针对这一结果,对实验装置提出你的一条改进建议在丁的后面增加一个盛有碱石灰的干燥管.
17.下列涉及学科观点的有关说法正确的是( )
| A. | 微粒观: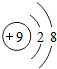 和 和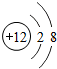 两个粒子核外电子数相同,属于同种元素 两个粒子核外电子数相同,属于同种元素 | |
| B. | 转化观:任何不饱和溶液降低温度后,一定会转化为饱和溶液 | |
| C. | 能量观:硝酸铵固体溶于水放出热量,天然气燃烧吸收热量 | |
| D. | 结构观:金刚石和石墨物理性质存在较大差异是由于碳原子排列方式不同 |
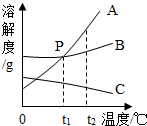 如图是A、B、C三种固体物质的溶解度曲线,请回答:
如图是A、B、C三种固体物质的溶解度曲线,请回答: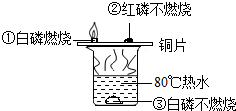 为探究物质的燃烧条件,某同学进行了如图所示的实验,下列有关说法正确的是( )
为探究物质的燃烧条件,某同学进行了如图所示的实验,下列有关说法正确的是( )