题目内容
12.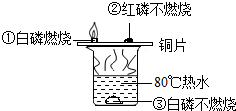 为探究物质的燃烧条件,某同学进行了如图所示的实验,下列有关说法正确的是( )
为探究物质的燃烧条件,某同学进行了如图所示的实验,下列有关说法正确的是( )A.现象①③说明白磷的着火点比红磷的着火点低
B.现象①②说明物质的燃烧需要达到一定程度
C.现象②说明物质必须是可燃物
D.现象①③说明物质燃烧需要氧气.
分析 A.现象①③不同是因为与氧气(或空气)的接触不同;
B.现象②是因为没有达到着火点,现象①是因为满足燃烧的条件;
C.红磷是可燃物;
D.结合燃烧的条件来分析.
解答 解:A.现象①③不同是因为铜片上的白磷满足了物质燃烧的三个条件;水中的白磷不能燃烧是因为不与氧气接触,故错误;
B.温水是80℃,铜片上的白磷燃烧,说明它的燃烧所需温度不高于80℃,而红磷不能燃烧则说明红磷的着火点高于80℃,说明白磷的着火点比红磷的着火点低,故正确;
C.红磷具有可燃性,属于可燃物,故错误;
D.现象①③说明了白磷的温度达到了其着火点,没有与氧气接触,所以不能发生燃烧.
故答案为:B;物质燃烧需要氧气.
点评 本题主要检测学生对“燃烧需要同时满足三个条件”这一知识点的掌握情况.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
2.工业上用电解饱和食盐水的方法生产烧醎、氢气、氯气等化工产品,其反应原理为:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑,某研究性小组对制得的烧碱样品进行了如下探究:
【提出问题】烧碱样品中可能含有哪些杂质?
【猜想】
猜想一:可能含有碳酸钠.猜想的依据是2NaOH+CO2=Na2CO3+H2O(用化学方程式表示)
猜想二:可能含有氯化钠.猜想的依据是化工生产中,原料往往不能完全转化为产品.
【实验探究】请帮甲同学完成以下探究实验:
乙同学为了验证猜想一的实验结论,也向烧碱样品的溶液中滴加了少量稀硝酸,却发现无气泡产生.
【解释与结论】大家经过分析,发现乙同学所用试剂与中同学相同,却没有看到气泡原因可能是少量的稀硝酸先与样品中的氢氧化钠反应完
【交流与反思】丙同学提出:“在甲同学做的实验中,稀硝酸也可以用稀盐酸代替.”你认为他的观点不正确(填“正确”或“不正确”)
【提出问题】烧碱样品中可能含有哪些杂质?
【猜想】
猜想一:可能含有碳酸钠.猜想的依据是2NaOH+CO2=Na2CO3+H2O(用化学方程式表示)
猜想二:可能含有氯化钠.猜想的依据是化工生产中,原料往往不能完全转化为产品.
【实验探究】请帮甲同学完成以下探究实验:
| 猜想 | 实验步骤 | 实验现象 | 实验结论 |
| 猜想一 | ①取少量烧碱样品于试管中,加水溶解向其中滴加过量稀硝酸 | 有气泡产生 | 样品中含有 Na2CO3 |
| ②将步骤①中产生的气体通入澄淸的石灰水中 | 澄清石灰水变浑浊 | ||
| 猜想二 | ③向步骤①所得的溶液中滴加几滴AgNO2溶液 | 产生白色沉淀 | 样品中含有氯化钠 |
【解释与结论】大家经过分析,发现乙同学所用试剂与中同学相同,却没有看到气泡原因可能是少量的稀硝酸先与样品中的氢氧化钠反应完
【交流与反思】丙同学提出:“在甲同学做的实验中,稀硝酸也可以用稀盐酸代替.”你认为他的观点不正确(填“正确”或“不正确”)
20.下列排列顺序正确的是( )
| A. | 硫元素的化合价: | B. | 利用金属的年代: | ||
| C. | 溶液的pH: | D. | 铜元素的质量分数: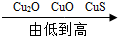 |
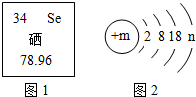
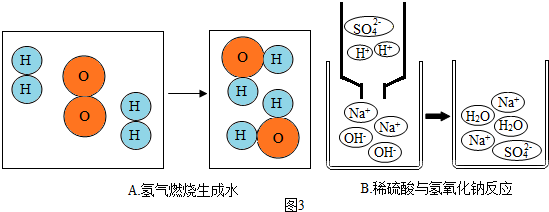

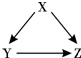 X、Y、Z为初中化学常见的物质,它们之间存在如图所示的转化关系(在一定条件下均能一步实现).
X、Y、Z为初中化学常见的物质,它们之间存在如图所示的转化关系(在一定条件下均能一步实现).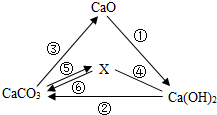 有关物质之间的部分转化关系如图所示.其中“-”表示物质之间能发生化学反应,“→”表示物质之间的转化关系.请回答相关问题:
有关物质之间的部分转化关系如图所示.其中“-”表示物质之间能发生化学反应,“→”表示物质之间的转化关系.请回答相关问题: