题目内容
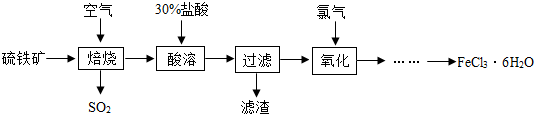
自来水厂常用氯气消毒杀菌,用明矾、氯化铁等絮凝剂净化水.以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3?6H2O)的工艺流程如下:
回答下列问题
(1)已知焙烧阶段就是硫铁矿燃烧,生成物是氧化铁和二氧化硫,试写出该反应化学方程式 ;硫铁矿进行燃烧之前要将其粉碎,其目的是 、 .
(2)流程中需用30%的盐酸“酸溶”焙烧后的残渣.试写出其主要化学方程式 .“酸溶”时可改用硫酸吗? (填写“行”或“不行”),原因是 .
(3)实际上焙烧阶段很难做到将硫铁矿完全反应,因此酸溶后的混合物中有FeCl2,试写出其在氧化阶段与氯气(Cl2)反应的化学方程式 .
(4)二氧化硫能形成酸雨,危害环境.常用下列方法除去:
方法1:用氨水中吸收二氧化硫.氨水的pH 7(填写“>”“=”或“<”).已知氨水与二氧化硫反应可生成A:(NH4)SO3、B:NH4HSO3,则氨水充分吸收二氧化硫所得的产物为 (填写“A”或“B”)
方法2:用石灰石悬浊液中,在空气作用下生成硫酸钙和二氧化碳,从而除去二氧化硫,写出反应的化学方程式 .

回答下列问题
(1)已知焙烧阶段就是硫铁矿燃烧,生成物是氧化铁和二氧化硫,试写出该反应化学方程式
(2)流程中需用30%的盐酸“酸溶”焙烧后的残渣.试写出其主要化学方程式
(3)实际上焙烧阶段很难做到将硫铁矿完全反应,因此酸溶后的混合物中有FeCl2,试写出其在氧化阶段与氯气(Cl2)反应的化学方程式
(4)二氧化硫能形成酸雨,危害环境.常用下列方法除去:
方法1:用氨水中吸收二氧化硫.氨水的pH
方法2:用石灰石悬浊液中,在空气作用下生成硫酸钙和二氧化碳,从而除去二氧化硫,写出反应的化学方程式
考点:物质的相互转化和制备,酸的化学性质,溶液的酸碱性与pH值的关系,书写化学方程式、文字表达式、电离方程式
专题:物质的制备
分析:(1)根据题中的叙述找出反应物、生成物以及反应条件,然后依据质量守恒定律书写化学方程式;
根据增大反应物的接触面积可以加快反应速率进行分析;
(2)根据氧化铁与盐酸的反应写出反应的化学方程式,根据硫酸和氧化铁反应会生成硫酸铁进行分析;
(3)根据题中的反应原理找出反应物、生成物以及反应条件,然后依据质量守恒定律书写化学方程式;
(4)方法1:根据氨水是一种常见的碱分析,根据足量的二氧化硫,与氨水生成亚硫酸铵,不足量的二氧化硫,与氨水反应生成亚硫酸氢氨;
方法2:根据二氧化硫与氢氧化钙、氧气反应生成了硫酸钙和二氧化碳,写出反应的化学方程式.
根据增大反应物的接触面积可以加快反应速率进行分析;
(2)根据氧化铁与盐酸的反应写出反应的化学方程式,根据硫酸和氧化铁反应会生成硫酸铁进行分析;
(3)根据题中的反应原理找出反应物、生成物以及反应条件,然后依据质量守恒定律书写化学方程式;
(4)方法1:根据氨水是一种常见的碱分析,根据足量的二氧化硫,与氨水生成亚硫酸铵,不足量的二氧化硫,与氨水反应生成亚硫酸氢氨;
方法2:根据二氧化硫与氢氧化钙、氧气反应生成了硫酸钙和二氧化碳,写出反应的化学方程式.
解答:解:(1)硫铁矿和氧气在点燃的条件下生成氧化铁和二氧化硫,化学方程式为:4FeS2+11O2
2Fe2O3+8SO2,增大反应物的接触面积可以加快反应速率,所以硫铁矿进行燃烧之前要将其粉碎,增大了反应物的接触面积,其目的是:快速燃烧、充足燃烧;
(2)流程中需用30%的盐酸“酸溶”焙烧后的残渣,盐酸和氧化铁反应生成氯化铁和水,化学方程式为:2Fe2O3+6HCl═2FeCl3+3H2O,酸溶”时可改用硫酸,硫酸和氧化铁反应生成硫酸铁和水,而题中需要制备氯化铁晶体,所以不能改用硫酸,原因是:主产物不再是氯化铁;
(3)通过分析题中的反应原理,酸溶后的混合物中通入氯气制取氯化铁,氯气和氯化亚铁反应生成氯化铁,化学方程式为:2FeCl2+Cl2═2FeCl3;
(4)方法1:氨水是一种常见的碱,所以溶液的pH大于7,足量的二氧化硫,与氨水生成亚硫酸铵,不足量的二氧化硫,与氨水反应生成亚硫酸氢氨,题中是氨水在吸收二氧化硫,氨水相对于二氧化硫是过量的,所以氨水充分吸收二氧化硫所得的产物为:B;
方法2:二氧化硫与碳酸钙、氧气反应生成硫酸钙和二氧化碳,化学方程式为:2CaCO3+O2+2SO2=2CaSO4+2CO2.故答案为:(1)4FeS2+11O2
2Fe2O3+8SO2,快速燃烧、充足燃烧;
(2)2Fe2O3+6HCl═2FeCl3+3H2O,不行,主产物不再是氯化铁;
(3)2FeCl2+Cl2═2FeCl3;
(4)方法1:>,B;
方法2:2CaCO3+O2+2SO2═2CaSO4+2CO2.
| ||
(2)流程中需用30%的盐酸“酸溶”焙烧后的残渣,盐酸和氧化铁反应生成氯化铁和水,化学方程式为:2Fe2O3+6HCl═2FeCl3+3H2O,酸溶”时可改用硫酸,硫酸和氧化铁反应生成硫酸铁和水,而题中需要制备氯化铁晶体,所以不能改用硫酸,原因是:主产物不再是氯化铁;
(3)通过分析题中的反应原理,酸溶后的混合物中通入氯气制取氯化铁,氯气和氯化亚铁反应生成氯化铁,化学方程式为:2FeCl2+Cl2═2FeCl3;
(4)方法1:氨水是一种常见的碱,所以溶液的pH大于7,足量的二氧化硫,与氨水生成亚硫酸铵,不足量的二氧化硫,与氨水反应生成亚硫酸氢氨,题中是氨水在吸收二氧化硫,氨水相对于二氧化硫是过量的,所以氨水充分吸收二氧化硫所得的产物为:B;
方法2:二氧化硫与碳酸钙、氧气反应生成硫酸钙和二氧化碳,化学方程式为:2CaCO3+O2+2SO2=2CaSO4+2CO2.故答案为:(1)4FeS2+11O2
| ||
(2)2Fe2O3+6HCl═2FeCl3+3H2O,不行,主产物不再是氯化铁;
(3)2FeCl2+Cl2═2FeCl3;
(4)方法1:>,B;
方法2:2CaCO3+O2+2SO2═2CaSO4+2CO2.
点评:在解此类题时,首先分析题中的反应原理,然后找出对应的学过的知识点,然后结合题中所给的知识进行分析解答.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
某无色气体可能含有H2、CO、CH4中的一种或几种,依次进行下列实验(假设每一步反应或吸收均完全):①无色气体在氧气中充分燃烧;②燃烧生成的气体通过盛浓硫酸的洗气瓶,装置质量增加10.8g;③再将剩余气体通过盛NaOH溶液的洗气瓶,装置质量增加13.2g.下列推断不正确的是( )
| A、该气体一定含有H2、CO、CH4 |
| B、该气体可能含有H2和CO |
| C、该气体可能含有CO和CH4 |
| D、该气体可能含有CH4 |


