题目内容
电石是一种重要的化工原料,极易与水反应:CaC2+2H2O=Ca(OH)2+X↑.
(1)将电石长期露置于空气中,会发生下列变化:电石(CaC2)→灰浆→残渣.题干中电石与水反应后所得的气体X的化学式是 ,残渣中主要成分是Ca(OH)2和 (写名称).
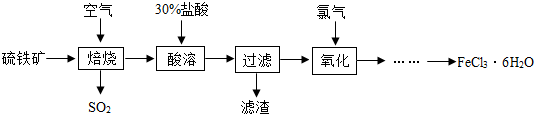
(2)工业上利用电石制备某化工原料的流程如图(注:加入NH4Cl溶液的目的是溶解残渣中的难溶盐):
①向CaCl2溶液中通入NH3、CO2两种气体,生成CaCO3的化学方程式为 .
②流程中溶液A可循环使用,溶液A中的主要成分的化学式是 .
③实验室中对过滤所得的固体进行洗涤在 中进行,加洗涤剂时以浸没固体的量为宜.
(3)检验沉淀洗涤干净的方法:取最后一次洗涤液少量置于试管中滴加试剂硝酸银溶液,观察到 已经洗涤干净.
(4)电石应该 保存.
(1)将电石长期露置于空气中,会发生下列变化:电石(CaC2)→灰浆→残渣.题干中电石与水反应后所得的气体X的化学式是
(2)工业上利用电石制备某化工原料的流程如图(注:加入NH4Cl溶液的目的是溶解残渣中的难溶盐):

①向CaCl2溶液中通入NH3、CO2两种气体,生成CaCO3的化学方程式为
②流程中溶液A可循环使用,溶液A中的主要成分的化学式是
③实验室中对过滤所得的固体进行洗涤在
(3)检验沉淀洗涤干净的方法:取最后一次洗涤液少量置于试管中滴加试剂硝酸银溶液,观察到
(4)电石应该
考点:质量守恒定律及其应用,证明盐酸和可溶性盐酸盐,物质的相互转化和制备,书写化学方程式、文字表达式、电离方程式
专题:物质的制备,化学用语和质量守恒定律
分析:(1)根据质量守恒定律和氢氧化钙露置在空气中,会与空气中的二氧化碳反应生成碳酸钙进行解答;
(2)①由流程图找出反应物和生成物,正确书写化学方程式;②根据①的解答回答;③实验室中对过滤所得的固体进行洗涤在过滤器中进行.
(3)根据过滤出的固体中可能沾有氯化铵,氯离子与银离子能结合成氯化银白色沉淀进行解答;
(4)根据电石极易与水反应进行解答.
(2)①由流程图找出反应物和生成物,正确书写化学方程式;②根据①的解答回答;③实验室中对过滤所得的固体进行洗涤在过滤器中进行.
(3)根据过滤出的固体中可能沾有氯化铵,氯离子与银离子能结合成氯化银白色沉淀进行解答;
(4)根据电石极易与水反应进行解答.
解答:解:(1)根据CaC2+2H2O=Ca(OH)2+X↑.可知反应前有Ca1个,C2个,H4个,O2个,反应后Ca1个,H2个,O2个,故X中有C2个,H2个,故化学式
为:C2H2;因为电石与水反应生成氢氧化钙,其露置在空气中,会与空气中的二氧化碳反应生成碳酸钙,故残渣中主要成分是Ca(OH)2和碳酸钙;
(2)①由流程图可以看出,反应物为氨气和二氧化碳和氯化钙和水,生成物为碳酸钙和氯化铵,用观察法配平,碳酸钙后面标上沉淀符号,其反应的化学方程式为:CaCl2+2NH3+CO2+H2O=CaCO3↓+2NH4Cl;
②由①中的化学方程式可以得知,A溶液的化学式为:NH4Cl.
③实验室中对过滤所得的固体进行洗涤在过滤器中进行,加洗涤剂时以浸没固体的量为宜.
(3)因过滤出的固体中可能沾有氯化铵,故加入硝酸银后,如果没有明显现象,则证明已洗涤干净.
(4)因电石极易与水反应,故应密封保存.
故答案为:(1)C2H2;碳酸钙; (2)①CaCl2+2NH3+CO2+H2O=CaCO3↓+2NH4Cl; ②NH4Cl; ③过滤器;(3)无明显现象; (4)密封;
为:C2H2;因为电石与水反应生成氢氧化钙,其露置在空气中,会与空气中的二氧化碳反应生成碳酸钙,故残渣中主要成分是Ca(OH)2和碳酸钙;
(2)①由流程图可以看出,反应物为氨气和二氧化碳和氯化钙和水,生成物为碳酸钙和氯化铵,用观察法配平,碳酸钙后面标上沉淀符号,其反应的化学方程式为:CaCl2+2NH3+CO2+H2O=CaCO3↓+2NH4Cl;
②由①中的化学方程式可以得知,A溶液的化学式为:NH4Cl.
③实验室中对过滤所得的固体进行洗涤在过滤器中进行,加洗涤剂时以浸没固体的量为宜.
(3)因过滤出的固体中可能沾有氯化铵,故加入硝酸银后,如果没有明显现象,则证明已洗涤干净.
(4)因电石极易与水反应,故应密封保存.
故答案为:(1)C2H2;碳酸钙; (2)①CaCl2+2NH3+CO2+H2O=CaCO3↓+2NH4Cl; ②NH4Cl; ③过滤器;(3)无明显现象; (4)密封;
点评:本题综合考查了产物的判断、化学方程式的书写,锻炼了学生的逻辑思维和分析解决问题的能力.

练习册系列答案
相关题目
在一密闭容器中,有甲、乙、丙、丁四种物质,在一定条件下存在某个反应,测得反应前后各物质的质量如下表.下列说法正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 20 | m | 20 | 20 |
| 反应后质量/g | 2 | 待测 | 32 | 26 |
| A、参加反应的甲、丙、丁的质量比为1:16:13 |
| B、乙可能是该反应的催化剂 |
| C、待测物质一定为4g |
| D、该反应是化合反应 |
 南海、钓鱼岛及其附属海域是我国固有领土,蕴藏着丰富的海洋资源.
南海、钓鱼岛及其附属海域是我国固有领土,蕴藏着丰富的海洋资源.