题目内容
11.将Cu-Zn合金粉末放到盛有稀硫酸的烧杯中,恰好完全反应.相关实验数据如表:| Cu-Zn合金的质量/g | 稀硫酸的质量/g | 反应后烧杯内物质的总质量/g |
| 4.0 | 10 | 13.96 |
(2)若不考虑该合金中除Cu、Zn以外的其它成分.请计算稀硫酸的溶质质量分数.
分析 根据稀硫酸和锌反应生成硫酸锌和氢气,所以反应前后减少的质量就是氢气的质量进行解答.
解答 解:(1)根据质量守恒定律,则生成氢气的质量=10g+4.0g-13.96g=0.04g,故填:0.04;
(2)设反应中消耗硫酸的质量为x,
Zn+H2SO4=ZnSO4+H2↑
98 2
x 0.04g
$\frac{98}{x}=\frac{2}{0.04g}$
x=1.96g
稀硫酸的溶质质量分数为$\frac{1.96g}{10g}×100%$=19.6%
答:稀硫酸的溶质质量分数为19.6%.
点评 此题考查的是根据化学方程式的有关计算,学会分析处理表中的数据是解答此题的关键.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
1.除去下列各物质中少量杂质,所选用的试剂和操作方法均正确的是( )
| 选项 | 物质(括号内为杂质) | 试剂 | 操作方法 |
| A | CaCO3(CaO) | 无 | 高温 |
| B | H2O(植物油) | 洗涤剂 | 振荡、搅拌 |
| C | CuO(铜粉) | 足量氧气 | 灼烧 |
| D | KCl(KClO3) | 二氧化锰 | 加热 |
| A. | A | B. | B | C. | C | D. | D |
16.下列关于S、Fe与氧气反应的相关说法,其中正确的是( )
| A. | S在氧气中燃烧会产生大量白烟 | |
| B. | Fe在氧气中燃烧反应生成Fe2O3 | |
| C. | Fe在氧气中燃烧是吸热反应 | |
| D. | S、Fe与氧气反应均体现了氧气的氧化性 |
20.下列气体中能供给呼吸的是( )
| A. | 氧气 | B. | 氮气 | C. | 二氧化碳 | D. | 水蒸气 |
1. 向一定量盐酸和CuCl2溶液的混合物中逐滴加入NaOH溶液,产生沉淀的质量与加入NaOH溶液的质量关系如图所示.下列说法正确的是( )
向一定量盐酸和CuCl2溶液的混合物中逐滴加入NaOH溶液,产生沉淀的质量与加入NaOH溶液的质量关系如图所示.下列说法正确的是( )
 向一定量盐酸和CuCl2溶液的混合物中逐滴加入NaOH溶液,产生沉淀的质量与加入NaOH溶液的质量关系如图所示.下列说法正确的是( )
向一定量盐酸和CuCl2溶液的混合物中逐滴加入NaOH溶液,产生沉淀的质量与加入NaOH溶液的质量关系如图所示.下列说法正确的是( )| A. | P点表示的溶液pH=7 | |
| B. | MN段表示CuCl2与NaOH反应 | |
| C. | 从M点到N点溶液质量增加20 g | |
| D. | P点表示的溶液比N点表示的溶液中氯化钠的质量分数大 |
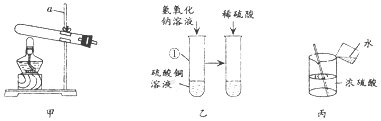

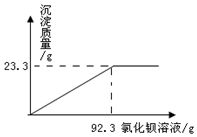 某硫酸铵[(NH4)2SO4]样品,可能含有少量的氯化铵[NH4Cl],为了测定硫酸铵样品中硫酸铵的质量分数,取样品16.0g,加入40.0g水中完全溶解后,向溶液中加入某种质量分数的氯化钡溶液,实验中精确测得产生白色沉淀的质量与加入氯化钡溶液的质量的关系如图所示.
某硫酸铵[(NH4)2SO4]样品,可能含有少量的氯化铵[NH4Cl],为了测定硫酸铵样品中硫酸铵的质量分数,取样品16.0g,加入40.0g水中完全溶解后,向溶液中加入某种质量分数的氯化钡溶液,实验中精确测得产生白色沉淀的质量与加入氯化钡溶液的质量的关系如图所示.