题目内容
19.有一含有纯碱的食盐样品,某同学称取30g的样品放入烧杯中,向烧杯中加入100g足量的稀盐酸,充分反应后气体全部逸出,烧杯中剩余物的总质量为125.6g.(1)反应生成气体的质量是4.4g.
(2)反应后所得溶液中溶质的质量分数是多少?(精确到0.1%)
分析 (1)根据质量守恒定律结合物质的质量反应前后的变化可得出生成的二氧化碳的质量;
(2)根据化学方程式结合二氧化碳的质量可以计算出碳酸钠的质量和生成氯化钠的质量.反应后所得溶液为氯化钠溶液,而样品中的氯化钠不与盐酸反应;至完全反应后,所得溶液为氯化钠溶液,其溶质氯化钠由两部分组成:一部分为原混合物质中的氯化钠,另一部分则是反应生成的氯化钠;
综上所述,所得溶液中溶质质量分数,则是原混合物中氯化钠与生成氯化钠质量总和与所得溶液的质量比.
解答 解:(1)根据质量守恒定律,可得出生成的二氧化碳的质量为:30g+100g-125.6g=4.4g;故填4.4;
(2)设30g样品中碳酸钠的质量为x,生成NaCl的质量为y
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 117 44
x y 4.4g
$\frac{106}{x}=\frac{117}{y}=\frac{44}{4.4g}$,
x=10.6g,y=11.7g,
所得溶液中氯化钠的质量质量分数$\frac{11.7g+30g-10.6g}{125.6g}$×100%≈24.8%
答:反应后所得溶液中溶质的质量分数24.8%.
点评 此题是对化学方程式以及溶液相关问题的考查,利用质量守恒定律,计算出反应放出二氧化碳的质量是解决问题的基础.

练习册系列答案
相关题目
9.推理和归纳是研究和学习化学的重要方法,以下说法正确的是( )
| A. | 分子可以构成物质,所以物质都是由分子构成的 | |
| B. | 离子是带电荷的粒子,所以带电荷的粒子一定是离子 | |
| C. | 因为水电解只产生氢气和氧气,所以水中只含氢、氧两种元素 | |
| D. | 氧化物中肯定含有氧元素,所以含氧元素的化合物一定是氧化物 |
10.下列是初中化学所学习到的物质,其中属于纯净物的是( )
| A. | 干冰 | B. | 可燃冰 | ||
| C. | 净化后的空气 | D. | 高锰酸钾受热分解后的剩余固体 |
7.下列化学用语表示正确的是( )
| A. | 氯化铁:FeCl2 | B. | 两个氧原子:2O | ||
| C. | 镁离子:Mg+2 | D. | 氧元素显-2价:O2- |
11.将Cu-Zn合金粉末放到盛有稀硫酸的烧杯中,恰好完全反应.相关实验数据如表:
(1)生成氢气的质量为0.04g.
(2)若不考虑该合金中除Cu、Zn以外的其它成分.请计算稀硫酸的溶质质量分数.
| Cu-Zn合金的质量/g | 稀硫酸的质量/g | 反应后烧杯内物质的总质量/g |
| 4.0 | 10 | 13.96 |
(2)若不考虑该合金中除Cu、Zn以外的其它成分.请计算稀硫酸的溶质质量分数.
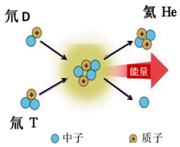 中科院的“人造太阳”EAST物理实验获重大突破,实验中首次实现持续时间达102秒的超高温长脉冲等离子体放电,为目前世界最长,其原理如图.
中科院的“人造太阳”EAST物理实验获重大突破,实验中首次实现持续时间达102秒的超高温长脉冲等离子体放电,为目前世界最长,其原理如图. 