题目内容
8.某同学在实验室进行有关浓硫酸的实验,观察瓶上的标签(如表所示).他从瓶中倒出100克用于配制成稀硫酸,求:(1)这瓶浓硫酸的质量为920g,其中含溶质纯硫酸的质量901.6g.
(2)将这100克浓硫酸与100克10%的硫酸溶液均匀混合,所得稀硫酸的质量分数是多少?
| 浓硫酸(H2SO4) 500毫升 | |
| 浓度(质量分数) | 98% |
| 密度 | 1.84克/厘米3 |
| 相对分子质量 | 98 |
| 强腐蚀性,阴冷,密封贮藏 | |
分析 (1)根据溶液的质量=溶液的体积×溶液的密度,溶质的质量=溶液的质量×溶质的质量分数来分析解答;
(2)根据溶质的质量分数=$\frac{溶质的质量}{溶液的质量}$×100%分析解答;
(3)根据溶液稀释前后溶质质量不变,可求出需要浓硫酸的质量,进一步计算出所需水的质量与体积.
解答 解:(1)这瓶浓硫酸的质量为:500毫升×1.84克/厘米3=920克;其中含溶质纯硫酸的质量为:920g×98%=901.6g;故填:920g;901.6g;
(2)将这100克浓硫酸与100克10%的硫酸溶液均匀混合,所得稀硫酸的质量分数为:$\frac{100g×98%+100g×10%}{100g+100g}×100%$=54%
答:所得溶液的溶质的质量分数为54%;
(3)设需要98%的浓硫酸的质量为x,则
98%x=500g×19.6%
x=100g
所需水的质量为:500g-100g=400g
水的体积为:400g÷1g/mL=400mL
答:需要加水400mL.
点评 本题考查物质质量分数有关计算等,比较基础,注意对公式的理解越灵活运用.

练习册系列答案
相关题目
19. 某同学采用如图装置,用一些植物的器官来代替MnO2作催化剂,分解H2O2制取氧气.实验各取溶质质量分数15%H2O2溶液的质量34克,记录数据如下表.
某同学采用如图装置,用一些植物的器官来代替MnO2作催化剂,分解H2O2制取氧气.实验各取溶质质量分数15%H2O2溶液的质量34克,记录数据如下表.
请依据上述信息分析:
(1)要使胡萝卜能够更快地催化过氧化氢的分解,可采用的方法是将胡萝卜切碎.
(2)当量筒内的水达到80毫升时,打开广口瓶的橡皮塞,立即将带火星的木条伸入瓶内,却发现木条不能复燃.请你解释木条不能复燃的原因可能是:水蒸气含量偏高.
(3)计算:34克15%的H2O2溶液中的溶质完全分解,能制得氧气多少克?
 某同学采用如图装置,用一些植物的器官来代替MnO2作催化剂,分解H2O2制取氧气.实验各取溶质质量分数15%H2O2溶液的质量34克,记录数据如下表.
某同学采用如图装置,用一些植物的器官来代替MnO2作催化剂,分解H2O2制取氧气.实验各取溶质质量分数15%H2O2溶液的质量34克,记录数据如下表.| 序号 | 植物的器官及质量 | 收集气体的体积(毫升) | 收集气体的时间(分钟) |
| 1 | 大颗粒胡萝卜16克 | 80 | 18 |
| 2 | 大颗粒马铃薯16克 | 80 | 10.5 |
| 3 | 小颗粒马铃薯16克 | 80 | 4 |
(1)要使胡萝卜能够更快地催化过氧化氢的分解,可采用的方法是将胡萝卜切碎.
(2)当量筒内的水达到80毫升时,打开广口瓶的橡皮塞,立即将带火星的木条伸入瓶内,却发现木条不能复燃.请你解释木条不能复燃的原因可能是:水蒸气含量偏高.
(3)计算:34克15%的H2O2溶液中的溶质完全分解,能制得氧气多少克?
16.小柯看到妈妈炒的一盘紫色高丽菜(一种紫色的卷心菜)的菜汁呈紫色,后来因为掺了醋变成了红色,在洗盘子时遇到碱性洗涤剂变成黄绿色.下列也能使紫色高丽菜汁呈现黄绿色的物质是( )
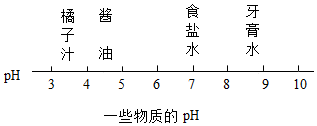

| A. | 橘子汁 | B. | 牙膏水 | C. | 食盐水 | D. | 酱油 |
17.根据《山东省城镇体系规划》,淄博市将被确立为中心城市.这将掀起又一轮经济投资热.为避免投资办厂引起的环境污染,下列措施可行的是( )
| A. | 对工厂的烟筒加高处理 | |
| B. | 工厂废水直接排放 | |
| C. | 对工厂的固体废弃物进行无害化处理 | |
| D. | 化工厂建在居民区 |
18.小冰取氯酸钾和氯化钾的混合物共20g,向其中加入5g二氧化锰,加热到不再产生气体为止,精确测量得知实验共生成氧气5.1g,则原20g混合物中钾元素的总质量为( )
| A. | 3.9g | B. | 4.14g | C. | 7.8g | D. | 7.92g |