题目内容
16.小柯看到妈妈炒的一盘紫色高丽菜(一种紫色的卷心菜)的菜汁呈紫色,后来因为掺了醋变成了红色,在洗盘子时遇到碱性洗涤剂变成黄绿色.下列也能使紫色高丽菜汁呈现黄绿色的物质是( )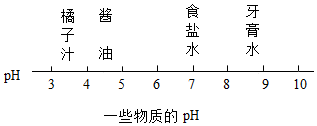
| A. | 橘子汁 | B. | 牙膏水 | C. | 食盐水 | D. | 酱油 |
分析 依据紫色高丽菜汁遇到碱性洗涤剂变成黄绿色可知:要想使紫色高丽菜汁呈现在黄绿色的物质必然显碱性,然后依据pH>7的溶液显碱性分析选择即可;
解答 解:依据题干叙述可知紫色高丽菜汁遇酸性溶液(醋酸是酸性溶液)变红,遇到碱性溶液会变成黄绿色,所以要想使紫色高丽菜汁呈现黄绿色的物质应该显碱性,因为pH>7的溶液显碱性、pH<7呈酸性、pH=7呈中性,据选项物质的pH图表可知:牙膏水pH>7,橘子汁、酱油pH<7显酸性,食盐水pH=7呈中性.
故选B.
点评 此题是与酸碱指示剂相关的考查题,依据题干结合学过的有关的酸碱指示剂的知识即可顺利解题.

练习册系列答案
 每课必练系列答案
每课必练系列答案
相关题目
6.在下列生活和生产过程中,发生了化学变化的是( )
| A. | 食物的消化 | B. | 活性炭净水 | ||
| C. | 干冰作制冷剂 | D. | 稀有气体通电发出彩光 |
7.下列有关实验现象的描述正确的是( )
| A. | 铁丝在氧气中燃烧时火星四射,有四氧化三铁生成 | |
| B. | 将高锰酸钾加入汽油中,振荡,得到紫红色溶液 | |
| C. | 打开浓盐酸试剂瓶的瓶塞,瓶口上方出现大量白烟 | |
| D. | 硫在空气中或氧气中燃烧,都会生成有刺激性气味的气体 |
4. 如图所示的装置有洗涤、收集和储存气体等多种用途(视实验需要,瓶中可装入不同物质).下列四个实验中均要使用该装置,则气体或水入口为y的是( )
如图所示的装置有洗涤、收集和储存气体等多种用途(视实验需要,瓶中可装入不同物质).下列四个实验中均要使用该装置,则气体或水入口为y的是( )
 如图所示的装置有洗涤、收集和储存气体等多种用途(视实验需要,瓶中可装入不同物质).下列四个实验中均要使用该装置,则气体或水入口为y的是( )
如图所示的装置有洗涤、收集和储存气体等多种用途(视实验需要,瓶中可装入不同物质).下列四个实验中均要使用该装置,则气体或水入口为y的是( )| A. | 排空气法收集氢气 | |
| B. | 排空气法收集二氧化碳 | |
| C. | 瓶中装有适量的NaOH溶液,除去氧气中少量的二氧化碳气体 | |
| D. | 瓶中装有氧气,将水从导气管通入以取用瓶内储存的氧气 |
11.根据表格回答下列问题:
(1)20℃时氯化钠的溶解度是36g,
(2)要将氯化钠晶体从氯化钠的溶液中析出,通常采用蒸发溶剂的方法.
| 温度/℃ | 0 | 10 | 20 | 40 | 60 | 80 | 100 |
| 氯化钠/克 | 35.7 | 35.8 | 36 | 36.6 | 37.3 | 38.4 | 39.8 |
(2)要将氯化钠晶体从氯化钠的溶液中析出,通常采用蒸发溶剂的方法.
8.某同学在实验室进行有关浓硫酸的实验,观察瓶上的标签(如表所示).他从瓶中倒出100克用于配制成稀硫酸,求:
(1)这瓶浓硫酸的质量为920g,其中含溶质纯硫酸的质量901.6g.
(2)将这100克浓硫酸与100克10%的硫酸溶液均匀混合,所得稀硫酸的质量分数是多少?
(3)欲配制500克溶质质量分数为19.6%的稀硫酸,需要加水多少毫升?
(1)这瓶浓硫酸的质量为920g,其中含溶质纯硫酸的质量901.6g.
(2)将这100克浓硫酸与100克10%的硫酸溶液均匀混合,所得稀硫酸的质量分数是多少?
| 浓硫酸(H2SO4) 500毫升 | |
| 浓度(质量分数) | 98% |
| 密度 | 1.84克/厘米3 |
| 相对分子质量 | 98 |
| 强腐蚀性,阴冷,密封贮藏 | |
5.以下对20℃的硝酸钾溶解度为31.6 g的解释中正确( )
| A. | 20℃,31.6 g硝酸钾完全溶解在水中 | |
| B. | 20℃,100 g溶液含31.6g硝酸钾 | |
| C. | 100g水中最多能溶解31.6g硝酸钾 | |
| D. | 20℃,31.6 g硝酸钾溶解在100g水中恰好饱和 |
6.下列各条件下,氢氧化钙质量分数最小的一项是( )
| A. | 100C时的饱和溶液 | B. | 20℃时的饱和溶液 | ||
| C. | 50℃时的不饱和溶液 | D. | 50℃时的饱和溶液 |