题目内容
3.某化学课外兴趣小组通过查阅资料知道过氧化钠(Na2O2)能与水反应生成氢氧化钠和氧气,于是他们做了以下探究实验.实验1:向包有过氧化钠粉末的脱脂棉上滴水,脱脂棉燃烧起来.
请你对脱脂棉燃烧的原因进行分析过氧化钠和水反应生成的氧气和脱脂棉接触,同时放热使温度达到了脱脂棉的着火点.
实验2:向盛有过氧化钠粉末的试管中加入水,充分反应后,取试管中的少量溶液放入另一小试管中加入几滴无色酚酞试液,溶液变红,过了一会,红色又褪去了.
[提出问题]溶液为什么先变红,过了一会,红色又褪去了呢?
[猜想]甲同学认为是氢氧化钠溶液与空气中的二氧化碳反应的缘故,该反应的化学方程式为2NaOH+CO2═Na2CO3+H2O.乙同学认为甲同学的猜想不正确,理由是碳酸钠溶液显碱性,也能使酚酞试液变红色.
[查阅资料]①滴加酚酞呈现红色的溶液遇到H2O2时,H2O2可以破坏酚酞的结构,使酚酞在碱性溶液中不能再显红色;②酚酞在稀碱性溶液中稳定显红色,而在浓氢氧化钠等溶液中显红色后又褪色.
[猜想]通过查阅资料后,该兴趣小组对溶液的红色褪去的主要原因进行了猜想.
猜想A:过氧化钠与水反应可能生成了H2O2;猜想B:生成的氢氧化钠溶液可能太浓.
[实验探究]请你将下列实验方案填写完整
| 猜想 | 实验操作 | 实验现象 | 结论 |
| A | 取过氧化钠与水反应后的溶液放入试管中, 加入适量二氧化锰后,把带火星的木条放在试管口 | 带火星的木条复燃 | 猜想A 正确 |
| B | 取过氧化钠与水反应后的溶液放入试管中, 加入足量的水后,滴加酚酞试液 | 溶液变红,过了一会,红色又褪去了 | 猜想B 错误 |
分析 实验1:可燃物燃烧的条件是:与氧气接触,温度达到可燃物的着火点,二者必须同时具备,缺一不可;
实验2:
[猜想]氢氧化钠和二氧化碳反应生成碳酸钠和水,碳酸钠溶液显碱性,能使酚酞试液变红色;
[实验探究]过氧化氢在二氧化锰催化作用下分解生成水和氧气,氧气能使带火星的木条复燃;
[得出结论]过氧化钠和水反应能够生成氢氧化钠和过氧化氢.
解答 解:实验1:
脱脂棉燃烧的原因是:过氧化钠和水反应生成的氧气和脱脂棉接触,同时放热使温度达到了脱脂棉的着火点.
故填:过氧化钠和水反应生成的氧气和脱脂棉接触,同时放热使温度达到了脱脂棉的着火点.
实验2:
[猜想]氢氧化钠和二氧化碳反应生成碳酸钠和水,该反应的化学方程式为:2NaOH+CO2═Na2CO3+H2O;
乙同学认为甲同学的猜想不正确,理由是:碳酸钠溶液显碱性,也能使酚酞试液变红色.
故填:2NaOH+CO2═Na2CO3+H2O;碳酸钠溶液显碱性,也能使酚酞试液变红色.
[实验探究]实验方案如下表所示:
| 猜想 | 实验操作 | 实验现象 | 结论 |
| A | 取过氧化钠与水反应后的溶液放入试管中,加入适量二氧化锰后,把带火星的木条放在试管口 | 带火星的木条复燃 | 猜想A 正确 |
| B | 取过氧化钠与水反应后的溶液放入试管中,加入足量的水后,滴加酚酞试液 | 溶液变红,过了一会,红色又褪去了 | 猜想B 错误 |
故填:Na2O2+2H2O=2NaOH+H2O2.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
相关题目
14.将汽车尾气中的有毒气体转化为空气中的成分,其微观结构示意图如下,说法不严谨的是( )
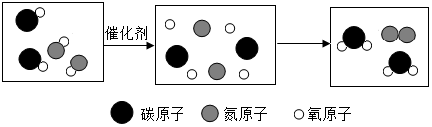

| A. | 反应前有两种物质的分子 | |
| B. | 化学变化的本质是:分子分成原子,原子重新组合成新物质的分子 | |
| C. | 在化学变化中,分子分成原子,原子重新组合成新物质 | |
| D. | 图中共有三种氧化物 |
11.除去下列物质中的杂志所选用的试剂及操作方法正确的一组是( )
| 物 质 | 所含杂质 | 除 去 杂 质 的 方 法 | |
| A | KOH溶液 | K2CO3 | 过量的Ca(OH)2溶液,过滤 |
| B | NaCl | Na2CO3 | 过量的盐酸、蒸发结晶 |
| C | H2气体 | 氯化氢、水蒸气 | 依次通过足量的浓硫酸、硝酸银溶液 |
| D | KNO3 | NaCl | 溶解、蒸发结晶、过滤 |
| A. | A | B. | B | C. | C | D. | D |
8.2015年10月5日中国药学家屠呦呦因创制新型抗疟药--青蒿素(化学式为C15H22O5)而成为首位获得诺贝尔科学类奖项的中国人.下列有关青蒿素的说法中正确的是( )
| A. | 青蒿素由C、H、O三种元素组成 | |
| B. | 青蒿素由15个碳原子、22个氢原子和5个氧原子构成 | |
| C. | 青蒿素中C、H、O三种元素的质量比为15:22:5 | |
| D. | 青蒿素中H元素的质量分数最高 |
15.下列图示实验操作中,不正确的是( )
| A. |  过滤 | B. |  滴加液体 | ||
| C. |  加热液体 | D. |  检查装置的气密性 |
12.为得知7克高锰酸钾完全分解能产生多少克氧气,小柯与小妍分别采取了以下方法:
请回答:
(1)在本实验条件下氧气的密度为1.4×10-3克/厘米3,则由小柯的测量结果可以算出7克高锰酸钾分解后所产生的氧气质量为0.84克;
(2)大家经过讨论,认为小妍的计算方法明显错误,此题不能采用该方法计算氧气质量的一项理由是B;
A.高锰酸钾中含氧元素B.锰酸钾和二氧化锰中含氧元素C.氧气中含氧元素
(3)请通过化学方程式计算7克高锰酸钾完全分解所产生的氧气质量;
(4)若实验操作无误,不考虑实验中的误差,针对小柯的测定结果与你的计算结果,请提出一种合理的猜测:可能是生成锰酸钾或二氧化锰分解放出了氧气.
| 小柯:实验测定法 | 小妍:计算法 |
| 小柯在老师指导下,将7克高锰酸钾充分加热,得到氧气600厘米3 | 解:高锰酸钾中氧元素的质量分数: =$\frac{O的相对原子质量×4}{KMn{O}_{4}的相对分子质量}$×100%=$\frac{16×4}{39+55+16×4}$×100%=40.5% 氧气的质量为7克×40.5%=2.84克 答:7克高锰酸钾完全分解产生氧气2.84克. |
(1)在本实验条件下氧气的密度为1.4×10-3克/厘米3,则由小柯的测量结果可以算出7克高锰酸钾分解后所产生的氧气质量为0.84克;
(2)大家经过讨论,认为小妍的计算方法明显错误,此题不能采用该方法计算氧气质量的一项理由是B;
A.高锰酸钾中含氧元素B.锰酸钾和二氧化锰中含氧元素C.氧气中含氧元素
(3)请通过化学方程式计算7克高锰酸钾完全分解所产生的氧气质量;
(4)若实验操作无误,不考虑实验中的误差,针对小柯的测定结果与你的计算结果,请提出一种合理的猜测:可能是生成锰酸钾或二氧化锰分解放出了氧气.
13.下列各组物质能在pH=1的无色溶液中大量共存的是( )
| A. | ZnSO4 NaNO3 KCl | B. | Cu(NO3)2 NaCl KNO3 | ||
| C. | Na2CO3 KNO3 NH4Cl | D. | K2SO4 Ba(OH)2 KCl |

