题目内容
18.金属钠很软,可以用刀切割.切开外皮后,可以看到钠具有银白色的金属光泽.钠是热和电的良导体.钠的密度是0.97g/cm3,比水的密度小,钠的熔点是97.81℃,沸点是882.9℃.将金属钠放入水中,可以反应生成NaOH和H2;钠跟氧气混合加热生成淡黄色的过氧化钠(Na2O2)固体,钠跟CO2在加热条件下反应生成碳酸钠和单质碳.(1)试写出钠跟水反应的化学方程式2Na+2H2O=2NaOH+H2↑.
(2)小刘同学用图A装置做钠跟氧气反应实验,观察到生成物中出现黑色固体,则该黑色固体是C(填化学式),试写出相应的化学反应方程式4Na+3CO2$\frac{\underline{\;\;△\;\;}}{\;}$C+2Na2CO3.

(3)为了探究黑色固体成分,小刘同学进行了下列探究.
探究反应中CO2的来源:
猜想①:CO2的来源于空气;猜想②:CO2的来源于酒精燃烧;在上述两种来源中,②(填序号)是CO2的主要来源.用图B和C装置实验的目的是验证空气中的二氧化碳是否参加反应.
分析 (1)根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式;
(2)空气中含有二氧化碳,酒精燃烧生成二氧化碳;
(3)酒精燃烧产生的二氧化碳在相同的空间中含量远大于空气中的二氧化碳含量.
解答 解:(1)钠跟水反应生成氢氧化钠和氢气,反应的化学方程式为:2Na+2H2O=2NaOH+H2↑.
故填:2Na+2H2O=2NaOH+H2↑.
(2)小刘同学用图A装置做钠跟氧气反应实验,观察到生成物中出现黑色固体,则该黑色固体是C,是二氧化碳和钠反应生成的,钠和二氧化碳反应的化学方程式为:4Na+3CO2$\frac{\underline{\;\;△\;\;}}{\;}$C+2Na2CO3.
故填:C;4Na+3CO2$\frac{\underline{\;\;△\;\;}}{\;}$C+2Na2CO3.
(3)
猜想①:CO2的来源于空气;
猜想②:CO2的来源于酒精燃烧;
在上述两种来源中,②是CO2的主要来源;
用图B和C装置实验的目的是验证空气中的二氧化碳是否参加反应,如果空气中的二氧化碳和钠发生反应,则B中生成的淡黄色固体中含有少量黑色固体,反之则没有黑色固体.
故填:空气;酒精燃烧;②;验证空气中的二氧化碳是否参加反应.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
8. 钾是维持人体生命和植物生长所必须的元素.如图是从元素周期表中得出的部分信息.下列有关叙述错误的是( )
钾是维持人体生命和植物生长所必须的元素.如图是从元素周期表中得出的部分信息.下列有关叙述错误的是( )
 钾是维持人体生命和植物生长所必须的元素.如图是从元素周期表中得出的部分信息.下列有关叙述错误的是( )
钾是维持人体生命和植物生长所必须的元素.如图是从元素周期表中得出的部分信息.下列有关叙述错误的是( )| A. | 钾原子的核外电子数为19 | |
| B. | 钾原子的相对原子质量为39.10 | |
| C. | 给农作物补充钾元素,可施用草木灰 | |
| D. | 钾原子在化学反应中易得电子形成稳定结构 |
6.下列物质的用途体现其化学性质的是( )
| A. | 用熟石灰来改良酸性土壤 | B. | 用洗涤剂去除油污 | ||
| C. | 用干冰进行人工降雨 | D. | 用石墨做干电池的电极 |
13.下列四个图象能正确反映实验变化关系的是( )
| A. | 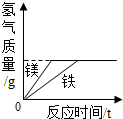 常温下,向等质量、等质量分数的稀盐酸中分别加入锌粉和铁粉 | |
| B. |  敞口放置于空气中的浓硫酸或稀盐酸 | |
| C. |  加热KNO3、Ca(OH)2的饱和溶液(不考虑溶剂的蒸发) | |
| D. |  少量的碳在密闭的集气瓶中与氧气完全燃烧 |
3.某化学课外兴趣小组通过查阅资料知道过氧化钠(Na2O2)能与水反应生成氢氧化钠和氧气,于是他们做了以下探究实验.
实验1:向包有过氧化钠粉末的脱脂棉上滴水,脱脂棉燃烧起来.
请你对脱脂棉燃烧的原因进行分析过氧化钠和水反应生成的氧气和脱脂棉接触,同时放热使温度达到了脱脂棉的着火点.
实验2:向盛有过氧化钠粉末的试管中加入水,充分反应后,取试管中的少量溶液放入另一小试管中加入几滴无色酚酞试液,溶液变红,过了一会,红色又褪去了.
[提出问题]溶液为什么先变红,过了一会,红色又褪去了呢?
[猜想]甲同学认为是氢氧化钠溶液与空气中的二氧化碳反应的缘故,该反应的化学方程式为2NaOH+CO2═Na2CO3+H2O.乙同学认为甲同学的猜想不正确,理由是碳酸钠溶液显碱性,也能使酚酞试液变红色.
[查阅资料]①滴加酚酞呈现红色的溶液遇到H2O2时,H2O2可以破坏酚酞的结构,使酚酞在碱性溶液中不能再显红色;②酚酞在稀碱性溶液中稳定显红色,而在浓氢氧化钠等溶液中显红色后又褪色.
[猜想]通过查阅资料后,该兴趣小组对溶液的红色褪去的主要原因进行了猜想.
猜想A:过氧化钠与水反应可能生成了H2O2;猜想B:生成的氢氧化钠溶液可能太浓.
[实验探究]请你将下列实验方案填写完整
[得出结论]根据实验分析,过氧化钠与水反应除了生成氢氧化钠和氧气外,还存在另一反应,则另一反应的化学方程式为Na2O2+2H2O=2NaOH+H2O2.
实验1:向包有过氧化钠粉末的脱脂棉上滴水,脱脂棉燃烧起来.
请你对脱脂棉燃烧的原因进行分析过氧化钠和水反应生成的氧气和脱脂棉接触,同时放热使温度达到了脱脂棉的着火点.
实验2:向盛有过氧化钠粉末的试管中加入水,充分反应后,取试管中的少量溶液放入另一小试管中加入几滴无色酚酞试液,溶液变红,过了一会,红色又褪去了.
[提出问题]溶液为什么先变红,过了一会,红色又褪去了呢?
[猜想]甲同学认为是氢氧化钠溶液与空气中的二氧化碳反应的缘故,该反应的化学方程式为2NaOH+CO2═Na2CO3+H2O.乙同学认为甲同学的猜想不正确,理由是碳酸钠溶液显碱性,也能使酚酞试液变红色.
[查阅资料]①滴加酚酞呈现红色的溶液遇到H2O2时,H2O2可以破坏酚酞的结构,使酚酞在碱性溶液中不能再显红色;②酚酞在稀碱性溶液中稳定显红色,而在浓氢氧化钠等溶液中显红色后又褪色.
[猜想]通过查阅资料后,该兴趣小组对溶液的红色褪去的主要原因进行了猜想.
猜想A:过氧化钠与水反应可能生成了H2O2;猜想B:生成的氢氧化钠溶液可能太浓.
[实验探究]请你将下列实验方案填写完整
| 猜想 | 实验操作 | 实验现象 | 结论 |
| A | 取过氧化钠与水反应后的溶液放入试管中, 加入适量二氧化锰后,把带火星的木条放在试管口 | 带火星的木条复燃 | 猜想A 正确 |
| B | 取过氧化钠与水反应后的溶液放入试管中, 加入足量的水后,滴加酚酞试液 | 溶液变红,过了一会,红色又褪去了 | 猜想B 错误 |
8.下列化学方程式所对应的基本反应类型不正确的是( )
| A. | 2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$C+2MgO(置换反应) | |
| B. | 2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑(分解反应) | |
| C. | 2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2 (化合反应) | |
| D. | CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$ CO2+2H2O(置换反应) |