题目内容
8.2015年10月5日中国药学家屠呦呦因创制新型抗疟药--青蒿素(化学式为C15H22O5)而成为首位获得诺贝尔科学类奖项的中国人.下列有关青蒿素的说法中正确的是( )| A. | 青蒿素由C、H、O三种元素组成 | |
| B. | 青蒿素由15个碳原子、22个氢原子和5个氧原子构成 | |
| C. | 青蒿素中C、H、O三种元素的质量比为15:22:5 | |
| D. | 青蒿素中H元素的质量分数最高 |
分析 A.根据物质的组成来分析;
B.根据物质的构成来分析;
C.根据化合物中元素的质量比来分析;
D.根据化合物中各元素的质量比来分析.
解答 解:A.由化学式可知,青蒿素是由碳、氢、氧三种元素组成的,故正确;
B.青蒿素是由青蒿素分子构成的,1个青蒿素分子是由15个碳原子、22个氢原子和5个氧原子构成的,故错误;
C.青蒿素中C、H、O三种元素的质量比为(12×15):(1×22):(16×5)=90:11:40≠15:22:5,故错误;
D.青蒿素中C、H、O三种元素的质量比为(12×15):(1×22):(16×5)=90:11:40,由此可见其中碳元素的质量分数最大,故错误.
故选A.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
18.根据下列实验方案进行实验,能达到相应实验目的是( )
| A. |  比较Zn和Fe的金属活动性强弱 | B. | 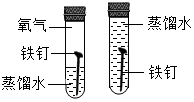 探究铁钉生锈时O2是否参与反应 | ||
| C. |  比较红磷和白磷的着火点 | D. |  测定空气中O2的含量 |
16.下列各组物质的俗称、学名与化学式表示同一种物质的是( )
| A. | 酒精 乙醇 C2H6O | B. | 纯碱 氢氧化钠 NaOH | ||
| C. | 熟石灰 氧化钙 CaO | D. | 铜绿 氢氧化铜 Cu2(OH)2CO3 |
3.某化学课外兴趣小组通过查阅资料知道过氧化钠(Na2O2)能与水反应生成氢氧化钠和氧气,于是他们做了以下探究实验.
实验1:向包有过氧化钠粉末的脱脂棉上滴水,脱脂棉燃烧起来.
请你对脱脂棉燃烧的原因进行分析过氧化钠和水反应生成的氧气和脱脂棉接触,同时放热使温度达到了脱脂棉的着火点.
实验2:向盛有过氧化钠粉末的试管中加入水,充分反应后,取试管中的少量溶液放入另一小试管中加入几滴无色酚酞试液,溶液变红,过了一会,红色又褪去了.
[提出问题]溶液为什么先变红,过了一会,红色又褪去了呢?
[猜想]甲同学认为是氢氧化钠溶液与空气中的二氧化碳反应的缘故,该反应的化学方程式为2NaOH+CO2═Na2CO3+H2O.乙同学认为甲同学的猜想不正确,理由是碳酸钠溶液显碱性,也能使酚酞试液变红色.
[查阅资料]①滴加酚酞呈现红色的溶液遇到H2O2时,H2O2可以破坏酚酞的结构,使酚酞在碱性溶液中不能再显红色;②酚酞在稀碱性溶液中稳定显红色,而在浓氢氧化钠等溶液中显红色后又褪色.
[猜想]通过查阅资料后,该兴趣小组对溶液的红色褪去的主要原因进行了猜想.
猜想A:过氧化钠与水反应可能生成了H2O2;猜想B:生成的氢氧化钠溶液可能太浓.
[实验探究]请你将下列实验方案填写完整
[得出结论]根据实验分析,过氧化钠与水反应除了生成氢氧化钠和氧气外,还存在另一反应,则另一反应的化学方程式为Na2O2+2H2O=2NaOH+H2O2.
实验1:向包有过氧化钠粉末的脱脂棉上滴水,脱脂棉燃烧起来.
请你对脱脂棉燃烧的原因进行分析过氧化钠和水反应生成的氧气和脱脂棉接触,同时放热使温度达到了脱脂棉的着火点.
实验2:向盛有过氧化钠粉末的试管中加入水,充分反应后,取试管中的少量溶液放入另一小试管中加入几滴无色酚酞试液,溶液变红,过了一会,红色又褪去了.
[提出问题]溶液为什么先变红,过了一会,红色又褪去了呢?
[猜想]甲同学认为是氢氧化钠溶液与空气中的二氧化碳反应的缘故,该反应的化学方程式为2NaOH+CO2═Na2CO3+H2O.乙同学认为甲同学的猜想不正确,理由是碳酸钠溶液显碱性,也能使酚酞试液变红色.
[查阅资料]①滴加酚酞呈现红色的溶液遇到H2O2时,H2O2可以破坏酚酞的结构,使酚酞在碱性溶液中不能再显红色;②酚酞在稀碱性溶液中稳定显红色,而在浓氢氧化钠等溶液中显红色后又褪色.
[猜想]通过查阅资料后,该兴趣小组对溶液的红色褪去的主要原因进行了猜想.
猜想A:过氧化钠与水反应可能生成了H2O2;猜想B:生成的氢氧化钠溶液可能太浓.
[实验探究]请你将下列实验方案填写完整
| 猜想 | 实验操作 | 实验现象 | 结论 |
| A | 取过氧化钠与水反应后的溶液放入试管中, 加入适量二氧化锰后,把带火星的木条放在试管口 | 带火星的木条复燃 | 猜想A 正确 |
| B | 取过氧化钠与水反应后的溶液放入试管中, 加入足量的水后,滴加酚酞试液 | 溶液变红,过了一会,红色又褪去了 | 猜想B 错误 |
13.氢化钙固体是登山运动员常用的能源提供剂.某探究小组的同学通过查阅资料得知,氢化钙(CaH2)与水反应生成氢氧化钙和氢气(CaH2+2H2O=Ca(OH)2+2H2↑),探究小组的同学把一定量的CaH2加入碳酸钠溶液中,充分反应后过滤,得到滤渣和滤液,经检验滤渣的成分是碳酸钙.
【提出问题】滤液中溶质的成分是什么?
【猜想与假设】
猜想一:NaOH 猜想二:NaOH、Ca(OH)2
猜想三:NaOH和Na2CO3 猜想四:NaOH、Na2CO3、Ca(OH)2
经过讨论,大家一致认为猜想四不合理,请用化学方程式说明原因:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
【实验验证】
【反思与拓展】
①若向NH4Cl的溶液中加一定量CaH2,充分反应,产生的气体是NH3和H2;(填化学式)
②登山运动员常用CaH2作为能源提供剂,与氢气相比,其优点是安全,固体便于携带.
【提出问题】滤液中溶质的成分是什么?
【猜想与假设】
猜想一:NaOH 猜想二:NaOH、Ca(OH)2
猜想三:NaOH和Na2CO3 猜想四:NaOH、Na2CO3、Ca(OH)2
经过讨论,大家一致认为猜想四不合理,请用化学方程式说明原因:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
【实验验证】
| 实验 | 现象 | 结论 |
| 实验一:取滤液,向其中滴入少量碳酸钠溶液 | 无明显现象 | 猜想二不成立 |
| 实验二:另取滤液,向其中加入足量稀盐酸 | 先无变化后产生气泡 | 猜想三成立 |
①若向NH4Cl的溶液中加一定量CaH2,充分反应,产生的气体是NH3和H2;(填化学式)
②登山运动员常用CaH2作为能源提供剂,与氢气相比,其优点是安全,固体便于携带.
20.A、B、C三种物质的溶解度曲线如图所示,下列分析不正确的是( )


| A. | t1℃时,A、C两种物质的饱和溶液中溶质的质量相等 | |
| B. | t2℃时,把50g水中能得到A的饱和溶液,其中溶质和溶液的质量比为1:3 | |
| C. | 将t2℃时,A、B、C三种物质的饱和溶液降温至t1℃时,所得溶液的溶质质量分数的大小关系是B>C=A | |
| D. | 将C的饱和溶液变为不饱和溶液,可采用降温的方法 |