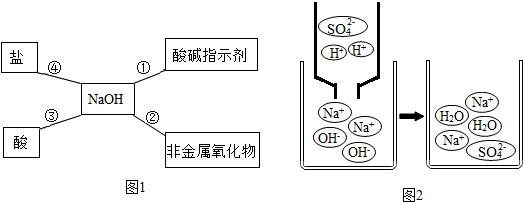
题目内容
13.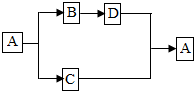 A~D都是初中化学中的常见物质,且有如图所示的转化关系(反应条件、部分反应物和生成物均已略去),请按照要求回答:
A~D都是初中化学中的常见物质,且有如图所示的转化关系(反应条件、部分反应物和生成物均已略去),请按照要求回答:(1)当A发生分解反应生成B和C时:①若C是最轻的气体,D是黑色固体,则C与D反应的化学方程式为4H2+Fe3O4$\frac{\underline{\;高温\;}}{\;}$3Fe+4H2O(或H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O);②若A是不溶于水的白色固体,D是改良酸性土壤的物质,则C与D反应的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O.
(2)若C与D发生化合反应时放出大量热,且C是相对分子质量最小的氧化物,则B的化学式为CaCO3.
分析 (1)当A发生分解反应生成B和C时:①若C是最轻的气体,则C是氢气,A是水,B为氧气;D是黑色固体,由氧气反应产生,则D可能是氧化铜或三氧化三铁;
②若A是不溶于水的白色固体,D是改良酸性土壤的物质,则A是碳酸钙,D是氢氧化钙,氢氧化钙和C反应产生碳酸钙,则C是二氧化碳,B是氧化钙,据此完成相关的问题;
(2)若C与D发生化合反应时放出大量热,且C是相对分子质量最小的氧化物,则C是水,D为氧化钙,A为氢氧化钙;氢氧化钙和二氧化碳等反应产生碳酸钙沉淀和水,碳酸钙分解产生氧化钙和二氧化碳,据此完成相关的问题.
解答 解:(1)当A发生分解反应生成B和C时:①若C是最轻的气体,则C是氢气,A是水,B为氧气;D是黑色固体,由氧气反应产生,则D可能是氧化铜或三氧化三铁,氢气和氧化铜、四氧化三铁反应产生铜、铁和水;故填:4H2+Fe3O4$\frac{\underline{\;高温\;}}{\;}$3Fe+4H2O(或H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O);
②若A是不溶于水的白色固体,D是改良酸性土壤的物质,则A是碳酸钙,D是氢氧化钙,氢氧化钙和C反应产生碳酸钙,则C是二氧化碳,B是氧化钙,氢氧化钙和二氧化碳反应产生碳酸钙沉淀和水;故填:CO2+Ca(OH)2═CaCO3↓+H2O;
(2)若C与D发生化合反应时放出大量热,且C是相对分子质量最小的氧化物,则C是水,D为氧化钙,A为氢氧化钙;氢氧化钙和二氧化碳等反应产生碳酸钙沉淀和水,碳酸钙分解产生氧化钙和二氧化碳,因此B为碳酸钙;故填:CaCO3.
点评 本考点属于图框式物质的推断题,在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

 名校课堂系列答案
名校课堂系列答案 A-E是初中化学常见的五种不同类别的物质,已知B为铁锈的主要成分,D是一种盐,其水溶液显碱性.它们相互之间的关系如图所示(图中“--”表示两端物质能反应,“→”表示物质间存在转化关系)下列说法正确的是( )
A-E是初中化学常见的五种不同类别的物质,已知B为铁锈的主要成分,D是一种盐,其水溶液显碱性.它们相互之间的关系如图所示(图中“--”表示两端物质能反应,“→”表示物质间存在转化关系)下列说法正确的是( )| A. | “B→A”反应一定是置换反应 | |
| B. | “C-D”反应的现象是产生白色沉淀 | |
| C. | “B-C”反应后溶液中的阳离子一定是亚铁离子 | |
| D. | “C-E”反应的微粒本质是氢离子与氢氧根离子结合生成水分子 |
| A. | 生成一氧化碳的质量为2.8g | |
| B. | 该有机物中可能含有氧元素 | |
| C. | 该物质在氧气中完全燃烧若只生成H2O和CO2,则该物质与氧气的化学计量系数之比为2:5 | |
| D. | 将反应后的物质通过氢氧化钠溶液,最后只得到一氧化碳气体 |
| 氢氧化钠 | 氯化钠溶液 | 碳酸钾溶液 | 硫酸钡溶液 | |
| 稀硫酸 | 能反应 | 不能反应 | 能反应 | 能反应 |
| 判断依据 | 有水生成 | 没有水、气体、沉淀生成 | 有气体和水生成 | 有沉淀生成 |
[实验方案]小丽同学设计实验方案进行探究,证明氢氧化钠溶液与稀硫酸发生了反应,请你和她一起完成实验报告.
| 实验操作 | 实验现象 |
| ①向试管中加入约2mL稀氢氧化钠溶液,滴加2滴酚酞溶液 | 溶液变为红色 |
| ②向①所得溶液中滴加过量稀硫酸 | 红色逐渐变浅至消失 |
[反思评价]小丽结合所学知识,认为初中常见的酸碱之间一定能发生复分解反应,她判断的依据是酸与碱生成盐和水,符合复分解反应发生的条件.
[拓展应用]为了测定某纯碱样品中碳酸钠的质量分数,取该样品与足量稀盐酸在烧杯中反应.有关实验数据如表.
| 反应前 | 反应后 | ||
| 实验数据 | 烧杯和稀盐酸的质量/g | 纯碱样品的质量/g | 烧杯和其中混合物的质量/g |
| 120 | 12 | 127.6 | |
| A. | Na+、H+、Cl-、HCO3- | B. | NH4+、Cu2+、NO3-、Cl- | ||
| C. | H+、Na+、OH-、SO42- | D. | Ag+、Ca2+、Cl-、NO3- |
 现有甲、乙、丙三种金属,采用将其中的一种金属分别放入另外两种金属的硫酸盐溶液中的方法进行实验,得到三种金属间的转化关系(如图所示).则三种金属的活动性由弱到强的顺序是( )
现有甲、乙、丙三种金属,采用将其中的一种金属分别放入另外两种金属的硫酸盐溶液中的方法进行实验,得到三种金属间的转化关系(如图所示).则三种金属的活动性由弱到强的顺序是( )| A. | 甲 丙 乙 | B. | 丙 甲 乙 | C. | 乙 甲 丙 | D. | 甲 乙 丙 |