题目内容
2.不锈钢材料中含有的金属铬(Cr)能提高钢的抗氧化性和耐腐蚀性,为了解金属铬与常见金属铝、铜在金属活动性顺序表中的相对位置关系,小娟与小涛分别进行了如下探究活动.【猜想和假设】根据所学知识,猜想三种金属在金属活动性顺序中的相对位置关系:
猜想一:Cr Al Cu; 猜想二:Al Cr Cu; 猜想三:Al Cu Cr.
【实验和探究】
(1)小娟的实验:取大小相同的铝、铬、铜三种金属片(用砂纸打磨光亮)
| 实验步骤 | 实验现象 | 解释与结论 |
| 分别取三支试管,向其中加入等质量、等浓度的稀硫酸,然后将铝、铬、铜三种金属片分别插入三支试管中 | 铝片表面产生气泡较快;铬片表面产生气泡较缓慢,溶液变蓝色;铜片无明显现象 | 猜想二成立. 铬与稀硫酸反应生成蓝色的硫酸亚铬(CrSO4),反应的化学方程式为Cr+H2SO4=CrSO4+H2↑ |
【归纳和总结】由上述实验得出比较金属活动性强弱的方法有:
①通过金属与酸反应比较;
②通过金属与盐溶液反应比较.
分析 【猜想和假设】根据铝和铜的金属活动性铝的强,再将铬加入出现三种情况:(1)Cr、Al、Cu;(2)Al、Cr、Cu;(3)Al、Cu、Cr解答.
【实验和探究】根据所学金属活动顺序可知铜不能与硫酸反应,铝可以与硫酸反应,进而解决问题.根据题中现象,写化学方程式进行.
(2)根据三种金属的活动性顺序选择药品,可选择两头金属中间盐,中间金属两头盐.
【归纳】根据金属和酸反应产生气泡的快慢、金属和盐溶液的反应判断金属性强弱.
解答 解:
【实验和探究】
根据实验现象:铝片表面产生的气泡较快;铬片表面产生气泡较缓慢,可知猜想二正确;
由题中信息可知,铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液,结合实验一有气泡产生,应该是氢气,根据质量守恒定律配平为:Cr+H2SO4═CrSO4+H2↑;
(2)如果已知三种金属的活动性顺序,用活动性位于中间的金属与另两种金属的盐溶液反应;或用活动性位于中间的金属的盐溶液与另两种金属反应,都可以验证三种金属的活动性顺序.故可选择:Al、CrSO4 、Cu或Al2(SO4)3、Cr、CuSO4等;
【总结与归纳】由上述实验得出比较金属活动性强弱的方法有①通过金属与酸反应比较;②通过金属与盐溶液反应比较.
故答案为:
【实验与探究】(1)二;Cr+H2SO4=CrSO4+H2↑;
(2)Al、CrSO4溶液、Cu;
【总结与归纳】
①金属与酸反应比较;
②金属与盐溶液反应比较
点评 本题考查的是金属的活动性顺序的探究,是近几年来中考考查的重点内容之一.本题型考查实验设计的同时,也考查了学生对实验设计题的评价能力,希望同学们认真把握.

练习册系列答案
相关题目
12. 甲同学对有关盐的知识进行了以下的整理.
甲同学对有关盐的知识进行了以下的整理.
(1)上述盐的排列是依据金属活动性顺序归纳整理的.
(2)上述盐因组成上相似而具有某些共同的化学性质,如都能与BaCl2溶液反应生成硫酸钡白色沉淀,试写出其中任意一种盐与BaCl2溶液反应的化学方程式为K2SO4+BaCl2=2KCl+BaSO4↓.
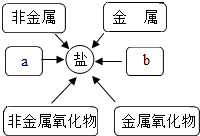
(3)甲同学通过查阅资料,发现许多反应都有盐类物质生成.他将这些知识间相互关系整理成右图,请将右图补充完整a酸,b碱(填物质的类别).
(4)乙同学提出可用右图指导进行物质的制备.请写出2个生成硫酸镁的化学反应方程式:Mg+H2SO4═MgSO4+H2↑;MgO+H2SO4═MgSO4+H2O.
 甲同学对有关盐的知识进行了以下的整理.
甲同学对有关盐的知识进行了以下的整理.| 硫酸钾 | 硫酸钙 | 硫酸钠 | 硫酸镁 | 硫酸铝 | 硫酸锌 | 硫酸亚铁 |
| K2SO4 | CaSO4 | Na2SO4 | MgSO4 | Al2(SO4)3 | ZnSO4 | FeSO4 |
(2)上述盐因组成上相似而具有某些共同的化学性质,如都能与BaCl2溶液反应生成硫酸钡白色沉淀,试写出其中任意一种盐与BaCl2溶液反应的化学方程式为K2SO4+BaCl2=2KCl+BaSO4↓.
(3)甲同学通过查阅资料,发现许多反应都有盐类物质生成.他将这些知识间相互关系整理成右图,请将右图补充完整a酸,b碱(填物质的类别).
(4)乙同学提出可用右图指导进行物质的制备.请写出2个生成硫酸镁的化学反应方程式:Mg+H2SO4═MgSO4+H2↑;MgO+H2SO4═MgSO4+H2O.
17.对“10%的NaCl溶液”的含义理解错误的是( )
| A. | 100g水中溶解了10gNaCl | |
| B. | 100gNaCl溶液中溶解有10gNaCl | |
| C. | 将5gNaCl溶解于45g水中所得到的溶液 | |
| D. | 将NaCl和水按1:9的质量比配成的溶液 |
7.下列物质在敞口的试剂瓶中放置一段时间后,发生化学变化质量增加的是( )
| A. | 浓盐酸 | B. | 浓硫酸 | C. | 氯化钠固体 | D. | 氢氧化钠固体 |
14.又到化学实验室开放日,老师拿出两瓶无标签的试剂,分别是一瓶固体和一瓶液体.他分别取了两种试剂各少量,在试管中混合,立即产生一种无色气体.此气体可能是什么物质?固体、液体分别是什么物质?试写出三种可能的情况,完成如表,要求气体不同:
| 气体成分 | 固体 | 液体 | |
| (1) | 氢气 | 锌粒 | 稀硫酸 |
| (2) | 二氧化碳 | 大理石 | 稀盐酸 |
| (3) | 氧气 | 二氧化锰 | 过氧化氢溶液 |
11.下列物质中,在装有氧气的集气瓶中燃烧能发出明亮的蓝紫色火焰的是( )
| A. | 铝箔 | B. | 铁丝 | C. | 硫粉 | D. | 木条 |
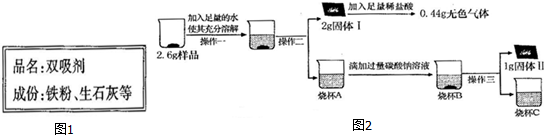
19.“双吸剂”是一种常见袋装食品的保鲜剂,能吸收空气中的氧气、二氧化碳、水蒸气 等.化学兴趣小组的同学在某食品袋中发现一包“双吸剂”,其标签如图1所示.同学们 对这包久置的“双吸剂”固体样品很好奇,设计实验进行探究.
【提出问题】久置“双吸剂”固体的成分是什么?
【查阅资料】
①铁与氯化铁溶液在常温下反应生成氯化亚铁
:Fe+2FeCl3═3FeCl2;
②碱性的Na2CO3溶液可以与中性的CaCl2溶液发生复分解反应.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【实验探究1】下表是小明设计的实验方案和记录的实验报告,请你补充完整.
【实验质疑】小组同学通过讨论认为实验并不能得出一定不含Fe2O3的结论,理由是Fe2O3+6HCl═2FeCl3+3H2O、Fe+2FeCl3=3FeCl2(用化学方程式表示).
为进一步确定这包久置的“双吸剂”固体的成分进行如下定量实验.
【实验探究2】取3g样品研碎,并用磁铁充分吸引后,得到剩余固体2.6g,按照图2流程进行实验,请回答相关问题:
(1)操作二、操作三名称是过滤.
(2)固体I的成分是CaCO3和Fe2O3.(填物质化学式,下同);
(3)烧杯A中溶液和加入的碳酸钠溶液反应的化学方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.

【提出问题】久置“双吸剂”固体的成分是什么?
【查阅资料】
①铁与氯化铁溶液在常温下反应生成氯化亚铁
:Fe+2FeCl3═3FeCl2;
②碱性的Na2CO3溶液可以与中性的CaCl2溶液发生复分解反应.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【实验探究1】下表是小明设计的实验方案和记录的实验报告,请你补充完整.
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量样品放入试管中,滴加一定量的稀盐酸.用带异營的单孔橡皮塞塞紧试管口,导管另 一端伸入澄清石灰水中. | 试管中固体逐漸减少,有大量无色气体产生,得到浅绿色溶液,澄清石灰水变浑浊. | 样品中一定含有Fe和CaCO3, 不含Fe2O3. |
| (2)取少量样品放入试管中,加水 溶解,静置后取上层清液滴加无 色酚酞试液. | 试管底部有不溶物,上层清液由无色变为红色. | 样品中含有氧化钙或氢氧化钙. |
为进一步确定这包久置的“双吸剂”固体的成分进行如下定量实验.
【实验探究2】取3g样品研碎,并用磁铁充分吸引后,得到剩余固体2.6g,按照图2流程进行实验,请回答相关问题:
(1)操作二、操作三名称是过滤.
(2)固体I的成分是CaCO3和Fe2O3.(填物质化学式,下同);
(3)烧杯A中溶液和加入的碳酸钠溶液反应的化学方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.