题目内容
4.依据下列要求,写出有关化学反应的化学方程式.(1)不能用铁制容器盛装硫酸铜溶液:Fe+CuSO4═FeSO4+Cu.
(2)市售打火机里装的不是汽油,而是液体丁烷(C4H10),丁烷在空气中燃烧后生成二氧化碳和水蒸气,写出丁烷完全燃烧的化学方程式:2C4H10+13O2$\frac{\underline{\;点燃\;}}{\;}$8CO2+10H2O.
(3)天然气(主要成分是CH4)用作燃料.CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O
(4)二氧化碳使澄清石灰水变浑浊.Ca(OH)2+CO2═CaCO3↓+H2O
(5)常温下,铝具有很好的抗腐性能,是因为铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜.4Al+3O2═2Al2O3.
分析 铁能和硫酸铜反应生成硫酸亚铁和铜;
丁烷燃烧生成水和二氧化碳;
甲烷燃烧生成水和二氧化碳;
澄清石灰水中含有氢氧化钙,氢氧化钙能和二氧化碳反应生成碳酸钙和水;
铝能和空气中的氧气反应生成氧化铝.
解答 解:(1)铁和硫酸铜反应的化学方程式为:Fe+CuSO4═FeSO4+Cu;
(2)丁烷燃烧的化学方程式为:2C4H10+13O2$\frac{\underline{\;点燃\;}}{\;}$8CO2+10H2O;
(3)甲烷燃烧的化学方程式为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
(4)二氧化碳和氢氧化钙反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O;
(5)铝和氧气反应的化学方程式为:4Al+3O2═2Al2O3.
故填:Fe+CuSO4═FeSO4+Cu;2C4H10+13O2$\frac{\underline{\;点燃\;}}{\;}$8CO2+10H2O;CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;Ca(OH)2+CO2═CaCO3↓+H2O;
4Al+3O2═2Al2O3.
点评 书写化学方程式要注意四步:一是反应物和生成物的化学式要正确;二是要遵循质量守恒定律,即配平;三是要有必要的条件;四是看是否需要“↑”或“↓”.

练习册系列答案
相关题目
14.如表呈现的是部分元素的原子结构示意图、主要化合价等信息.

下列叙述错误的是( )

下列叙述错误的是( )
| A. | 铝原子结构示意图的最外层有3个电子 | |
| B. | 元素最高正价与最低负价绝对值的和等于8 | |
| C. | 元素的正化合价数一定等于原子的最外层电子数 | |
| D. | 核电荷数分别为8和14的元素,组成化合物的化学式为SiO2 |
15.碳酸钾(K2CO3)和硝酸钾(KNO3)在不同温度时的溶解度及其溶解度曲线如下:
(1)图1中能表示KNO3溶解曲线的是甲(填“甲”或“乙”).
(2)曲线上M点的含义是在t1℃时甲和乙的溶解度相等.
(3)要配制100g 10%的KNO3溶液.溶液配制过程中,除用到玻璃棒、胶头滴管外,还需用到下列仪器中的ABD.(填字母编号)
A.托盘天平 B.烧杯 C.漏斗 D.量筒
(4)40℃时,向两个分别盛有相同质量的硝酸钾和碳酸钾的烧杯中,各加入100g水,充分溶解后,恢复至40℃,其结果如图2所示.下列有关说法中,正确的有AC.(填字母编号)
A.烧杯①中溶解的是KNO3,烧杯②中溶解的是K2CO3
B.烧杯②中溶液是不饱和溶液
C.升高温度或增加溶剂都有可能将烧杯①中固体全部溶解
D.若将烧杯①中的溶液变为不饱和溶液,溶液中溶质质量分数一定减小.
| 温度/℃ | 20 | 30 | 50 | 60 | 80 | |
| 溶解度g/100g水 | K2CO3 | 110 | 114 | 121 | 126 | 139 |
| KNO3 | 31.6 | 45.8 | 85.5 | 110 | 169 | |

(2)曲线上M点的含义是在t1℃时甲和乙的溶解度相等.
(3)要配制100g 10%的KNO3溶液.溶液配制过程中,除用到玻璃棒、胶头滴管外,还需用到下列仪器中的ABD.(填字母编号)
A.托盘天平 B.烧杯 C.漏斗 D.量筒
(4)40℃时,向两个分别盛有相同质量的硝酸钾和碳酸钾的烧杯中,各加入100g水,充分溶解后,恢复至40℃,其结果如图2所示.下列有关说法中,正确的有AC.(填字母编号)
A.烧杯①中溶解的是KNO3,烧杯②中溶解的是K2CO3
B.烧杯②中溶液是不饱和溶液
C.升高温度或增加溶剂都有可能将烧杯①中固体全部溶解
D.若将烧杯①中的溶液变为不饱和溶液,溶液中溶质质量分数一定减小.
12.下列符号中,既能表示一个原子,又能表示一种元素,还能表示一种物质的是( )
| A. | H | B. | O2 | C. | H2O | D. | Al |
19.某化学小组进行化学实验:鉴别澄清石灰水和氢氧化钠溶液.请你参与探究:
【提出问题】如何鉴别这两种无色溶液?
【实验方案】几位同学进行了如图所示的实验.

请你回答下列问题:
(1)C组实验中反应的现象为生成白色沉淀;
(2)其中不能达到实验目的是A、B(填字母);解释不能达到目的原因是:A方案都反应,但都无现象,故不能鉴别(如有多个,只答一点即可)
(3)D组实验中变浑浊的原溶液是澄清石灰水或Ca(OH)2溶液.
【继续探究】实验结束后,同学们将A、B、C、D四组试管中的物质全部 倒入同一个干净的烧杯中,充分反应后,得到无色澄清透明的溶液,对该溶液的成分又进行了探究.
【提出问题】该溶液中除水、酚酞外还含有哪些物质?
【查阅资料】氯化钙溶液呈中性.
【猜想与假设】
Ⅰ.NaCl、CaCl2
Ⅱ.NaCl、CaCl2、HCl
Ⅲ.NaCl、CaCl2、NaOH
【反思与拓展①上述猜想与假设中只有一个不合理,它是Ⅲ(填序号),理由是NaOH溶液能使无色酚酞试液变红,不能得到无色溶液.
②根据所学化学知识,验证烧杯内溶液中可能有的物质是否存在,下列哪些物质单独使用不能完成该实验b、d(填字母)
a.pH试纸 b.硝酸银溶液 c.紫色石蕊试液 d.铜 e.足量氢氧化钠溶液.
③经实验猜想(Ⅱ)成立,小明取烧杯内溶液,向其中加一种黑色氧化物,也得到同样是结论.请一起完成实验报告:
【提出问题】如何鉴别这两种无色溶液?
【实验方案】几位同学进行了如图所示的实验.

请你回答下列问题:
(1)C组实验中反应的现象为生成白色沉淀;
(2)其中不能达到实验目的是A、B(填字母);解释不能达到目的原因是:A方案都反应,但都无现象,故不能鉴别(如有多个,只答一点即可)
(3)D组实验中变浑浊的原溶液是澄清石灰水或Ca(OH)2溶液.
【继续探究】实验结束后,同学们将A、B、C、D四组试管中的物质全部 倒入同一个干净的烧杯中,充分反应后,得到无色澄清透明的溶液,对该溶液的成分又进行了探究.
【提出问题】该溶液中除水、酚酞外还含有哪些物质?
【查阅资料】氯化钙溶液呈中性.
【猜想与假设】
Ⅰ.NaCl、CaCl2
Ⅱ.NaCl、CaCl2、HCl
Ⅲ.NaCl、CaCl2、NaOH
【反思与拓展①上述猜想与假设中只有一个不合理,它是Ⅲ(填序号),理由是NaOH溶液能使无色酚酞试液变红,不能得到无色溶液.
②根据所学化学知识,验证烧杯内溶液中可能有的物质是否存在,下列哪些物质单独使用不能完成该实验b、d(填字母)
a.pH试纸 b.硝酸银溶液 c.紫色石蕊试液 d.铜 e.足量氢氧化钠溶液.
③经实验猜想(Ⅱ)成立,小明取烧杯内溶液,向其中加一种黑色氧化物,也得到同样是结论.请一起完成实验报告:
| 操作 | 实验现象 | 结论与化学方程式 |
| 取烧杯内溶液,向其中加入CuO (填化学式) | 溶液变蓝色 | 猜想(Ⅱ)成立; 化学反应方程式: CuO+2HCl=CuCl2+H2O |
9.为延缓袋装食品因缓慢氧化而变质,包装时不宜采用( )
| A. | 充入氮气 | B. | 充入氧气 | C. | 充入二氧化碳 | D. | 真空包装 |
16.下列图象与对应实验相符合的是( )
| A. | 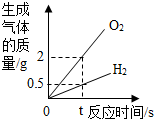 电解水实验 | |
| B. | 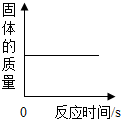 红磷在盛有氧气的密闭容器中燃烧 | |
| C. | 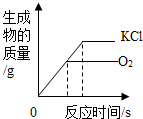 加热一定量的氯酸钾和二氧化锰固体 | |
| D. | 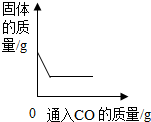 一氧化碳还原一定量氧化铁 |
14. 用如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验.已知:白磷的着火点为40℃.
用如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验.已知:白磷的着火点为40℃.
(1)H2O2稀溶液与MnO2接触时发生反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)实验1中,推入H2O2溶液前,燃烧匙和水中的白磷均没燃烧,燃烧匙中白磷没燃烧是因为未达到白磷的着火点,水中的白磷没燃烧是因为没有与O2接触; 推入H2O2溶液后,观察到烧杯中的现象是导管口有气泡冒出,白磷燃烧;
(3)实验2中,推入H2O2溶液后,观察到木炭燃烧得更剧烈,由此得出氧气的性质是助燃性;木炭熄灭后冷却一段时间,烧杯中的部分溶液流入集气瓶.在实验2的整个过程中,集气瓶内压强的变化过程是先增大后减小.
 用如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验.已知:白磷的着火点为40℃.
用如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验.已知:白磷的着火点为40℃.| 内容步骤 | 【实验1】研究燃烧条件 | 【实验2】研究氧气性质 |
Ⅰ | 烧杯中盛有80℃的热水,分别在燃烧匙和烧杯中导管口放置一小块白磷,塞紧瓶塞 | 烧杯中盛有NaOH溶液,燃烧匙中放入木炭 点燃木炭后,迅速将燃烧匙伸入瓶中,塞紧瓶塞 |
| Ⅱ | 推入适量H2O2 溶液 | 推入适量H2O2 溶液 |
(2)实验1中,推入H2O2溶液前,燃烧匙和水中的白磷均没燃烧,燃烧匙中白磷没燃烧是因为未达到白磷的着火点,水中的白磷没燃烧是因为没有与O2接触; 推入H2O2溶液后,观察到烧杯中的现象是导管口有气泡冒出,白磷燃烧;
(3)实验2中,推入H2O2溶液后,观察到木炭燃烧得更剧烈,由此得出氧气的性质是助燃性;木炭熄灭后冷却一段时间,烧杯中的部分溶液流入集气瓶.在实验2的整个过程中,集气瓶内压强的变化过程是先增大后减小.